
【题目】某无色溶液中,可大量共存的离子组是
A.Cu2+、NO3-、Cl-、SO42-B.H+、Cl-、K+、CO32-
C.Na+、HCO3-、SO42-、Cl-D.K+、Mg2+、SO42-、OH-
科目:高中化学 来源: 题型:
【题目】随着社会经济的发展,人们生活水平的提高和对环境要求的加强,来源广泛的高氨氮废水(主要含有NH4+)处理越来越受到重视。对于高氨氮废水的处理有多种方法。
(1)吹脱法:
![]()
使用吹脱法时需要在①中加入碱,写出发生的离子反应方程式______________________。
(2)MAP沉淀法:
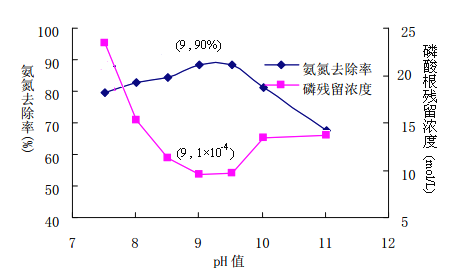
①使用化学沉淀剂处理高氨氮废水时,向高氨氮废水中投入含有Mg2+的物质和H3PO4,调节溶液pH,与NH4+反应生成MgNH4PO4(MAP)沉淀。为有效控制溶液PH,并考虑污水处理效果,则最好选用下列物质中_____。
A MgO B MgSO4 C MgCl2
②控制溶液PH的合理范围为____________________
③从溶解平衡角度解释PH过高或过低不易形成沉淀MAP的原因(已知PO43-在酸性较强条件下以HPO42-形式存在)_______________
(3)生物脱氮传统工艺:
①在有氧气的条件下,借助于好氧微生物(主要是好氧菌)的作用生成NO3-,写出反应的离子方程式_________________________。
②在无氧的酸性条件下,利用厌氧微生物(反硝化菌)的作用使NO3-与甲醇作用生成N2,达到净化水的目的。写出离子方程式____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家设计了一种双室微生物燃料电池,以苯酚(C6H6O)为燃料,同时可除去酸性废水中的硝酸盐。下列说法正确的是
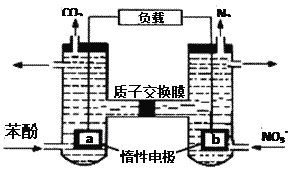
A. a极的电极反应式为C6H6O+11H2O + 28e-=6CO2↑ + 28H+
B. 外电路电子移动方向由b极到a极
C. 若正极产生5.6L气体(标况下),则转移电子2.5mol
D. 电池工作一段时间后,左池溶液的pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有六种短周期元素,已知A的单质是最清洁的能源物质,其他元素的原子半径及主要化合价如下表:
元素代号 | B | C | D | E | F |
原子半径/nm | 0.186 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +1 | +3 | +6、-2 | +7、-1 | -2 |
根据上述信息回答以下问题。
(1)D在元素周期表中的位置______________;E的离子结构示意图______________。
(2)关于A元素在周期表中的位置,一直存在纷争,有人主张把它放在第ⅦA族,试分析其理由________________________________。
(3)用电子式表示B的单质与D的单质形成化合物的过程________________________。
(4)下列各项比较,正确的是________________________。
①氢化物的沸点:D低于F ②A~F元素的简单离子半径:C的最大
③气态氢化物稳定性:D比E稳定 ④最高价氧化物对应的水化物碱性:B小于C
(5)E单质常用于自来水消毒。用必要的文字和离子方程式解释原因______________________________________________________________。
(6)写出C的单质与B的最高价氧化物的水化物反应的离子方程式________________。
(7)C的单质与元素M的红棕色氧化物N反应可用于焊接钢轨,该反应的化学方程式为________________________________。
(8)已知单质M的燃烧热为375kJ/mol,写出表示其燃烧热的热化学方程式___________________________。
(9)已知NH3结合质子的能力强于F的氢化物,请用最恰当的离子方程式证明这个结论________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为M的气态化合物VL(标准状况)溶于mg水中,得到溶液的质量分数为ω%,物质的量浓度cmol/L,密度为ρg/cm3,则下列说法正确的是
A. 相对分子质量M可表示为:![]()
B. 溶液密度ρ可表示为:![]()
C. 溶液的质量分数ω%可表示为:![]()
D. 物质的量浓度C可表示为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.某学习小组做Na2O2与H2O反应的实验,发现一些有趣的现象:
①取适量Na2O2固体用脱脂棉包好放在石棉网上,然后向脱脂棉上滴加3-4滴水,结果脱脂棉剧烈燃烧。
②取适量Na2O2固体置于试管中,加水使其充分反应至不再产生气体为止,滴入几滴酚酞试液,溶液先变红后褪色。回答有关问题。
(1)写出Na2O2的电子式_______________________。
(2)已知Na2O2可看作二元弱酸H2O2对应的盐,其第一步水解完全进行。写出其第一步水解的离子方程式为___________________________________。
(3)由①实验现象所得出的有关结论是:a.有氧气生成;b.___________________。
(4)Na2O2与H2O反应的离子方程式____________________________________。
II.为探究Na2O2与H2O反应的机理,他们在老师的指导下设计了下图所示装置。连接好装置,打开K1、K2,通过注射器注入适量蒸馏水,充分反应后用气球鼓气,Na2S溶液变浑浊,酸性KMnO4溶液褪色。分别取A、C中溶液滴入几滴酚酞,开始都变红,以后A中溶液很快褪色,C中溶液缓慢褪色。另取A、C中溶液分别加入少量二氧化锰,充分振荡,发现均反应剧烈、产生大量气泡,把带火星的木条伸入试管,木条复燃,向反应后的溶液中滴入几滴酚酞试液,溶液变红不褪色。
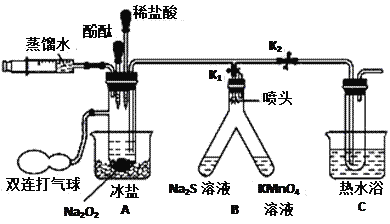
(5)A中冰盐和C中热水的作用分别是__________________,___________________。
(6)用化学方程式表示Na2S变浑浊的原因___________________________________。
(7)用离子方程式表示KMnO4溶液褪色的原因(MnO4-在酸性条件下被还原成Mn2+)__________________________________________。
(8)Na2O2与H2O反应的机理是(用化学方程式表示)第一步_____________________,第二步_______________________________。
(9)若向Na2O2中滴加适量的稀盐酸,也能产生同样的气体,请写出该反应的化学方程式___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关金属晶体的说法中,正确的是( )
A. 简单立方堆积的晶胞中原子配位数是8
B. 晶胞中配位数为12的金属,一定是面心立方最密堆积
C. Zn的晶胞类型与铜相同
D. 铁的晶胞中空间利用率为68%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,有以下三种物质:①18 g H2O;②11.2 L H2S气体;③0.5 mol C2H5OH(酒精)。下列排列顺序正确的是
A. 密度:①>③>② B. 体积:①>③>②
C. 质量:③>②>① D. 氢原子数:①>②>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com