

分析 海水提取氯化钠后得到苦卤,在卤水中通入氯气氧化溴在为溴单质,得到含溴单质的海水混合物Ⅰ,利用热空气和溴单质的挥发性吹出溴单质,得到含溴的空气,再用二氧化硫吸收得到吸收液,通入氯气氧化富集溴,得到溴水混合物Ⅱ,蒸馏得到溴蒸气冷凝分离得到液溴,
(1)步骤①获得Br2的离子反应是氯气氧化溴离子生成溴单质;
(2)步骤③所发生反应是溴单质和二氧化硫在水溶液中发生氧化还原反应生成硫酸和溴化氢,反应中元素化合价降低的物质做氧化剂,依据电子守恒和化学方程式定量关系计算电子转移总数;
(3)根据氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性进行判断;
(4)液溴易挥发分析;
(5)在溴水中,溴的沸点是58.5°C,水的是100°C,温度80℃-90℃时,水不沸腾而溴蒸气挥发;
(6)根据分液是分离两种不相溶的液体,用分液漏斗分离;
(7)海水中溴离子的浓度较少,在海水提取溴之前,必须进行海水浓缩以节约成本;
解答 解:(1)步骤①获得Br2的离子反应是氯气氧化溴离子生成溴单质,反应的离子方程式Cl2+2Br-═Br2+2Cl-,
故答案为:Cl2+2Br-═Br2+2Cl-;
(2)步骤③所发生反应是溴单质和二氧化硫在水溶液中发生氧化还原反应生成硫酸和溴化氢,反应的化学方程式为:Br2+SO2+2H2O═2HBr+H2SO4,反应中元素化合价降低的物质做氧化剂,负值溴单质中溴元素化合价降低,所以Br2为氧化剂,依据电子守恒和化学方程式定量关系计算电子转移总数,若反应中生成2molHBr,转移电子物质的量为2mol,则转移电子数约为2mol×6.02×1023/mol=1.204×1024,
故答案为:Br2+SO2+2H2O═2HBr+H2SO4; Br2; 1.204×1024;
(3)根据以上分析可知,氯气能够将溴离子氧化成溴单质,溴单质能够氧化二氧化硫,则说明氧化性强弱为:Cl2>Br2>SO2,
故答案为:Cl2>Br2>SO2;
(4)步骤②通入热空气或水蒸气吹出Br2,利用的是液溴易挥发,故选C,
故答案为:C;
(5)在溴水中,溴的沸点是58.5°C,水的是100°C,温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低,
故答案为:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
(6)由于液溴与溴水不相溶,可用分液漏斗分离,
故答案为:分液漏斗;
(7)海水中溴离子的含量较少,在海水提取溴之前,必须进行海水浓缩,:“空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低;
故答案为:空气吹出、SO2吸收、氯化”的过程实际上是一个Br2的浓缩过程,与直接蒸馏含Br2海水相比效率更高,消耗能源少,成本降低;
点评 本题考查了海水资源的综合利用,题目难度中等,把握流程中发生的化学反应及混合物分离方法为解答的关键,注意掌握海水资源及其综合应用方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:解答题
| 1 | 2 | 3 | |
| 空白试验消耗硫酸铈标准溶液的体积(ml) | 0.75 | 0.50 | 0.80 |
| 0.25克样品消耗硫酸铈标准溶液的体积(ml) | 24.65 | 24.75 | 24.70 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
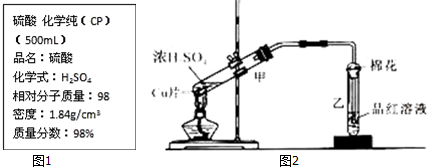
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
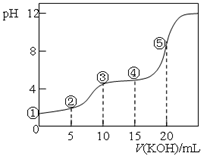 常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )
常温下,用0.10mol•L-1 KOH溶液滴定 10.00mL 0.10mol•L-1H2C2O4(二元弱酸)溶液 所得滴定曲线如图(混合溶液的体积可看成混合前溶液的体积之和).下列说法正确的是( )| A. | 点①所示溶液中:c(H+)/c(OH-)=1012 | |
| B. | 点②所示溶液中:c(K+)+c(H+)=c(HC2O4-)+c(C2O42-)+c(OH-) | |
| C. | 点③所示溶液中:c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.05mol•L-1 | |
| D. | 点⑤所示溶液中:c(K+)>c(HC2O4-)>c(C2O42-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径大小:Na>S>O | B. | 还原性强弱:F->Cl->Br->I- | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 气态氢化物稳定性:HBr>HCl>HF |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
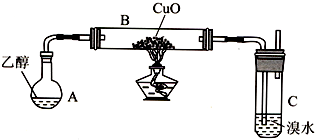
| 试剂、用品 | 预期现象 | |
| 甲 | 酸性高锰酸钾溶液 | 溶液紫红色褪去 |
| 乙 | 溴水 | 溴水褪色 |
| 丙 | 铜丝 酒精灯 | 铜丝由黑色变成光亮的红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

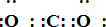 ;写出物质E的电子式:
;写出物质E的电子式: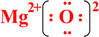 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
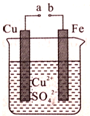
| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为Cu2++2eˉ=Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b用导线连接时,电流从铁片经导线流向铜片 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 NaCl
NaCl .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com