
【题目】能够说明氯的非金属性比硫强的反应是( )
A. CuCl2+H2S===CuS↓+ 2HCl
B. Cl2+ H2S===2HCl+ S
C. 3Cl2+6FeSO4===2Fe2(SO4)3+2FeCl3
D. H2SO4(浓)+ NaCl(固)===NaHSO4+ HCl
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染,生产流程如下: 
已知石油裂解已成为生产H的主要方法,E的溶液能发生银镜反应,G是具有香味的液体,试填空.
(1)A的名称;G的名称;
(2)B的结构简式;H的结构简式;
(3)写出H发生加聚反应的方程式:;
(4)D→E的化学方程式:;
(5)E→F的化学方程式:;
(6)F→G的化学方程式;
(7)写出G的一种与CH3COOH互为同系物的同分异构体的结构简式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下自发反应能用ΔH判据来解释的是( )
A. 硝酸铵自发地溶于水
B. 2N2O5(g)===4NO2(g)+O2(g) ΔH=+156.7 kJ·mol-1
C. (NH4)2CO3(s)===NH4HCO3(s)+NH3(g) ΔH=+74.9 kJ·mol-1
D. 2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g) ![]() 2Z(g),此反应达到平衡状态的标志是( )
2Z(g),此反应达到平衡状态的标志是( )
A. 容器内气体密度不随时间变化 B. 容器内各物质的浓度不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2 D. 单位时间内消耗0.1 mol X,同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)25℃时,0.005mol/LH2SO4溶液的pH=______ ,0.001mol/LNaOH溶液的pH=______ 。
(2)某温度下纯水的c(H+)=2.0×10-7mol/L,则此溶液中的c(OH-)=_______;若温度不变,滴入稀盐酸,使c(H+)=5.0×10-4mol/L,则此溶液中由水电离产生的c(H+)=_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 氧化还原反应的本质是元素化合价的升降
B. 氧化还原反应一定有氧元素参加
C. 氧化反应一定先于还原反应
D. 发生氧化反应的物质也可能同时发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间通过一步反应不能实现右图所示转化的是()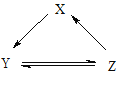
项目 | X | Y | Z |
A | Si | SiO2 | H2SiO3 |
B | Na | NaOH | NaCl |
C | NO | NO2 | HNO3 |
D | NaClO | HClO | Cl2 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是()
A. CO、NO、NO2都是大气污染气体,在空气中都能稳定存在,都不是酸性氧化物
B. N2+3H2![]() 2NH3、N2+O2
2NH3、N2+O2![]() 2NO都属于氮的固定,且N2都表现还原性
2NO都属于氮的固定,且N2都表现还原性
C. 向BaCl2溶液中加入Na2SO3产生沉淀,再通入NO2,沉淀完全溶解
D. 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,该溶液一定含有NH![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)2NH3(g)
(1)若反应进行到某时刻t时,n1(N2)=13mol,n1(NH3)=6mol,计算a的值.
(2)反应达平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的含量(体积分数)为25%.计算平衡时NH3的物质的量.
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同).n1(始):n1(平)= .
(4)原始混合气体中,a:b= .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com