
【题目】福莫特罗是一种治疗哮喘病的药物,它的关键中间体(G)的合成路线如下:

回答下列问题:
(1)F的分子式为_____________,反应①的反应类型为_________。
(2)反应④的化学方程式为___________________________。
(3)C能与FeC13 溶液发生显色反应,C的结构简式为________________, D中的含氧官能团为_________________。
(4)B的同分异构体(不含立体异构)中能同时满足下列条件的共有_____种。
a.能发生银镜反应 b.能与NaOH溶液发生反应 c.含有苯环结构
其中核磁共振氢谱显示为4组峰,且峰面积比为3:2:2:1的是________________(填结构简式)。
(5)参照G的合成路线,设计一种以![]() 为起始原料(无机试剂任选)制备的
为起始原料(无机试剂任选)制备的![]() 合成路线________。
合成路线________。
【答案】C15H12NO4Br 取代反应 ![]() +
+
![]()
 +HCl
+HCl ![]() 羟基、羰基和硝基 17
羟基、羰基和硝基 17 ![]()
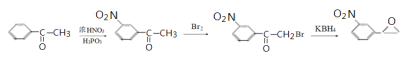
【解析】
由D的分子式与E的结构可知,D与![]() 发生取代反应生成E,则D为
发生取代反应生成E,则D为 ,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为
,C能与FeCl3溶液发生显色反应,含有酚羟基,结合C的分子式逆推可知C为 ,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为
,A的分子式为C6H6O,A与乙酸酐反应得到酯B,B在氯化铝作用下得到C,则A为![]() ,B为
,B为![]() .E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F。据此分析解答。
.E与溴发生取代反应生成F,相当于E中羰基还原为羟基,再发生取代反应得到F。据此分析解答。
(1)F( )的分子式为:C15H12NO4Br,反应①是
)的分子式为:C15H12NO4Br,反应①是![]() 与(CH3CO)2O反应生成
与(CH3CO)2O反应生成![]() 与CH3COOH,属于取代反应,故答案为:C15H12NO4Br;取代反应;
与CH3COOH,属于取代反应,故答案为:C15H12NO4Br;取代反应;
(2)反应④的化学方程式为:![]() +
+
![]()
 +HCl,故答案为:
+HCl,故答案为:![]() +
+
![]()
 +HCl;
+HCl;
(3)根据上述分析,C的结构简式为  ,D的结构简式为
,D的结构简式为 ,其中的含氧官能团有:羰基、羟基、硝基,故答案为:
,其中的含氧官能团有:羰基、羟基、硝基,故答案为: ;羰基、羟基、硝基;
;羰基、羟基、硝基;
(4)B(![]() )的同分异构体(不含立体异构)能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能与NaOH溶液发生反应,说明含有酯基或酚羟基,c.含有苯环结构,若为甲酸形成的酯基,含有1个取代基,可以为甲酸苯甲酯,含有2个取代基为-CH3、-OOCH,有邻、间、对3种,若含有醛基、酚羟基,含有2个取代基,其中一个为-OH,另外的取代基为-CH2CHO,有邻、间、对3种,含有3个取代基,为-OH、-CH3、-CHO,当-OH、-CH3处于邻位时,-CHO有4种位置,当-OH、-CH3处于间位时,-CHO有4种位置,当-OH、-CH3处于对位时,-CHO有2种位置,符合条件的同分异构体共有17种,其中核磁共振氢谱显示为4组峰,且峰面积比为3∶2∶2∶1的是
)的同分异构体(不含立体异构)能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能与NaOH溶液发生反应,说明含有酯基或酚羟基,c.含有苯环结构,若为甲酸形成的酯基,含有1个取代基,可以为甲酸苯甲酯,含有2个取代基为-CH3、-OOCH,有邻、间、对3种,若含有醛基、酚羟基,含有2个取代基,其中一个为-OH,另外的取代基为-CH2CHO,有邻、间、对3种,含有3个取代基,为-OH、-CH3、-CHO,当-OH、-CH3处于邻位时,-CHO有4种位置,当-OH、-CH3处于间位时,-CHO有4种位置,当-OH、-CH3处于对位时,-CHO有2种位置,符合条件的同分异构体共有17种,其中核磁共振氢谱显示为4组峰,且峰面积比为3∶2∶2∶1的是 ![]() ,故答案为:17;
,故答案为:17;![]() ;
;
(5)模仿E→F→G的转化, 发生硝化反应生成
发生硝化反应生成 ,然后与溴发生取代反应生成
,然后与溴发生取代反应生成![]() ,最后在NaBH4条件下反应生成
,最后在NaBH4条件下反应生成 ,合成路线流程图为:
,合成路线流程图为:![]() ,故答案为:
,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. MgCO3![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
B. H2SO4(浓)![]() SO2
SO2![]() BaSO3(s)
BaSO3(s)
C. NaAlO2![]() AlCl3(aq)
AlCl3(aq)![]() AlCl3(s)
AlCl3(s)
D. NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌锰电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2。下列有关说法错误的是( )
A.锌为负极材料
B.该电解质溶液可能是稀硫酸
C.正极反应式为MnO2+H2O+e-=MnOOH+OH-
D.消耗13g锌时电路中转移电子的物质的量为0.4mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气及许多含氯化合物是生产、生活中应用非常广泛的物质。磺酰氯(SO2Cl2)是实验室中常见试剂。已知:SO2Cl2(g)![]() SO2(g)+Cl2(g)
SO2(g)+Cl2(g)
(1)在2 L恒容密闭耐腐蚀性的容器中充入0.1 mol SO2Cl2(g)发生反应,在101 kPa、375K条件下进行该反应,SO2Cl2的转化率与时间关系如图所示。
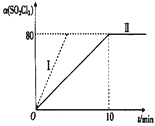
①平衡时,容器内压强p=_________________。
②相对曲线Ⅱ对应实验,仅改变一个条件得到曲线I,曲线I改变的条件可能是_____________________。
(2)一定量氯气用饱和纯碱溶液吸收恰好只生成三种盐(不产生气体),该溶液中阴离子浓度大小顺序为______________________________________________________。
(3)已知:常温下,次氯酸(HClO)的电离常数Ka=2.5×10-8,则在该温度下,NaClO水解反应的水解常数Kh为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池是燃料(如氢气、甲烷、一氧化碳等)跟氧气(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱溶液。下面关于甲烷燃料电池的说法正确的是( )
A. 负极反应式:O2+2H2O+4e-![]() 4OH-
4OH-
B. 负极反应式:CH4+8OH--8e-![]() CO2+6H2O
CO2+6H2O
C. 随着放电的进行,溶液中氢氧根离子的浓度不变
D. 放电时溶液中的阴离子向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】求下列溶液的pH(常温条件下,已知lg2=0.3,lg5=0.7,lg5.5=0.74)
(1)0.0005mol/L的硫酸溶液pH=________.(2)0.0005mol/L的氢氧化钠溶液pH=_________.
(3)把10ml,pH=12的氢氧化钡加水稀释到1LpH=______________.
(4)将pH=1的盐酸和pH=4的硫酸等体积混合pH=_______________.
(5)将pH=1的盐酸aL和pH=11的氢氧化钠bL溶液混合,若混合液为中性,则a:b=_______.
(6)将pH=3与pH=4的稀硫酸等体积混合时,混合后溶液的pH=_________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃时,向50.00mL未知浓度的氨水中逐滴加入0.5mol·L-1的HC1溶液。滴定过程中,溶液的pOH[pOH=-lgc(OH-)]与滴入HCl溶液体积的关系如图所示,则下列说法中正确的是
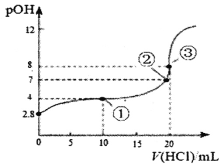
A. 图中②点所示溶液的导电能力弱于①点
B. ③点处水电离出的c(H+)=1×10-8mol·L-1
C. 图中点①所示溶液中,c(C1-)>c(NH4+)>c(OH-)>c(H+)
D. 25℃时氨水的Kb约为5×10-5.6mo1·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中烧杯中盛的是天然水,铁腐蚀的速率由快到慢的顺序是( )

A. ③>②>①>⑤>④ B. ⑤>②>①>③>④ C. ⑤>②>③>④>① D. ③>④>⑤>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,相同体积的0.5mol·L-1的下列四种溶液:①KCl溶液、②FeCl3溶液、③HF溶液、④Na2CO3溶液,其中所含阳离子数由多到少的顺序是( )
A. ④>①=②>③ B. ①>④>②>③ C. ④>①>③>② D. ④>②>①>③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com