
| A. | 过量的铁与稀H2SO4反应 | B. | FeO与H2SO4反应 | ||
| C. | FeCO3与H2SO4稀反应 | D. | Fe(OH)3与稀H2SO4反应 |
分析 A.无论Fe是否过量,Fe和稀硫酸都只生成硫酸亚铁;
B.FeO和稀硫酸反应生成硫酸亚铁和水;
C.碳酸铁和稀硫酸反应生成硫酸亚铁、二氧化碳和水;
D.氢氧化铁和稀硫酸反应生成硫酸铁和水.
解答 解:A.无论Fe是否过量,Fe和稀硫酸都只生成硫酸亚铁,过量的Fe和稀硫酸反应生成硫酸亚铁和氢气,且稀硫酸没有剩余,所以该方法制备较适宜,故A选;
B.FeO和稀硫酸反应生成硫酸亚铁和水,稀硫酸如果过量导致溶液中溶质有两种,故B不选;
C.碳酸铁和稀硫酸反应生成硫酸亚铁、二氧化碳和水,如果稀硫酸过量导致溶液中溶质有两种,故C不选;
D.氢氧化铁和稀硫酸反应生成硫酸铁和水,如果稀硫酸过量,导致溶液中溶质有两种,故D不选;
故选A.
点评 本题以物质制备为载体考查化学实验方案评价,为高频考点,明确物质性质及物质量的多少是解本题关键,为易错题.


 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:选择题
| A. | 钠与乙醇反应比与水反应剧烈 | |
| B. | 常温下可用铝制容器贮存稀硝酸 | |
| C. | 干燥的氯气具有漂白性 | |
| D. | 用氯化铁溶液与铜反应制印刷电路板 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol H2 | B. | 0.5molNH3 | ||
| C. | 6.02×1023个的CH4分子 | D. | 29.4gH3PO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和④ | B. | ②和③ | C. | ④和⑤ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.45mol | B. | 0.35mol | C. | 0.4mol | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
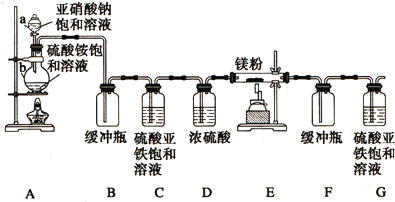
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
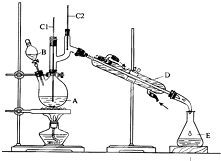 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
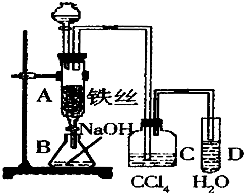 某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.
某化学课外小组用如图装置制取溴苯.先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe0溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | 明矾溶液中滴加过量氨水:Al3++3NH3.H2O═Al(OH)3↓+3NH${\;}_{4}^{+}$ | |
| C. | 漂白粉溶液中通入S02:Ca2++2ClO-+SO2+H2O═2HClO+CaSO3↓ | |
| D. | 小苏打溶液中加足量澄清石灰水:2HCO${\;}_{3}^{-}$+Ca2++2OH-═CaCO3↓+2H2O+CO${\;}_{3}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com