
����Ŀ����ˮ�а�̬����NH3��H2O��NH3��NH4+����ʽ���ڣ���ˮ�ѵ��ѳ�Ϊ��Ҫ��Ⱦ����ź�ˮ�帻Ӫ�������ε��о��ȵ㡣
������
���ˮ��Ͷ��MgCl2��Na2HPO4������MgNH4PO4��6H2O�������ɽ���̬����������10mg��L1���¡�
��1��NH3�ĵ���ʽ��______��
��2����ˮ�е�NH3��H2Oת��ΪMgNH4PO4��6H2O�����ӷ���ʽ��______��

��3��16��ʱ�����ˮ�м���MgCl2��Na2HPO4��ʹþ�����������ʵ���֮��Ϊ1�U1�U1�����������е�pH��ʣ�ఱ̬��Ũ�ȵ�Ӱ����ͼ����ʹʣ�ఱ̬��Ũ�ȵ���10mg��L1��pH�����˷�Χ��______��pHƫ�����ƫС��������MgNH4PO4��6H2O�����ɡ�
����������
��4����ЭͬCuO��H2O2��ȥ��̬��
������������ͬ��ȡ��ͬ�����ͬһ��ˮ��Ʒ����10 min��ʣ�ఱ̬��Ũ����һ��Ũ��H2O2��Һ�������Ĺ�ϵ����ͼ����ͼ�Ʋ�CuO�ڰ�̬���ѳ��п���������ã�����_____________

����ЭͬCuO������H2O2��ȥ��̬�����������£�H2O2��NH3����ΪN2�Ļ�ѧ����ʽ��____________________��
���𰸡�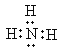 Mg2+ + NH3��H2O+HPO42 + 5H2O = MgNH4PO4��6H2O�� pH��8~10�� pHƫ�� NH4+��Mg2+����OH�������NH3��H2O��Mg(OH)2�� NH3��H2O�ĵ��뱻���ƣ�ʹNH4+��Mg2+Ũ�Ƚ��ͣ�pHƫС��������HPO42���룬PO43Ũ��ƫ�͡�����pHƫ���ƫС��������MgNH4PO4��6H2O�����ɣ� ��ͬ��H2O2��Һ����������ͬʱ���ڣ��벻��CuO��ȣ�����CuO����̬��Ũ�Ƚ��͵Ķ࣬��Ӧ���ʿ� 3H2O2+ 2NH3
Mg2+ + NH3��H2O+HPO42 + 5H2O = MgNH4PO4��6H2O�� pH��8~10�� pHƫ�� NH4+��Mg2+����OH�������NH3��H2O��Mg(OH)2�� NH3��H2O�ĵ��뱻���ƣ�ʹNH4+��Mg2+Ũ�Ƚ��ͣ�pHƫС��������HPO42���룬PO43Ũ��ƫ�͡�����pHƫ���ƫС��������MgNH4PO4��6H2O�����ɣ� ��ͬ��H2O2��Һ����������ͬʱ���ڣ��벻��CuO��ȣ�����CuO����̬��Ũ�Ƚ��͵Ķ࣬��Ӧ���ʿ� 3H2O2+ 2NH3![]() N2+6H2O
N2+6H2O
��������
(1)NH3�ĵ���ʽΪ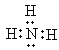 ��
��
(2)�������⣬��ˮ�е�NH3��H2Oת��ΪMgNH4PO4��6H2O����Ӧ�����ӷ���ʽΪMg2+ + NH3��H2O+HPO42 + 5H2O = MgNH4PO4��6H2O����
(3)��ͼ���Կ�������ʹʣ�ఱ̬��Ũ�ȵ���10mg��L1��pH���˷�ΧΪ8~10��pHƫ�� NH4+��Mg2+����OH�������NH3��H2O��Mg(OH)2�� NH3��H2O�ĵ��뱻���ƣ�ʹNH4+��Mg2+Ũ�Ƚ��ͣ�pHƫС��������HPO42���룬PO43Ũ��ƫ�͡�����pHƫ���ƫС��������MgNH4PO4��6H2O�����ɣ�
(4)����ͼ��֪������ͬʱ���H2O2��Һ��������ͬʱ��������CuO�ķ�Ӧ���ʽϿ죬��̬����ʣ��Ũ��ԶԶС��δ����CuO��
![]() �ڸ�����������������ЭͬCuO�����£�H2O2��NH3����N2����Ӧ�ķ���ʽΪ3H2O2+ 2NH3
�ڸ�����������������ЭͬCuO�����£�H2O2��NH3����N2����Ӧ�ķ���ʽΪ3H2O2+ 2NH3![]() N2+6H2O��
N2+6H2O��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(VB2)-������ع���ʱ��ӦΪ��4VB2+11O2 = 4B2O3+2V2O5���øõ��Ϊ��Դ��ѡ�ö��Ե缫�������ͭ��Һ��ʵ��װ����ͼ��ʾ�������·��ͨ��0.04mol����ʱ��Bװ���ڹ��ռ���0.448L����(��״��)��������˵����ȷ����(�� ��)
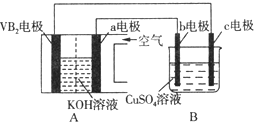
A. VB2�缫�����ĵ缫��ӦΪ��2VB2+11H2O-22e- = V2O5+2B2O3+22H+
B. ���·�е�����c�缫����VB2�缫
C. �������У�c�缫�������к�ɫ����������Ȼ�������ݲ���
D. ��Bװ���ڵ�Һ�����Ϊ100mL����CuSO4��Һ�����ʵ���Ũ��Ϊ0.2mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NAΪ�����ӵ�������ֵ������˵����ȷ����
A. 18gD2O��18gH2O�к��е���������Ϊ10NA
B. 2L0.5mol/L��������Һ�к��е�H+��Ϊ2NA
C. 42g��ϩ�ͱ�ϩ�Ļ��������ȼ�����������ķ�����Ϊ4.5 NA
D. �ܱ�������2molNO��1molO2��ַ�Ӧ������ķ�����Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V L Fe2(SO4)3��Һ�к���ag SO42-��ȡ����Һ0.5V L����ˮϡ����2V L����ϡ�ͺ���Һ��Fe3+�����ʵ���Ũ��Ϊ�� ��
A.![]() mol��L��1B.
mol��L��1B.![]() mol��L��1C.
mol��L��1C.![]() mol��L��1D.
mol��L��1D.![]() mol��L��1
mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ����ͺ���Ԫ�صĻ��ϼ����о��������ʵ����������ӽǡ�
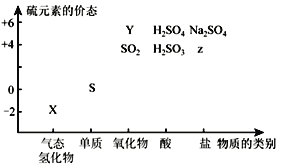

(1)ͼ��Y���ʵĻ�ѧʽΪ______��
(2)������CO��SO2���̵��������Խ����ڴ���������ת��Ϊ����S���������壮�������̵�����Ӧ�Ļ�ѧ����ʽΪ____________________________��
(3)ʵ������X�����ɲ����Ե�������(FeS)�����ϡ�����Ϸ�Ӧ�Ƶã��÷�Ӧ�����ӷ���ʽΪ��_____________________________________________��
(4)Na2S2O3(���������)��һ����;�㷺�����Ρ�
��������������Na2S2O3���Ʊ�����������ԭ��Ӧ�ĽǶȣ��������п��ܵ���___��
a.Na2S+S b.Z+S c.Na2SO3+Y d.NaHS+NaHSO3
��Na2S2O3���н�ǿ��ԭ�ԣ�����Ϊ֯����Ư������ȼ������Ⱥ�S2O32-ת��ΪSO42-�� ���账������״����Cl2 2.24L��֯�����������Ҫ0.00100mol/L Na2S2O3��Һ�����Ϊ_______L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л��ϳ��г��õ��ܼ���ijʵ��С����ʵ���������Ҵ���ˮ�Ʊ����ѣ�װ��ʾ��ͼ���гֺͼ���װ������ȥ�����й����ݺ�ʵ�鲽�����£�
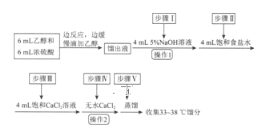

���� | ��Է������� | �ܶȣ���g��mL��1�� | �е㣯�� | ��ˮ�е��ܽ��� |
�Ҵ� | 46 | 0.816 | 78 | ���� |
���� | 74 | 0.713 | 34.6 | ���� |
��֪������ͬ�����£������ڱ���ʳ��ˮ�б���ˮ�и����ܡ�
���Ȼ��ƿ����Ҵ��γ������CaCl2��6C2H5OH��
��ش��������⣺
��1������B������Ϊ________��
��2�����Ҵ��Ʊ����ѵ��ܷ�ӦΪ2C2H5OH![]() CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4
CH3CH2OCH2CH3��H2O���˷�Ӧ���������У���һ����Ӧ�Ļ�ѧ����ʽΪ��CH3CH2OH��H2SO4![]() CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ_____________��
CH3CH2OSO2OH��H2O����ڶ�����Ӧ�Ļ�ѧ����ʽΪ_____________��
��3������D��ʢ�б�ˮ����������Ϊ____________��
��4������1������Ϊ_______________��
��5����ʡ�Բ����ᵼ�µĺ����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��±�����ڼ��Դ���Һ���ܷ�����ȥ��Ӧ�����漸���л��������ת����ϵ��
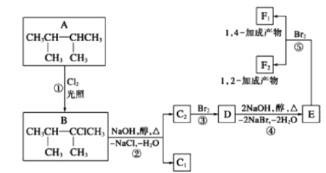
��1������ϵͳ��������������A��������_________
��2��д������D�����������ŵ�����_____________
��3��������E����Ҫ�Ĺ�ҵԭ�ϣ�д����D����E�Ļ�ѧ����ʽ___________
��4��C2�Ľṹ��ʽ��____________��F1�Ľṹ��ʽ��___________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ����Ҫ�Ļ���ԭ�ϡ������йر���ϩ��˵���������( )
A. ��Һ���Ϻ�������ۿɷ���ȡ����Ӧ
B. ��ʹ���Ը��������Һ��ɫ
C. �����Ȼ��ⷢ��ȡ����Ӧ�����ȴ�����ϩ
D. �ڴ��������¿����Ƶþ۱���ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ǿ������ʴ��,����Ǧ����Ϊ���Դ,��Al��������Pb������,���ϡ����,ʹ�����������Ĥ����Ӧԭ������:
���:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l)
����:2Al+3H2O![]() Al2O3+3H2��
Al2O3+3H2��
��������,�����ж���ȷ����( )
��� | ���� | |
A | H+����Pb�缫 | H+����Pb�缫 |
B | ÿ����3molPb | ����2molAl2O3 |
C | ����:PbO2+4H++2e-=Pb2++2H2O | ����:2Al+3H2O-6e-=Al2O3+6H+ |
D |
|
|
A. AB. BC. CD. D
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com