
【题目】卤代烃在碱性醇溶液中能发生消去反应。下面几种有机化合物的转化关系:
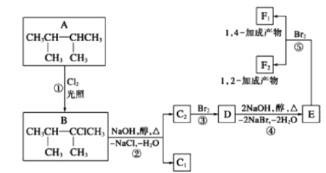
(1)根据系统命名法,化合物A的名称是_________
(2)写出物质D中所含官能团的名称_____________
(3)化合物E是重要的工业原料,写出由D生成E的化学方程式___________
(4)C2的结构简式是____________,F1的结构简式是___________
【答案】2,3-甲基丁烷 溴原子 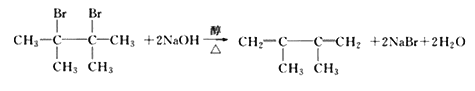 (CH3)2C=C(CH3)2 BrCH2C(CH3)=C(CH3)CH2Br
(CH3)2C=C(CH3)2 BrCH2C(CH3)=C(CH3)CH2Br
【解析】
A在光照条件下与氯气发生取代反应生成B,B在氢氧化钠醇溶液、加热条件下发生消去反应生成C1、C2,C2与溴发生加成反应生成D,D在氢氧化钠醇溶液、加热条件下发生消去反应生成E,E与溴可以发生1,2-加成反应生成F2,发生1,4-加成反应生成F1,则E为CH2=C(CH3)C(CH3)=CH2、F2为CH2=C(CH3)CBr(CH3)CH2Br,F1为BrCH2C(CH3)=C(CH3)CH2Br.逆推可得D为CH3CBr(CH3)CBr(CH3)2,C2为(CH3)2C=C(CH3)2,C1为(CH3)2CHC(CH3)=CH2。
根据上述分析可知,
(1)由化合物A的结构简式,则名称是:2,3-二甲基丁烷,
故答案为:2,3-二甲基丁烷;
(2)D为CH3CBr(CH3)CBr(CH3)2,其所含官能团名称为故答案为:溴原子,
故答案为:溴原子;
(3)根据以上分析,D生成E的化学方程式: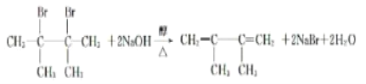 ,
,
故答案为: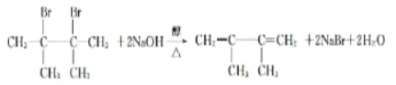 ;
;
(4)根据以上分析,C2的结构简式是:(CH3)2C=C(CH3)2,F1的结构简式是:BrCH2C(CH3)=C(CH3)CH2Br,
故答案为:(CH3)2C=C(CH3)2;BrCH2C(CH3)=C(CH3)CH2Br。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小组利用下列装置检验草酸亚铁晶体受热分解的部分产物。
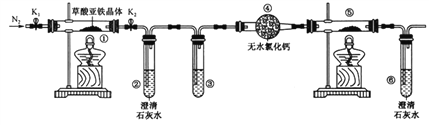
下列说法正确的是
A. 若③和⑤中分别盛放足量NaOH溶液和CuO,可检验生成的CO
B. 实验时只需要在装置①中反应结束后再通入N2
C. 若将④中的无水CaCl2换成无水硫酸铜可检验分解生成的水蒸气
D. 实验结束后,①中淡黄色粉末完全变成黑色,则产物一定为铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Bodensteins研究反应H2(g)+I2(g)![]() 2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
2HI(g) △H<0 ,温度为T时,在两个体积均为1L的密闭容器中进行实验,测得气体混合物中碘化氢的物质的量分数w(HI)与反应时间t的关系如下表:
容器编号 | 起始物质 | t/min | 0 | 20 | 40 | 60 | 80 | 100 |
Ⅰ | 0.5molI2、0.5molH2 | w(HI)/% | 0 | 50 | 68 | 76 | 80 | 80 |
Ⅱ | xmolHI | w(HI)/% | 100 | 91 | 84 | 81 | 80 | 80 |
研究发现上述反应中:v正=kaw(H2)w(I2),v逆=kbw2(HI),其中ka、kb为常数。下列说法不正确的是( )
A. 温度为T时,该反应![]() =64
=64
B. 容器I中在前20min的平均速率v(HI)=0.025molL-1min-1
C. 若起始时,向容器I中加入物质的量均为0.1mol的H2、I2、HI,反应逆向进行
D. 无论x为何值,两容器中达平衡时w(HI)%均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水中氨态氮以NH3·H2O、NH3和NH4+的形式存在,废水脱氮已成为主要污染物减排和水体富营养化防治的研究热点。
Ⅰ.沉淀法
向废水中投入MgCl2和Na2HPO4,生成MgNH4PO4·6H2O沉淀,可将氨态氮含量降至10mg·L1以下。
(1)NH3的电子式:______。
(2)废水中的NH3·H2O转化为MgNH4PO4·6H2O的离子方程式是______。

(3)16℃时,向废水中加入MgCl2和Na2HPO4,使镁、氮、磷物质的量之比为1︰1︰1,沉淀过程中的pH对剩余氨态氮浓度的影响如图。欲使剩余氨态氮浓度低于10mg·L1,pH的适宜范围是______,pH偏大或者偏小均不利于MgNH4PO4·6H2O的生成。
Ⅱ.微波氧化法
(4)微波协同CuO和H2O2除去氨态氮
①其他条件相同,取相同体积的同一废水样品,微波10 min,剩余氨态氮浓度与一定浓度H2O2溶液添加量的关系如下图。据图推测CuO在氨态氮脱除中可能起催化作用,理由_____________

②微波协同CuO有利于H2O2除去氨态氮。该条件下,H2O2将NH3氧化为N2的化学方程式是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列装置完成相关实验,合理的是( )
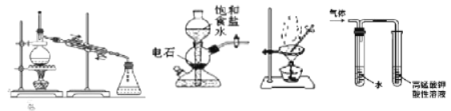
A. 提纯工业乙醇(含甲醇、水等杂质)的装置①
B. 实验室中若需制备较多量的乙炔可用装置②
C. 提纯含苯甲酸钠杂质的粗苯甲酸选择装置③
D. 检验溴乙烷与NaOH乙醇溶液加热制得的气体选择装置④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是
A. 氢氧化钠与盐酸;氢氧化钠与醋酸
B. Na2CO3溶液与盐酸;CaCO3与盐酸
C. BaCl2溶液与Na2SO4溶液;BaCl2溶液与NaHSO4溶液
D. Fe(OH)3胶体的制备;Fe(OH)3沉淀的制备
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语的表达正确的是( )
A. 原子核内有10个中子的氧原子:![]() O
O
B. 氯原子的结构示意图:![]()
C. Fe3+的最外层电子排布式:3s23p63d5
D. 基态铜原子的外围电子轨道表示式:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将Na、Mg、Al各0.4mol分别放入100mL、2mol/L的盐酸中,同温同压下产生的气体的体积比是:
A.1:1:1 B.2:1:1 C.3:1:1 D.1:2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在湿法炼锌的电解循环溶液中,较高浓度的![]() 会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去
会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去![]() 。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是
。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是

A. ![]() 的数量级为
的数量级为![]()
B. 除![]() 反应为Cu+Cu2++2
反应为Cu+Cu2++2![]() =2CuCl
=2CuCl
C. 加入Cu越多,Cu+浓度越高,除![]() 效果越好
效果越好
D. 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com