
【题目】铜片和锌片用导线连接后插入稀硫酸中,锌片是 ( )
A. 正极 B. 负极 C. 阳极 D. 阴极
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)![]() K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol1
已知:碳的燃烧热ΔH1=a kJ·mol1
S(s)+2K(s)![]() K2S(s) ΔH2=b kJ·mol1
K2S(s) ΔH2=b kJ·mol1
2K(s)+N2(g)+3O2(g)![]() 2KNO3(s) ΔH3=c kJ·mol1
2KNO3(s) ΔH3=c kJ·mol1
则x为
A.3a+bc B.c3ab C.a+bc D.cab
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2Fe2O3(s) +3C(s)=3CO2(g) +4Fe(s) △H=+468.2 kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5 kJ/mol
根据以上热化学方程式判断,下列说法正确的是 ( )
A. C(s)的燃烧热为393.5kJ
B. 右图可表示由C生成CO2的反应过程和能量关系
C. O2(g)与Fe(s)反应放出824.35kJ热量时,转移电子数为4NA
D. Fe2O3(s)+ ![]() C(g)=
C(g)= ![]() CO2(g)+2Fe(s) △H <234.1 kJ/mol
CO2(g)+2Fe(s) △H <234.1 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向0.1mol/I.的NH4HCO3溶液中逐渐加入0.1mol/LNaOH溶液时,含氮、含碳粒子的分布情况如图所示(纵坐标是各粒子的分布系数,即物质的量分数)。根据图象,下列说法不正确的是( )
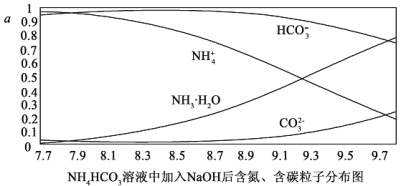
A.开始阶段,HCO3-反而略有增加,可能是因为NH4HCO3溶液中存在H2CO3发生的主要反应是H2CO3+OH-═HCO3-+H2O
B.当pH大于8.7以后,碳酸氢根离子和铵根离子同时与氢氧根离子反应
C.pH=9.5时,溶液中c(HCO3-)>c(HN3H2O)>c(NH4+)>c(CO32-)
D.滴加氢氧化钠溶液时,首先发生的反应为2NH4HCO3+2NaOH═(NH4)2CO3+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是 ( )
A. 1L 0.1 moI·L-1氨水中含有OH -数日为0.1NA
B. KIO3与HI溶液反应时.生成0.1molI2转移的电子数为0.2NA
C. l0g D2O和l0g H218O中含有的中子数均为5NA
D. 0.1 mol N2与0.3mol H2通过高温高压催化剂,生成的气体分子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应既是氧化还原反应,又是吸热反应的是
A. 铝片与稀H2SO4反应 B. Ba(OH)2·8H2O与NH4Cl反应
C. 灼热的炭与CO2反应 D. 甲烷在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是
A.苯的硝化反应属于取代反应
B.苯和乙烯均能使酸性KMnO4溶液褪色
C.苯环是单、双键交替组成的平面环状结构
D.苯跟溴水在催化剂作用下发生取代反应生成溴苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某硫酸钠溶液50mL中含有1.15gNa+,取出10mL稀释至20mL后所得溶液中SO42-的物质的量浓度是______。
(2)12.4 g Na2X中含有0.4 mol Na+,则该物质的化学式为_______________。
(3)标准状况下四种气体:①6.72 L CH4②3.01×1023个HCl分子③13.6 g H2S④0.2 mol NH3,氢原子个数从大到小的排序是__________________________(写序号)。
(4)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,分别向A、B两室充入H2、O2的混合气体和1 mol空气,此时活塞的位置如图所示。

①A室混合气体所含分子总数约为___________________________。
②实验测得A室混合气体的质量为34 g,则该混合气体的密度是同温同压下氦气密度的___倍。
③若将A室H2、O2的混合气体点燃引爆,恢复原温度后,最终活塞停留的位置在____刻度,容器内气体压强与反应前气体压强之比为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以熔融Na2CO3为电解质,H2和CO混合气为燃料的电池原理如下图所示。

下列说法正确的是( )
A. b是电池的负极
B. a电极的反应为:CO+CO32ˉ-2eˉ= 2CO2;H2+CO32ˉ-2eˉ= H2O+CO2
C. a电极上每消耗22.4L原料气,电池中转移电子数约为2╳6.02╳1023
D. a、b两极消耗的气体的物质的量之比是1︰1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com