
【题目】在中和滴定实验用到的仪器中,只需用蒸馏水洗净不能用待盛放液体润洗的是( )
A. 酸式滴定管 B. 碱式滴定管 C. 烧杯 D. 锥形瓶
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
【题目】元素 Y 的原子获得 3 个电子或元素 X 的原子失去 2 个电子后,它们的电子层结构都与氖原子的电子层结构相同。X、Y 两种元素的单质在高温下反应得到的化合物的化学式是
A.Y3X2B.X2Y3C.X3Y2D.Y2X3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2009年,美国麻省理工学院的唐纳德·撒多维教授领导的小组研制出一种镁一锑液态金属储能电池。该电池工作温度为700摄氏度,其工作原理如图所示:

该电池所用液体密度不同,在重力作用下分为三层,充放电时中间层熔融盐的组成及浓度不变。下列说法正确的是
A. 该电池放电时,正极反应式为Mg2+-2e-=Mg
B. 该电池放电时,Mg(液)层生成MgCl2,质量变大
C. 该电池充电时,Mg-Sb(液)层中Mg发生氧化反应
D. 该电池充电时,熔融盐中的Cl-进入Mg-Sb(液)层
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内作为主要能源物质、生物体内的储能物质、结构物质、遗传物质的分别是:
A. 核酸、脂肪、蛋白质、糖类 B. 糖类、核酸、脂肪、蛋白质
C. 糖类、脂肪、蛋白质、核酸 D. 糖类、脂肪、核酸、蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
A. C14H10O5 B. C14H16O4 C. C14H18O5 D. C14H22O5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定浓度的盐酸和醋酸加水稀释,溶液的导电能力随溶液体积变化的曲线如图所示.判断下列说法中,正确的是( ) 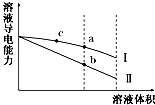
A.两溶液稀释前的浓度相同
B.a、b、c三点溶液的pH由大到小顺序为a>b>c
C.a点的KW值比b点的KW值大
D.a点水电离的c(H+)大于c点水电离的c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产生活中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
2C(s)+O2(g)=2CO(g) △H=-221kJ/mol
若某反应的平衡常数表达式为:k=[c(N2)·c2(CO2)]/[c2(NO)·c(CO)2],请写出此反应的热化学方程式:___________。
(2)N2O5 在一定条件下可发生分解:2N2O5(g)=4NO2(g)+O2(g),某温度下恒容密闭容器中加入一定量 N2O5,测得 N2O5 浓度随时间的变化如下表:
t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
c(N2O5)/(mol/L) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
①反应开始时体系压强为 P0,第 2.00min 时体系压强为 P1,则 P1:P0=_________。2.00~5.00min 内用 NO2 表示的该反应的平均反应速率为_________。
②一定温度下,在恒容密闭容器中充入一定量 N2O5 进行该反应,能判断反应已达到化学平衡状态的是________(填字母序号)。
a.NO2 和 O2 的浓度比保持不变 b.容器中压强不再变化
c.2v 正(NO2)=v 逆(N2O5) d.气体的平均相对分子质量为 43.2,且保持不变
(3)平衡常数 Kp 是用反应体系中气体物质的分压来表示的,即将K表达式中平衡浓度用平衡分压代替,分压=总压 × 物质的量分数,例如:p(NO2)=p总·x(NO2)(x表示气体的物质的量分数)。
N2O4 与 NO2 转换的热化学方程式为N2O4(g)![]() 2NO2(g) △H=+24.4kJ/mol
2NO2(g) △H=+24.4kJ/mol
上述反应中,正反应速率 v正=k正·p(N2O4),逆反应速率v逆=k逆·p2(NO2),其中k正、k逆为速率常数,则 Kp 为_________(以 k 正、k 逆表示)。
(4)下图是密闭反应器中按 n(N2):n(H2)=1:3 投料后,在 200℃、400℃、600℃下,合成 NH3 反应达到平衡时,混合物中 NH3 的物质的量分数随压强的变化曲线,已知该反应为放热反应。

①曲线 a 对应的温度是________。
②M 点对应的 H2 的转化率是___________。
(5)工业上常用氨水吸收二氧化硫,可生成(NH4)2SO3。通过计算判定(NH4)2SO2 溶液的酸碱性________。(写出计算过程,并用简要的文字加以说明)(已知:氨水Kb=1.8×10-5;H2SO3:Ka1=1.3×10-2 Ka2=6.3×10-8)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com