
����Ŀ��ij����С����Ƴ����ù�ҵ����(ϡ����)����ȡij����������ͭп��ķ�����ʵ�ַ����ۺ����ã�������ͼ��ʾ��
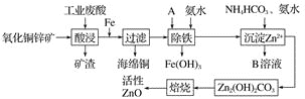
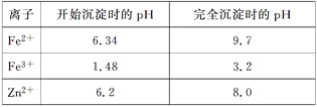
��֪�������ӿ�ʼ��������ȫ����ʱ��pH�����ʾ��
��ش��������⣺
(1)�ڡ�����������У�Ϊ��߽������ʣ���ͨ����������衱�⣬���ɲ�ȡ�Ĵ�ʩ��(��дһ�㼴��)__________________________________________________________��
(2)����A���ʹ�����������е�____________����ѡ����ţ���
A��KMnO4����B��H2O2����C��HNO3
(3)���������м��백ˮ��Ŀ���ǵ�����Һ��pH��pHӦ������__________��Χ֮�䡣
(4)����B��ֱ���������ʣ���B�Ļ�ѧʽ��________��
(5)������õ��������������ô��������Һ�ڼ��Ի������������õ�һ�ָ�Ч�Ķ�ܴ�����(K2FeO4)��д���÷�Ӧ�����ӷ���ʽ��__________________________��
���𰸡����������¶ȣ����������Ũ�ȡ�������ͭп������B3.2��6.2(NH4)2SO42Fe(OH)3��3ClO����4OH��=2FeO42����3Cl����5H2O
��������
(1)����ǽ�����ͭп�������ܽ⣬�ٽ��ܽ�Ĵ�ʩ�н��衢���������¶ȡ��������Ũ�ȡ�������ͭп�����ȡ�(2)���������м���A�Ͱ�ˮ��ʹ�������ӱ���������������� AӦΪ�����������Ǽ���A�������µ����ʣ�H2O2�⣬�����Լ����������µ����ʡ�(3)��ͼ�����ݿ�֪�������ӳ�����ȫ��pHΪ3.2��п���ӿ�ʼ������pHΪ6.2���ʳ���pH��ΧΪ3.2��6.2��(4)�����÷���Ϊ���ᣬB�ֿ������ʣ�����BΪ����李�(5)�������Ϣ��֪����Ӧ��Ϊ��������������������ӡ����������ӣ�������֮һΪ![]() �������ڷ�Ӧ�л��ϼ����ߣ���Ԫ�صĻ��ϼ۽��ͣ���һ����Ϊ�����ӣ�����Ԫ�ء����ӡ�����غ���ƽ(��֪���ﻹ��ˮ)�����ӷ���ʽΪ2Fe(OH)3��3ClO����4OH��===2
�������ڷ�Ӧ�л��ϼ����ߣ���Ԫ�صĻ��ϼ۽��ͣ���һ����Ϊ�����ӣ�����Ԫ�ء����ӡ�����غ���ƽ(��֪���ﻹ��ˮ)�����ӷ���ʽΪ2Fe(OH)3��3ClO����4OH��===2![]() ��3Cl����5H2O��
��3Cl����5H2O��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ȼ����������H2S�����忪��Ӧ�����ޡ�T��F����������Һ�п�ʵ����Ȼ���Ĵ�������ԭ����ͼ��ʾ������˵������ȷ����
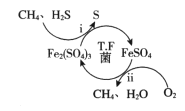
A. �����������Ҫ��������Fe2(SO4)3��Һ
B. �������O2�������H2S
C. ������Ѫ�쵰����Ҫ��ɳɷ֣�FeSO4����������ȱ����ƶѪ
D. ��������־��������ȡ������֮��һ��ˮ���嶷�������ҹ��Ŵ���������Ȼ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾװ����,�ס��ҡ��������ձ����ηֱ�ʢ��������NaCl��Һ��AgNO3��Һ��x��Һ,a��b��c��d�缫��Ϊʯī�缫![]() ��ͨ��Դ,����һ��ʱ���,����c�缫��������
��ͨ��Դ,����һ��ʱ���,����c�缫��������![]() �ݴ˻ش����⣺
�ݴ˻ش����⣺
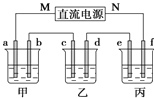
(1)��Դ��M��Ϊ_____________����
(2)�缫d�Ϸ����ĵ缫��ӦʽΪ__________�� �ҳ���ҺPH__________���������������С��������������
(3)�׳��е��ܷ�ӦʽΪ___________________________________��
(4)����·����0.04mol����ͨ��ʱ,a��b��c��d�缫�ϲ�����������������ʵ���֮����____________��
(5)�����ñ���ʵ�����϶�ͭ,����e-f-x��![]() ��Һ��__________________________��(Ҫ��e��f��x�þ������ʻش�,��ͬ),�����ñ���ʵ�ֵ�⾫��ͭ,��f�缫������_______________________
��Һ��__________________________��(Ҫ��e��f��x�þ������ʻش�,��ͬ),�����ñ���ʵ�ֵ�⾫��ͭ,��f�缫������_______________________
(6) ʵ����, 1g�״���CH3OH��Һ���������г��ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷų�22.68kJ������,���ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ��_____________________________________________________
(7)��������![]() �ṹʽΪ
�ṹʽΪ![]() ���л��ϳ��е���Ҫ�Լ�,����
���л��ϳ��е���Ҫ�Լ�,����![]() ��
��![]() ��ͨ����Ӧ�������Ƶ�,��Ӧ����ʽΪ
��ͨ����Ӧ�������Ƶ�,��Ӧ����ʽΪ![]() ����֪���ֻ�ѧ���ļ����������±���ʾ��
����֪���ֻ�ѧ���ļ����������±���ʾ��
��ѧ�� |
|
|
|
|
���� | 243 | a | 607 | 630 |
��![]() ��NO��Ӧ����ClNO�Ĺ�����ת����4mol����,�����Ϸų�������Ϊ______kJ��(�����ֺ���ĸ��ʾ)
��NO��Ӧ����ClNO�Ĺ�����ת����4mol����,�����Ϸų�������Ϊ______kJ��(�����ֺ���ĸ��ʾ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ�����ڼӳɷ�Ӧ����(����)
A. CH4��Cl2![]() CH3Cl��HCl
CH3Cl��HCl
B. CH2===CH2��HCl�D��CH3CH2Cl
C. CH3CH2OH��HBr![]() CH3CH2Br��H2O
CH3CH2Br��H2O
D. 2CH3CH3��7O2![]() 4CO2��6H2O
4CO2��6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�����������˵����ȷ����( )
A.����Ϊ16g��O2��O3�Ļ����������������ԭ�ӵĸ���ΪNA
B.18 g NH4+����������Ϊ10NA
C.1 mol��������������ˮ��Ӧʱ��ת�Ƶ��ӵ���ĿΪ2NA
D.0.1 molL��1��NaCl��Һ�У�Na+��Cl������������Ϊ0.2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ʵ�����ý���ͭ��ϡ������ȡNO�����ӷ���ʽΪ______________________��
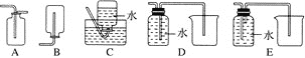
(2)NO���ж����壬ijѧ��Ϊ��ֹ��Ⱦ���÷�Һ©�����ձ�װ����һ���ġ����濪���á������ͣ��NO���巢��װ�ã���ͼ����ʾ��

��ʵ������û��ͭ˿����ֻ��Сͭ������ʹ������װ�ý���ʵ��ʱ������˿״���ϰ���ͭ���Դ���ͭ˿����ʵ�飬����˿״���ϵijɷֿ�����________(�����)��
A���� B���� C���� D������
�ڴ�Һ©���Ļ���ʹ��Ӧ���У��ڷ�Һ©����ʵ�ʿ����������Ǻ���ɫ�ģ�ԭ����__________(�ѧ����ʽ)��
(3)Ϊ֤��ͭ˿��ϡ���ᷴӦ���ɵ�ȷʵ��NO��ijѧ���������һ����ͼ����ʾ��װ����ȡNO����Ӧ��ʼ������U�ι��Ҷ˹۲쵽��ɫ��NO���塣
�ٳ������ܵ�������______________________________________________________��
���÷�Ӧֹͣ�IJ���������ԭ����__________________________________________��
(4)�����ռ�NO�����װ�ã���������________(�����)��
(5)��32.64 gͭ��140 mLһ��Ũ�ȵ����ᷴӦ��ͭ��ȫ�ܽ������NO��NO2��������ڱ�״���µ����Ϊ11.2 L����ش�
��NO�����Ϊ________ L��NO2�����Ϊ________ L��
�ڴ�����������ȫ���ͷź�����Һ�м���VmLamol��L��1��NaOH��Һ��ǡ��ʹ��Һ�е�Cu2��ȫ��ת���ɳ�������ԭ������Һ��Ũ��Ϊ________ mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ij100 mL�Ļ��Һ�У��������������ʵ���Ũ�ȷֱ���0.4 mol��L-1��0.1 mol��L-1,��û��Һ�м���1.92 gͭ��,����,����ַ�Ӧ��,������Һ��ͭ�������ʵ���Ũ��( mol��L-1)�ǣ� ��
A. 0.15 B. 0.225 C. 0.35 D. 0.45
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��F�Ǽ�ͥ�г������л��E��ʯ�ͻ�����չˮƽ�ı�־��F��һ�ֳ����ĸ߷��Ӳ��ϡ���������ת����ϵ�ش��������⣺

(1)�����ޡ������ߵ����Ʒֱ�Ϊ________��________��
(2)���������зе���ߵ���________��
A ���� B ú��
C ���� D ����
(3)�ڢ١���������ȡ����Ӧ����________��ԭ��������Ϊ100%�ķ�Ӧ��________��(�����)
(4)д���ṹ��ʽ��A________��F________��
(5)д����Ӧ�۵����ӷ���ʽ��___________��
(6)��Ϊ��ͥ�г���������F���������Ǵ����˼���ķ��㣬ͬʱҲ����˻�����Ⱦ��������Ⱦ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס��ҡ����������������У��ס��ҡ�����������ͬ��ij��Ԫ�أ�����֮���������ת����ϵ��

�����й����ʵ��ƶϲ���ȷ����(����)
A. ����Ϊ��̿��������O2B. ����ΪSO2�������ǰ�ˮ
C. ����ΪFe������������D. ����ΪNaOH��Һ��������CO2
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com