
【题目】下表是一些键能数据![]() :
:

回答下列问题。
(1)由表中数据能否得出下列结论:
①半径越小的原子形成的共价键越牢固(即键能越大),__________(填“能”或“不能”);
②非金属性越强的原子形成的共价键越牢固,__________(填“能”或“不能”)。能否从数据中找出一些规律,请写出一条:______________________________。试预测C-Br键的键能范围:__________<C-Br键能<__________。
(2)由热化学方程式![]()
![]() 并结合上表数据可推知一个化学反应的反应热(设反应物和生成物均为气态)与反应物和生成物的键能之间的关系是_____________;
并结合上表数据可推知一个化学反应的反应热(设反应物和生成物均为气态)与反应物和生成物的键能之间的关系是_____________;
(3)由热化学方程式![]()
![]() 和表中数值可计算出
和表中数值可计算出![]() 变为
变为![]() 时将__________(填“吸收”或“放出”)__________kJ的热量。
时将__________(填“吸收”或“放出”)__________kJ的热量。
【答案】不能 不能 与相同原子结合时同主族元素原子形成的共价键,原子半径越小,共价键越牢固 ![]()
![]() 化学反应的反应热等于反应物的键能之和与生成物的键能之和的差 吸收 36.5
化学反应的反应热等于反应物的键能之和与生成物的键能之和的差 吸收 36.5
【解析】
(1)比较半径与键能大小要在同一标准下进行,否则没有可比性,同主族元素的半径越大,键能越小;
(2)化学反应的反应热等于反应物的键能之和与生成物的键能之和的差计算解答(2)和(3)。
(1)①由表中数据可知,原子半径F>H,但键能:H-F>H-H,则不能得出半径越小的原子形成的共价键越牢固的结论;②Cl的非金属性大于H,但键能H-H>Cl-Cl,也不能说明非金属性越强的原子形成的共价键越牢固;由H-F、H-Cl、H-Br、H-I的键能可以看出,与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越牢固;Br的原子半径介于Cl与I之间,C-Br的键能介于C-Cl与C-I之间,即216kJmol-1~339 kJmol-1之间,故答案为:不能;不能;与相同原子结合时同主族元素形成的共价键,原子半径越小,共价键越牢固;216kJmol-1;339 kJmol-1;
(2)已知:热化学方程式H2(g)+Cl2(g)→2HCl(g) △H=-183kJmol-1,
可得出△H=436kJ/mol+243kJ/mol-2×431kJ/mol=-183kJ/mol,则有化学反应的反应热等于反应物的键能之和与生成物的键能之和的差,故答案为:化学反应的反应热等于反应物的键能之和与生成物的键能之和的差;
(3)由表中数据可得:①2H2(g)+S2(g)→2H2S(g)![]() ,又知②2H2(g)+S2(s)→2H2S(g) △H=-224.5kJmol-1,则②-①得:S2(s)→S2(g) △H=-224.5kJmol-1—(-261kJmol-1)=+36.5kJ/mol,则1mol S2(s)气化时将吸收36.5kJ的能量,故答案为:吸收;36.5。
,又知②2H2(g)+S2(s)→2H2S(g) △H=-224.5kJmol-1,则②-①得:S2(s)→S2(g) △H=-224.5kJmol-1—(-261kJmol-1)=+36.5kJ/mol,则1mol S2(s)气化时将吸收36.5kJ的能量,故答案为:吸收;36.5。


科目:高中化学 来源: 题型:
【题目】硫酸锰在锰系产品中具有重要地位,由软锰矿(MnO2) 和硫铁矿(FeS2)制备流程如下:

(1)从“除质2”后的溶液中得到MnSO4的操作为______、降温结晶、过滤和干燥。
(2)下图是在一定条件下,不同浓度的硫酸对各元素浸出率的影响,由此得出的相关结论是:

①__________;②__________。提高软锰矿浸出率的措施还有______和_______。
(3)除铁剂为H2SO5和氨水。
①H2SO5 中S的化合价为+6,其中过氧键的数目为______,加入其目的是_________。
②写出Fe3+生成沉淀黄铵铁矾NH4Fe3(SO4)2(OH)6的离子方程式____________。
(4)工业除质剂为MnF2,发生反应为(已知,该温度下MnF2、CaF2 和MgF2 的Ksp分别为5.0×10-3、2.0×10-10、8.0×10-11)
反应I:MnF2(s) +Ca2+=CaF2(s) +Mn2+
反应II:MnF2(s) +Mg2+=MgF2(s) + Mn2+
若滤液中c(Mg2+) =0.02 mol/L,加入MnF2(s),使Ca2+恰好沉淀完全即溶液中c(Ca2+) =1.0×10-5mol/L,此时是否有MgF2 沉淀生成?_________(列式计算)。
查看答案和解析>>
科目:高中化学 来源: 题型:
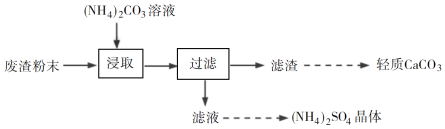
【题目】实验室以工业废渣(主要含CaSO4·2H2O,还含少量SiO2、Al2O3、Fe2O3)为原料制取轻质CaCO3和(NH4)2SO4晶体,其实验流程如下:
(1)室温下,反应CaSO4(s)+![]() (aq)
(aq)![]() CaCO3(s)+
CaCO3(s)+![]() (aq)达到平衡,则溶液中
(aq)达到平衡,则溶液中 =________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
=________[Ksp(CaSO4)=4.8×105,Ksp(CaCO3)=3×109]。
(2)将氨水和NH4HCO3溶液混合,可制得(NH4)2CO3溶液,其离子方程式为________;浸取废渣时,向(NH4)2CO3溶液中加入适量浓氨水的目的是________。
(3)废渣浸取在如图所示的装置中进行。控制反应温度在60~70 ℃,搅拌,反应3小时。温度过高将会导致CaSO4的转化率下降,其原因是________;保持温度、反应时间、反应物和溶剂的量不变,实验中提高CaSO4转化率的操作有________。

(4)滤渣水洗后,经多步处理得到制备轻质CaCO3所需的CaCl2溶液。设计以水洗后的滤渣为原料,制取CaCl2溶液的实验方案:______[已知pH=5时Fe(OH)3和Al(OH)3沉淀完全;pH=8.5时Al(OH)3开始溶解。实验中必须使用的试剂:盐酸和Ca(OH)2]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨分子中的一个氢原子被甲基取代后,所得甲胺(CH3NH2)的性质与氨相似,CH3NH2·H2O也是一元弱碱,25℃时电离常Kb=4.0×10-5。现用0.0500mol/L的稀硫酸滴定10mL 0.1000mol/L的甲胺溶液,溶液中c(OH-)的负对数(pOH)与所加稀硫酸的体积(V)的关系如图所示。下列说法正确的是
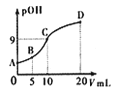
A. 甲胺在水中的电离方程式为:CH3NH2·H2O=CH3NH3++OH-
B. A、B、C三点溶液中,水电离出来的c(H+):B>C>A
C. C点所在溶液中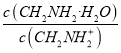 =2.5×10-5
=2.5×10-5
D. B点溶液中存在c(CH3NH2·H2O)>c(CH3NH3+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(![]() CH=CH-CHO),杏仁含苯甲醛(
CH=CH-CHO),杏仁含苯甲醛(![]() CHO)。下列说法错误的是
CHO)。下列说法错误的是
A. 肉桂醛,苯甲醛都能发生加成反应、取代反应和聚合反应
B. 可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团
C. 肉桂醛和苯甲醛互为同系物
D. 苯甲醛分子中所有原子可能位于同一平面内
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种短周期元素的原子序数依次增大,A 的一种核素在考古时常用来鉴定一些文物的年代,B的气态氢化物的水溶液呈碱性;C为金属元素且有两种常见含氧化合物(都含两种元素);若往D单质的水溶液中滴加少量紫色石蕊溶液,可观察到先变红后褪色。下列说法中正确的是( )
A.C的两种含氧化合物中阴、阳离子个数比都为1∶2
B.最高价氧化物对应的水化物的酸性:B>D
C.B的氢化物的沸点一定高于A的氢化物
D.电负性:D>B>A>C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然气因含有少量 H2S 等气体开采应用受限。T.F 菌在酸性溶液中可实现天然气的催化脱硫,其原理如下图所示。下列说法不正确的是( )

A.脱硫过程 O2 间接氧化 H2S
B.该脱硫过程需要不断添加 Fe2(SO4)3 溶液
C.亚铁是血红蛋白重要组成成分,FeSO4 可用于治疗缺铁性贫血
D.《华阳国志》记载“取井火煮之,一斛水得五斗盐”,我国古代已利用天然气煮盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】因新型冠状病毒肺炎疫情防控需求,口罩已经成为了2020每个人必备之品。熔喷布,俗称口罩的“心脏”,是口罩中间的过滤层,能过滤细菌,阻止病菌传播。熔喷布是一种以高熔融指数的聚丙烯(PP)为材料,由许多纵横交错的纤维以随机方向层叠而成的膜。其中有关聚丙烯的认识正确的是
A.由丙烯通过加聚反应合成聚丙烯
B.聚丙烯的链节:—CH2—CH2—CH2—
C.合成聚丙烯单体丙烯的结构简式:CH2CHCH3
D.聚丙烯能使溴水发生加成反应而褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com