
ΓΨΧβΡΩΓΩ”–50mLNaOH»ή“ΚΘ§œρΤδ÷–÷πΫΞΆ®»κ“ΜΕ®ΝΩΒΡCO2Θ§ΥφΚσ»Γ¥Υ»ή“Κ10mLΫΪΤδœΓ ΆΒΫ100mLΘ§≤Δœρ¥ΥœΓ ΆΚσΒΡ»ή“Κ÷–÷πΒΈΦ”»κ0.1mol/LΒΡHCl»ή“ΚΘ§≤ζ…ζΒΡCO2ΤχΧεΧεΜΐΘ®±ξΉΦΉ¥Ωωœ¬Θ©”κΥυΦ”»κΒΡHClΒΡΧεΜΐ÷°ΦδΒΡΙΊœΒ»γΆΦΥυ ΨΘΚ ‘Ζ÷ΈωΘΚ
Θ®1Θ©NaOH‘ΎΈϋ ’CO2ΤχΧεΚσΘ§‘ΎΦΉΓΔ““ ΝΫ÷÷«ιΩωœ¬Θ§ΥυΒΟ»ή“Κ÷–¥φ‘ΎΒΡ»ή÷ «

ΦΉΘΚ_____________ΤδΈο÷ ΒΡΝΩ÷°±» «ΘΚ__________
““ΘΚ_____________ΤδΈο÷ ΒΡΝΩ÷°±» «ΘΚ__________
Θ®2Θ©‘ΎΝΫ÷÷«ιΩωœ¬≤ζ…ζΒΡCO2ΤχΧεΘ®±ξΉΦΉ¥ΩωΘ©Ης «ΦΉΘΚ___________ΘΜ““ΘΚ___________ΓΘ
Θ®3Θ©‘≠NaOH»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε» «___________ΘΜ
ΓΨ¥πΑΗΓΩ NaOHΘ§Na2CO3 1:1 NaHCO3ΚΆNa2CO3 1:1 56mL 112mL 0.75mol/L
ΓΨΫβΈωΓΩ ‘ΧβΖ÷ΈωΘΚΧΦΥαΡΤ”κ―ΈΥαΖ¥”Π ±Ζ÷ΝΫ≤ΫΫχ––Θ§Ζ÷±π «CO32-+H+=HCO3-Θ§HCO3-+H+=H2O+CO2ΓϋΘ§Υυ“‘ΝΫ≤ΫœϊΚΡ―ΈΥαΒΡΝΩœύΆ§ΓΘ”…ΦΉΆΦΩ…÷ΣΘ§œΓ ΆΚσΒΡ»ή“Κ÷–÷πΒΈΦ”»κΒΎ“ΜΖί25mL―ΈΥα ±”κ«β―θΜ·ΡΤΖ¥”ΠΘ§ΒΎΕΰΖί25mL―ΈΥα ±ΖΔ…ζCO32-+H+=HCO3-Θ§ΒΎ»ΐΖί25mL―ΈΥα ±ΖΔ…ζHCO3-+H+=H2O+CO2ΓϋΘ§Υυ“‘»ή“Κ÷–ΒΡ»ή÷ ΈΣNaOHΚΆNa2CO3Θ§ΤδΈο÷ ΒΡΝΩ÷°±» «1:1ΓΘ”…ΆΦ““Ω…÷ΣΘ§œΓ ΆΚσΒΡ»ή“Κ÷–÷πΒΈΦ”»κΒΎ“ΜΖί25mL―ΈΥα ±ΖΔ…ζCO32-+H+=HCO3-Θ§Φ”»κΒΎΕΰΖίΚΆΒΎ»ΐΖί25mL―ΈΥα ±ΖΔ…ζHCO3-+H+=H2O+CO2ΓϋΘ§Υυ“‘»ή“Κ÷–ΒΡ»ή÷ «NaHCO3ΚΆNa2CO3Θ§ΤδΈο÷ ΒΡΝΩ÷°±» «1:1ΓΘ
Θ®1Θ©NaOH‘ΎΈϋ ’CO2ΤχΧεΚσΘ§‘ΎΦΉΓΔ““ ΝΫ÷÷«ιΩωœ¬Θ§ΥυΒΟ»ή“Κ÷–¥φ‘ΎΒΡ»ή÷ «
ΦΉΘΚNaOHΘ§Na2CO3Θ§ΤδΈο÷ ΒΡΝΩ÷°±» «ΘΚ1:1ΓΘ
““ΘΚNaHCO3ΚΆNa2CO3ΤδΈο÷ ΒΡΝΩ÷°±» «ΘΚ1:1ΓΘ
Θ®2Θ©‘ΎΝΫ÷÷«ιΩωœ¬≤ζ…ζΒΡCO2ΤχΧεΘ®±ξΉΦΉ¥ΩωΘ©Ης «ΘΚΦΉ÷–”…HCO3-+H+=H2O+CO2ΓϋΒΟn(CO2)=n(HCl)=0.025L![]() 0.1mol/L=0.0025molΘ§ΧεΜΐΈΣ0.0025mol
0.1mol/L=0.0025molΘ§ΧεΜΐΈΣ0.0025mol ![]() 22.4L/mol=0.056L=56mLΘΜ““‘Ύ…ζ≥…ΤχΧεΒΡΙΐ≥Χ÷–Θ®HCO3-+H+=H2O+CO2ΓϋΘ©œϊΚΡ―ΈΥα «ΦΉΒΡ2±ΕΘ§Υυ“‘…ζ≥…CO2ΤχΧε112mLΓΘ
22.4L/mol=0.056L=56mLΘΜ““‘Ύ…ζ≥…ΤχΧεΒΡΙΐ≥Χ÷–Θ®HCO3-+H+=H2O+CO2ΓϋΘ©œϊΚΡ―ΈΥα «ΦΉΒΡ2±ΕΘ§Υυ“‘…ζ≥…CO2ΤχΧε112mLΓΘ
Θ®3Θ©”…ΝΫΆΦœώΩ…÷ΣΘ§50mLNaOH»ή“ΚΉν÷’ΕΦΩ…œϊΚΡ75mL0.1mol/LΒΡ―ΈΥα…ζ≥…¬»Μ·ΡΤ»ή“ΚΘ§‘ΎΖ¥”ΠΙΐ≥Χ÷–ΡΤάκΉ” ΊΚψΓΔ¬»άκΉ” ΊΚψΘ§Υυ“‘‘≠NaOH»ή“ΚΒΡΈο÷ ΒΡΝΩ≈®Ε» «![]() 0.75mol/LΓΘ
0.75mol/LΓΘ


 –¬ΩΈ±ξΩλά÷Χα”≈ νΦΌΉς“Β…¬Ές¬Ο”Έ≥ωΑφ…γœΒΝ–¥πΑΗ
–¬ΩΈ±ξΩλά÷Χα”≈ νΦΌΉς“Β…¬Ές¬Ο”Έ≥ωΑφ…γœΒΝ–¥πΑΗ νΦΌœΈΫ”≈ύ”≈ΫΧ≤Ρ’ψΫ≠ΙΛ…Χ¥σ―ß≥ωΑφ…γœΒΝ–¥πΑΗ
νΦΌœΈΫ”≈ύ”≈ΫΧ≤Ρ’ψΫ≠ΙΛ…Χ¥σ―ß≥ωΑφ…γœΒΝ–¥πΑΗ –ά”οΈΡΜ·Ωλά÷ νΦΌ…ρ―τ≥ωΑφ…γœΒΝ–¥πΑΗ
–ά”οΈΡΜ·Ωλά÷ νΦΌ…ρ―τ≥ωΑφ…γœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΒβΦΑΤδΜ·ΚœΈο‘ΎΚœ≥……±ΨζΦΝΓΔ“©ΈοΒ»ΖΫΟφΨΏ”–ΙψΖΚ”ΟΆΨΓΘΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©¥σΝΩΒΡΒβΗΜΦ·‘ΎΚΘ‘ε÷–Θ§”ΟΥ°Ϋΰ»ΓΚσ≈®ΥθΘ§‘Όœρ≈®Υθ“Κ÷–Φ”MnO2ΚΆH2SO4Θ§Φ¥Ω…ΒΟΒΫI2ΓΘΗΟΖ¥”ΠΒΡΜΙ‘≠≤ζΈοΈΣ______ΓΘ
Θ®2Θ©“―÷ΣΖ¥”Π2HI(g)![]() H2(g)+I2(g)ΒΡΓςH = +11 kJΓΛmolΘ≠1Θ§l molH2(g)ΓΔ1 mol I2(g)Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±Ζ÷±π–η“ΣΈϋ ’436 kJΓΔ151 kJΒΡΡήΝΩΘ§‘ρ1 mol HI(s)Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±–ηΈϋ ’ΒΡΡήΝΩΈΣ______kJΓΘ
H2(g)+I2(g)ΒΡΓςH = +11 kJΓΛmolΘ≠1Θ§l molH2(g)ΓΔ1 mol I2(g)Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±Ζ÷±π–η“ΣΈϋ ’436 kJΓΔ151 kJΒΡΡήΝΩΘ§‘ρ1 mol HI(s)Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±–ηΈϋ ’ΒΡΡήΝΩΈΣ______kJΓΘ
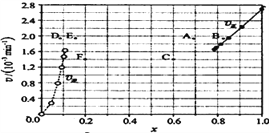
Θ®3Θ©Bodensteins―–ΨΩΝΥœ¬Ν–Ζ¥”ΠΘΚ2HI(g)![]() H2(g)+I2(g)ΓΘ‘Ύ716 K ±Θ§ΤχΧεΜλΚœΈο÷–ΒβΜ·«βΒΡΈο÷ ΒΡΝΩΖ÷ ΐx(HI)”κΖ¥”Π ±ΦδtΒΡΙΊœΒ»γœ¬±μΘΚ
H2(g)+I2(g)ΓΘ‘Ύ716 K ±Θ§ΤχΧεΜλΚœΈο÷–ΒβΜ·«βΒΡΈο÷ ΒΡΝΩΖ÷ ΐx(HI)”κΖ¥”Π ±ΦδtΒΡΙΊœΒ»γœ¬±μΘΚ
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
ΔΌΗυΨί…œ ω Β―ιΫαΙϊΘ§ΗΟΖ¥”ΠΒΡΤΫΚβ≥Θ ΐKΒΡΦΤΥψ ΫΈΣ__________________ΓΘ
ΔΎ…œ ωΖ¥”Π÷–Θ§’ΐΖ¥”ΠΥΌ¬ ΈΣ![]() ’ΐ=k’ΐx2(HI)Θ§ΡφΖ¥”ΠΥΌ¬ ΈΣ
’ΐ=k’ΐx2(HI)Θ§ΡφΖ¥”ΠΥΌ¬ ΈΣ![]() Ρφ=kΡφx(H2)x(I2)Θ§Τδ÷–k’ΐΓΔkΡφΈΣΥΌ¬ ≥Θ ΐΘ§‘ρkΡφΈΣ____________________(“‘KΚΆk’ΐ±μ Ψ)ΓΘ»τk’ΐ=0.0027 minΘ≠1Θ§‘Ύt = 40 min ±Θ§
Ρφ=kΡφx(H2)x(I2)Θ§Τδ÷–k’ΐΓΔkΡφΈΣΥΌ¬ ≥Θ ΐΘ§‘ρkΡφΈΣ____________________(“‘KΚΆk’ΐ±μ Ψ)ΓΘ»τk’ΐ=0.0027 minΘ≠1Θ§‘Ύt = 40 min ±Θ§ ![]() ’ΐ = _______________minΘ≠1ΓΘ
’ΐ = _______________minΘ≠1ΓΘ
Δέ”……œ ω Β―ι ΐΨίΦΤΥψΒΟΒΫ![]() ’ΐΓΪx(HI)ΚΆ
’ΐΓΪx(HI)ΚΆ![]() ΡφΓΪx(H2)ΒΡΙΊœΒΩ…”Οœ¬ΆΦ±μ ΨΓΘΒ±…ΐΗΏΒΫΡ≥“ΜΈ¬Ε» ±Θ§Ζ¥”Π÷Ί–¬¥οΒΫΤΫΚβΘ§œύ”ΠΒΡΒψΖ÷±πΈΣ______________(ΧνΉ÷ΡΗ)ΓΘ
ΡφΓΪx(H2)ΒΡΙΊœΒΩ…”Οœ¬ΆΦ±μ ΨΓΘΒ±…ΐΗΏΒΫΡ≥“ΜΈ¬Ε» ±Θ§Ζ¥”Π÷Ί–¬¥οΒΫΤΫΚβΘ§œύ”ΠΒΡΒψΖ÷±πΈΣ______________(ΧνΉ÷ΡΗ)ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœρœ¬Ν–≈δΚœΈοΒΡΥ°»ή“Κ÷–Φ”»κAgNO3»ή“ΚΘ§≤ΜΡή…ζ≥… AgCl≥ΝΒμΒΡ «Θ® Θ©
A.[Co(NH3) 4Cl2] ClB.[Co(NH3)3Cl3]
C.[Co(NH3)6] Cl3D.[Co(NH3)5Cl] Cl
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΚΘ¥χ÷–Κ§Ββ‘ΣΥΊΓΘ¥”ΚΘ¥χ÷–Χα»ΓΒβ”–»γœ¬≤Ϋ÷ηΘΚΔΌ‘Ύ¬Υ“Κ÷–Ά®»κΉψΝΩCl2ΘΜΔΎΫΪΚΘ¥χ±Κ…’≥…Μ“ΚσΦ”Υ°ΫΝΑηΘΜΔέΦ”CCl4’ώΒ¥ΘΜΔή”ΟΖ÷“Κ¬©ΕΖΖ÷“ΚΘΜΔίΙΐ¬ΥΓΘΚœάμΒΡ≤ΌΉςΥ≥–ρ «( )
A. ΔΌΔΎΔέΔήΔί B. ΔΎΔίΔΌΔέΔή C. ΔΌΔέΔίΔΎΔή D. ΔΎΔΌΔέΔίΔή
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–άκΉ”ΖΫ≥Χ Ϋ ι–¥’ΐ»ΖΒΡ «
A. ”ΟPtΒγΦΪΒγΫβ…ΌΝΩΒΡMgC12»ή“ΚΘΚ2H2OΘΪ2ClΘ≠![]() H2ΓϋΘΪC12ΓϋΘΪ2OHΘ≠
H2ΓϋΘΪC12ΓϋΘΪ2OHΘ≠
B. ΟςΖ·»ή“Κ÷–Φ”»κBa(OH)2»ή“Κ÷Ν…ζ≥…ΒΡ≥ΝΒμΒΡ÷ ΝΩΉνΕύΘΚAl3ΘΪΘΪ2SO42Θ≠ΘΪ2Ba2ΘΪΘΪ4OHΘ≠ΘΫAlO2Θ≠ΘΪ2BaSO4ΓΐΘΪ2H2O
C. œρΚ§”–4 mol FeBr2ΒΡ»ή“Κ÷–Ά®»κ3 mol Cl2≥δΖ÷Ζ¥”ΠΘΚ2Fe2ΘΪΘΪ4BrΘ≠ΘΪ3Cl2ΘΫ4Fe3ΘΪΘΪ6ClΘ≠ΘΪ2Br2
D. ΫΪ1 mol FeΆΕ»κΒΫΚ§3 mol H NO3ΒΡœΓœθΥα»ή“Κ÷–ΘΚ6Fe ΘΪ 5NO3Θ≠ ΘΪ 20HΘΪ ΘΫ3Fe2ΘΪ ΘΪ3Fe3ΘΪ ΘΪ 11NOΓϋ ΘΪ10H2O
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–“«ΤςΘΚΔΌ…’±≠ΓΔΔΎέαέωΓΔΔέΉΕ–ΈΤΩΓΔΔή’τΖΔΟσΓΔΔί ‘ΙήΓΔΔό…’ΤΩΓΔΔΏ±μΟφΟσΘ§”ΟΨΤΨΪΒΤΦ”»» ±Θ§–η“ΣΒφ ·ΟόΆχΒΡ «
A. ΔΎΔήΔί B. ΔΌΔόΔΏ
C. ΔέΔήΔό D. ΔΌΔέΔό
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΖ¥”ΠNH4HS(s) ![]() NH3(g)+H2S(g)‘ΎΡ≥Έ¬Ε»œ¬¥οΒΫΤΫΚβΘ§œ¬Ν–Ης÷÷«ιΩωœ¬Θ§≤ΜΜα ΙΤΫΚβΖΔ…ζ“ΤΕ·ΒΡ «
NH3(g)+H2S(g)‘ΎΡ≥Έ¬Ε»œ¬¥οΒΫΤΫΚβΘ§œ¬Ν–Ης÷÷«ιΩωœ¬Θ§≤ΜΜα ΙΤΫΚβΖΔ…ζ“ΤΕ·ΒΡ «
A. Έ¬Ε»ΓΔ»ίΜΐ≤Μ±δ ±Θ§Ά®»κSO2ΤχΧε B. ΫΪNH4HSΙΧΧε»Ϊ≤Ω“ΤΉΏ
C. »ίΤςΧεΜΐ≤Μ±δΘ§≥δ»κΒΣΤχ D. ±Θ≥÷―Ι«Ω≤Μ±δΘ§≥δ»κΒΣΤχ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ηNAΈΣΑΔΖϋΌΛΒ¬¬ό≥Θ ΐΒΡ ΐ÷ΒΘ§œ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «Θ® Θ©
A.23gNa”κΉψΝΩH2OΖ¥”ΠΆξ»ΪΚσ ß»Ξ2NAΗωΒγΉ”
B.1molCuΚΆΉψΝΩ»»≈®ΝρΥαΖ¥”ΠΩ……ζ≥…NAΗωSO3Ζ÷Ή”
C.±ξΉΦΉ¥Ωωœ¬Θ§22.4LN2ΚΆH2ΜλΚœΤχ÷–Κ§2NAΗω‘≠Ή”
D.3molΒΞ÷ FeΆξ»ΪΉΣ±δΈΣFe3O4 Θ§ ß»Ξ9NAΗωΒγΉ”
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν––π ω’ΐ»ΖΒΡ «
A.…ΐΗΏΈ¬Ε»Ω…ΫΒΒΆΜνΜ·Ρή
B.ΖœΒγ≥Ί–ηΜΊ ’Θ§÷ς“Σ «“Σάϊ”ΟΒγ≥ΊΆβΩ«ΒΡΫπ τ≤ΡΝœ
C.““¥ΦΚΆΤϊ”ΆΕΦ «Ω…‘Ό…ζΡή‘¥Θ§”Π¥σΝΠΆΤΙψΓΑ““¥ΦΤϊ”ΆΓ±
D.ΆΤΙψ Ι”ΟΧΪ―τΡήΓΔΖγΡήΓΔΒΊ»»ΡήΓΔ«βΡήΘ§”–άϊ”ΎΜΚΫβΈ¬ “–ß”Π
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com