
【题目】重铬酸钾常用作有机合成的氧化剂和催化剂等。由含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)制备K2Cr2O7的流程如下图所示。

已知:I 在酸性条件下,H2O2能将Cr2O72-还原为Cr3+
II相关金属离子形成氢氧化物沉淀的pH范围如下:
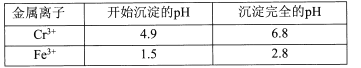
回答下列问题:
(l)滤渣②的主要成分为____(填化学式)。
(2)写出“氧化”步骤中反应的化学方程式____。
(3)“加热”操作的目的是____。
(4)“酸化”过程中发生反应2CrO42-+2H+![]() Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=____
Cr2O72-+H2O (K=4×1014L3.mol3)已知,“酸化”后溶液中c(Cr2O72-)=1.6×10-3mol/L则溶液中c(CrO42-)=____
(5)“结晶”后得到K2Cr2O7(M=294g.mol-1)产品0.5000 g,将其溶解后用稀H2SO4酸化,再用浓度为1.0000 mol.L-l (NH4)2Fe(SO4)2 标准溶液滴定,滴定终点消耗标准溶液的体积为9.00 mL,则产品的纯度为____。[滴定反应为:K2Cr2O7+6(NH4)2Fe(SO4)2+7H2SO4 =K2SO4 +Cr2(SO4)3 +6(NH4)2SO4+3Fe2(SO4)3+7H2O]
(6)在K2Cr2O7存在下,可利用微生物电化学技术实现含苯酚废水的有效处理,其工作原理如下图所示。

①负极的电极反应式为____;
②一段时间后,中间室中NaCl溶液的浓度____(填“增大”、“减小”或“不变”)。
【答案】Fe(OH)3 2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O 分解除去过量H2O2 2![]() 10-8mol/L 88.20% C6H5OH+11H2O-28e-=6CO2↑+28H+ 减小
10-8mol/L 88.20% C6H5OH+11H2O-28e-=6CO2↑+28H+ 减小
【解析】
含铬废液(主要含Cr3+、Fe3+、K+、SO42-等)加入KOH溶液调pH=7~8,生成Cr(OH)3和Fe(OH)3沉淀,过滤后得滤渣①为Cr(OH)3和Fe(OH)3;向滤渣①加入过量H2O2溶液和KOH溶液,Cr(OH)3在碱性条件下被氧化为K2CrO4进入溶液,经过滤除去滤渣②的主要成分为Fe(OH)3;滤液②经加热除去过量H2O2,冷却后酸化至pH=1,结晶析出K2Cr2O7晶体,以此分析解答。
(l)根据以上分析,滤渣②的主要成分为Fe(OH)3,
故答案为:Fe(OH)3;
(2)“氧化”步骤中Cr(OH)3在碱性条件下被H2O2氧化为K2CrO4,化学方程式为2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O,
故答案为:2Cr(OH)3+3H2O2+4KOH=2K2CrO4+8H2O;
(3) 根据题给信息,在酸性条件下,H2O2能将Cr2O72-还原为Cr3+,所以酸化之前,要除去H2O2,故 “加热”操作的目的是分解除去过量H2O2,
故答案为:分解除去过量H2O2;
(4) 2CrO42-+2H+![]() Cr2O72-+H2O ,K=
Cr2O72-+H2O ,K=![]() ,酸化后pH=1,c(H+)=0.1mol/L,c(Cr2O72-)=1.6×10-3mol/L,则溶液中c(CrO42-)=
,酸化后pH=1,c(H+)=0.1mol/L,c(Cr2O72-)=1.6×10-3mol/L,则溶液中c(CrO42-)=![]() =2
=2![]() 10-8mol/L,
10-8mol/L,
故答案为:2![]() 10-8mol/L;
10-8mol/L;
(5)根据反应关系:K2Cr2O7~6(NH4)2Fe(SO4)2,n(K2Cr2O7)=![]() n[(NH4)2Fe(SO4)2]=
n[(NH4)2Fe(SO4)2]=![]() ×1.0000 mol.L-l×0.009L=0.0015mol,则产品的纯度为
×1.0000 mol.L-l×0.009L=0.0015mol,则产品的纯度为![]() ×100%=88.20%,
×100%=88.20%,
故答案为:88.20%;
(6)①由图可知,负极发生氧化反应,C6H5OH失电子生成CO2,根据电子守恒、电荷守恒和原子守恒写出电极反应式为C6H5OH+11H2O-28e-=6CO2↑+28H+;
②负极产生的H+通过阳离子交换膜进入中间室,正极产生的OH-通过阴离子交换膜也进入中间室,H+和OH-中和生成水,溶液体积增大,NaCl溶液的浓度将减小。
故答案为:C6H5OH+11H2O-28e-=6CO2↑+28H+;减小。


科目:高中化学 来源: 题型:
【题目】将一块金属钠投入到滴有紫色石蕊试液的盛冷水的烧杯中,甲同学认为可观察到下列现象,其中正确的有( )
①钠投入水中,先沉入水底,后浮出水面
②钠立即与水反应,并有气体产生
③反应后溶液变红
④钠熔成闪亮的小球
⑤小球在水面上四处游动
⑥有“嘶嘶”的响声发出
A. ①②③④ B. ②③④⑤
C. ②④⑤⑥ D. ③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应aA(s)+bB(g)![]() cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是
cC(g) +dD(g) △H= Q ,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是

A. T1 > T2 ,Q > 0
B. Tl < T2 ,Q > 0
C. P1 > P2 ,a+b=c+d
D. Pl< P2 ,b=c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
具有自主知识产权、中国制造的C919,是一款与波音737MAX同等体量的民用飞机。制造C919需要大量的合金材料,其中包括钢,钢是现代社会的物质基础,钢中除含有铁外还含有碳和少量不可避免的硅、锰、磷、硫等元素。请回答下列有关问题:
(1)基态Mn原子的价电子排布式为___________。
(2)NO3-的立体构型名称为___________,其中心原子的杂化方式为___________。
(3)C、O、Si三种元素第一电离能由大到小的顺序是___________。
(4)写出和CN-互为等电子体的一种离子的电子式___________。
(5)铵盐大多易分解,NH4F和NH4Br两种盐中较易分解的是___________(填化学式);理由是___________。
(6)氧化亚铁晶胞与NaC1的相似,NaCl的晶胞如图所示。由于晶体缺陷,某氧化亚铁晶体的实际组成为Fe0.9O,其中包含有Fe2+和Fe3+,晶胞边长为apm,该晶体的密度为ρg·cm-3,则a=___________(列出计算式即可,用NA表示阿伏加德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C又称为抗坏血酸,在人体内有重要功能。其结构简式如图。
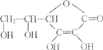
请回答下列问题:
(1)维生素C的分子式为_________,维生素C可以治疗的疾病是___________
A.坏血病 B.脑炎 C.骨折 D.肺炎
(2)小明同学在超市中购买了以下食品:苹果、西红柿、薯片、牛肉干,上述食品中,富含维生素C的是______、_______;
(3)铁是人体必需微量元素中含量最多的一种,食物中的Fe2+易被吸收,给贫血者补充铁时,应给予含Fe2+的盐,如硫酸亚铁。服用维生素C,可使食物中的Fe3+转化成Fe2+,有利于人体吸收,在该化学反应中维生素C体现____________(填“氧化”或“还原”)性。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关叙述正确的是
A.现有CO、CO2、O3三种气体,它们都含有1molO,则三种气体的物质的量之比为3:2:1
B.相同条件下,同体积、同密度的C2H4和N2,两种气体的分子数一定相等
C.28gCO和22.4LCO2中含有的碳原子数一定相等
D.配制450mL0.1mol·L-1的NaOH溶液,用托盘天平称取NaOH固体1.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
回答下列问题:

(1)反应的ΔH___0(填“大于”或“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为______mol·L-1·s-1;反应的平衡常数K1为________mol·L-1。
(2)100 ℃时达到平衡后,改变反应温度为T,N2O4以0.0020 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。则T_______100 ℃(填“大于”或“小于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g) ![]() zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是
zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系。则下列结论正确的是

A. 若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前υ(正)>υ(逆)
B. 200℃时,反应从开始到刚好达平衡的平均速率υ(B)=0.02 mol·L﹣1·min﹣1
C. 图Ⅱ所知反应xA(g)+yB(g) ![]() zC(g)的△H<0
zC(g)的△H<0
D. 200℃时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数大于0.5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列不能用勒夏特列原理解释的事实是( )
A.棕红色的NO2加压后颜色先变深后变浅
B.氢气、碘蒸气、碘化氢气体组成的平衡体系加压后颜色变深
C.黄绿色的氯水光照后颜色变浅
D.合成氨工业使用高压以提高氨的产量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com