
【题目】(1)氢气是一种理想的新能源,与化石燃料相比,氢能源有哪三大优点______、_____、____。
(2)4 g甲烷在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,写出甲烷燃烧的热化学方程式_________。
(3)拆开1mol H-H键、1mol N-H键、1mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则合成氨反应的热化学方程式为_________。
(4)已知:H2 (g) + 1/2O2(g) =H2O (g) △H = -241.8 kJ /mol ;C (s) + O2(g) =CO2(g)△H = -393.5 kJ /mol;现有0.2 mol的炭粉和氢气组成的悬浮气,混合物在氧气中完全燃烧,共放出63.53 kJ热量,则混合物中C与H2的物质的量之比为_________。
【答案】热值大 无污染 原料充足 CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ/mol N2(g)+3H2(g)![]() 2NH3(g)△H=-92kJ/mol 1﹕1
2NH3(g)△H=-92kJ/mol 1﹕1
【解析】
(1)单位质量的氢气和其他燃料相比,燃烧产生的热量多,氢气燃烧产物是水,无污染,而且氢气可以用水为原料制取,原料充足。所以氢气和其他化石燃料相比,具有热值大、无污染、原料充足等优点。
(2)4 g甲烷的物质的量为0.25mol,在氧气中燃烧生成CO2和液态水,放出222.5 kJ热量,那么1mol甲烷完全燃烧放出222.5kJ×4=890kJ的热量,所以甲烷燃烧的热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890kJ/mol。
(3)拆开1mol H-H键、1mol N-H键、1mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2(g)+3H2(g)![]() 2NH3(g)的△H=946 kJ+3×436 kJ-6×391 kJ=-92kJ,所以合成氨反应的热化学方程式为N2(g)+3H2(g)
2NH3(g)的△H=946 kJ+3×436 kJ-6×391 kJ=-92kJ,所以合成氨反应的热化学方程式为N2(g)+3H2(g)![]() 2NH3(g)△H=-92kJ/mol。
2NH3(g)△H=-92kJ/mol。
(4)设炭粉的物质的量为xmol,则氢气的物质的量为0.2-x,根据氢气和碳燃烧的热化学方程式:393.5x+241.8(0.2-x)=63.53,解得x=0.1,则混合物中C和H2 的物质的量均为0.1mol ,C与H2的物质的量之比为1﹕1。


科目:高中化学 来源: 题型:
【题目】金属锰及化合物广泛应用于工业生产、制造业等领域。
(1)科研人员将锰粉碎后加入到![]() 溶液中使其浸出(假定杂质不反应,溶液体积不变),发生反应
溶液中使其浸出(假定杂质不反应,溶液体积不变),发生反应![]() (已知含
(已知含![]() 水溶液为米黄色)
水溶液为米黄色)
①为加快上述反应速率可以采取的措施有________(写出一条即可)。不考虑温度因素,一段时间后Mn的溶解速率加快,可能的原因是_______。
②下列说明反应已达平衡的有_______(填编号)。
A.溶液的颜色不发生变化
B.溶液中![]()
C.体系中固体的质量不变
D.![]() 与
与![]() 浓度的比值保持不变
浓度的比值保持不变
③室温下,测得溶液中阳离子浓度![]() 随时间的变化情况如下图所示,则上述反应的平衡常数K=___,
随时间的变化情况如下图所示,则上述反应的平衡常数K=___,![]() 的转化率为_____。
的转化率为_____。

④若其他条件不变,10mim后向容器中迅速加入蒸馏水至溶液体积变为原来的2倍,则再次平衡时![]() =_____(不考虑离子水解的影响)。
=_____(不考虑离子水解的影响)。
(2)![]() 也可在
也可在![]() 为体系的电解液中电解获得,其阳极反应式为_____。
为体系的电解液中电解获得,其阳极反应式为_____。
(3)电解制锰后的废水中含有![]() ,常用石灰乳进行一级沉降得到
,常用石灰乳进行一级沉降得到![]() 沉淀,过滤后再向滤液中加入等体积的
沉淀,过滤后再向滤液中加入等体积的![]() 溶液,进行二级沉降,为了将
溶液,进行二级沉降,为了将![]() 的浓度降到
的浓度降到![]() ,则加入的
,则加入的![]() 溶液的浓度至少是___mol/L[已知
溶液的浓度至少是___mol/L[已知![]() ]。
]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是

A.构成原电池的两个电极必须是活泼性不同的两种金属
B.通过构成原电池,能将反应的化学能全部转化为电能
C.右图原电池中,电池工作时,SO42-移向电池的正极
D.银锌纽扣电池的放电反应:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其中Ag2O作正极,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,A、B两个装置中两个烧杯分别盛有足量的CuSO4溶液:
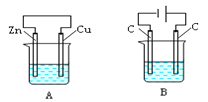
(1)A、B两个装置中属于原电池的是_____(填标号,下同),属于电解池的是____。
(2)A池中Zn是___极,发生______(填氧化或还原)反应,电极反应式为____________; Cu极电极反应式为_______;A中总反应的离子方程式为__________。
(3)B池中左边C是___极,发生______(填氧化或还原)反应,电极反应式____________;右边C极电极反应式为_________;B中总反应的化学方程式为_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_______________。
(2)氨是制备氮肥、硝酸等的重要原料②③
①己知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) ![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) ![]() 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式________________。
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式__________。

(3)反应:2NO(g)+O2(g)![]() 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。
①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:____________。

②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g) ![]() N2O2(g) △H<0
N2O2(g) △H<0
II N2O2(g)+O2(g) ![]() 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因________。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.01mol·L-1MOH溶液的pH为10。已知:2MOH(aq)+H2SO4(aq)===M2SO4(aq)+2H2O(l) ΔH1=-24.2 kJ·mol-1;H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1。则MOH在水溶液中电离的ΔH为( )
A. +33.1 kJ·mol-1 B. +45.2 kJ·mol-1
C. -81.5 kJ·mol-1 D. -33.1 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的固定容器中发生反应:N2(g)+3H2(g)2NH3(g) ΔH<0,反应过程如图所示。下列说法正确的是( )

A.t1 min时正、逆反应速率相等
B.X曲线表示NH3的物质的量随时间变化的关系
C.0~8 min,H2的平均反应速率v(H2)=0.09 mol·L-1·min-1
D.10~12 min,N2的平均反应速率v(N2)=0.25 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有四种元素基态原子电子排布式如下:
①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p3;④1s22s22p5.则下列有关比较中正确的是
A. 单电子数:③>① B. 原子半径:④>③
C. 电负性:②>① D. 最高正化合价:④>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0L恒容密闭容器中充入1.0molA,反应A(g)===B(g)+C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(B)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A. 反应在前50s的平均速率v(B)=0.0032mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(B)=0.11mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0mol A、0.20mol B和0.20mol C,反应达到平衡前v正<v逆
D. 相同温度下,起始时向容器中充入2.0mol B和2.0mol C,达到平衡时,B的转化率大于80%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com