
【题目】氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_______________。
(2)氨是制备氮肥、硝酸等的重要原料②③
①己知:N2(g)+3H2(g) ![]() 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) ![]() 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) ![]() 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式________________。
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式__________。

(3)反应:2NO(g)+O2(g)![]() 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。
①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:____________。

②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g) ![]() N2O2(g) △H<0
N2O2(g) △H<0
II N2O2(g)+O2(g) ![]() 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因________。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=________________。
【答案】AlN+H2O+OH-=AlO2-+NH3↑NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(l) △H=-382.5kJ/molN2十6H++6e-=2NH3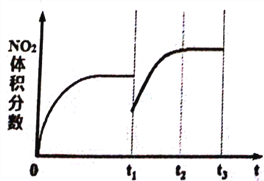 当温度升高时,反应(I)向逆反应方向进行,且由于反应I进行速率相当快,瞬间达到平衡,使得体系中c(N2O2)浓度迅速减小,所以反应(II),速率减慢180
当温度升高时,反应(I)向逆反应方向进行,且由于反应I进行速率相当快,瞬间达到平衡,使得体系中c(N2O2)浓度迅速减小,所以反应(II),速率减慢180
【解析】(1)本题考查离子方程式的书写,利用元素及其化合物知识入手,反应方程式为AlN+NaOH+H2O=NaAlO2+NH3↑,其离子反应方程式为:AlN+H2O+OH-=AlO2-+NH3↑ ;(2)①本题考查热化学反应方程式的计算,从盖斯定律入手,①N2(g)+3H2(g) ![]() 2NH3(g),②2H2(g)+O2(g)
2NH3(g),②2H2(g)+O2(g) ![]() 2H2O(1),氨气的燃烧热反应方程式为:NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(l),②×3/4-①/2得出NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(l) △H=(-571.6×3/4+92.4/2)kJ·mol-1=-382.5kJ·mol-1 ;②本题考查电解池中电极反应式的书写,电解池是制取NH3,N2的化合价由0价→-3价,化合价降低,得到电子,即左端为阴极,右端为阳极,电解质只允许质子通过,因此阴极反应式为:N2十6H++6e-=2NH3;(3)①本题考查影响化学平衡的移动,再通入2:1的NO和O2,瞬间NO2体积分数降低,平衡向正反应方向移动,NO2的体积分数增大,即图像是:
2H2O(1),氨气的燃烧热反应方程式为:NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(l),②×3/4-①/2得出NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(l) △H=(-571.6×3/4+92.4/2)kJ·mol-1=-382.5kJ·mol-1 ;②本题考查电解池中电极反应式的书写,电解池是制取NH3,N2的化合价由0价→-3价,化合价降低,得到电子,即左端为阴极,右端为阳极,电解质只允许质子通过,因此阴极反应式为:N2十6H++6e-=2NH3;(3)①本题考查影响化学平衡的移动,再通入2:1的NO和O2,瞬间NO2体积分数降低,平衡向正反应方向移动,NO2的体积分数增大,即图像是: ;②本题考查影响化学反应速率和化学平衡的因素,当温度升高时,反应(I)向逆反应方向进行,且由于反应I进行速率相当快,瞬间达到平衡,使得体系中c(N2O2)浓度迅速减小,所以反应(II),速率减慢,所以NO转化成NO的速率减慢;(4)因为CH3COOH和NH3·H2O电离平衡常数相同,因此CH3COO-和NH4+水解程度相同,即CH3COOH和NH3·H2O的浓度相同,溶液显中性, c(CH3COO-)×c(H+)/c(CH3COOH)=Ka,c(CH3COO-)/c(NH3·H2O)=Ka/c(H+)=1.8×10-5/10-7=180。
;②本题考查影响化学反应速率和化学平衡的因素,当温度升高时,反应(I)向逆反应方向进行,且由于反应I进行速率相当快,瞬间达到平衡,使得体系中c(N2O2)浓度迅速减小,所以反应(II),速率减慢,所以NO转化成NO的速率减慢;(4)因为CH3COOH和NH3·H2O电离平衡常数相同,因此CH3COO-和NH4+水解程度相同,即CH3COOH和NH3·H2O的浓度相同,溶液显中性, c(CH3COO-)×c(H+)/c(CH3COOH)=Ka,c(CH3COO-)/c(NH3·H2O)=Ka/c(H+)=1.8×10-5/10-7=180。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在一密闭的2L的容器里装有4mol SO2和2mol O2,在一定条件下开始反应。2min末测得容器中共有5.2mol 气体,试计算:
(1)2min末SO3气体的物质的量浓度;
(2)2min内O2的平均反应速率v(O2);
(3)2min末SO2的转化率.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化必须加入氧化剂且通过一步反应就能完成的是( )
①N2→NO2 ②NO2→NO ③NO2→HNO3 ④N2→NO ⑤N2→NH3
A.① B.②⑤
C.④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为六种短周期主族元素,它们的原子序数依次增大;A元素的原子半径最小;B元素原子的最外层电子数是次外层电子数的3倍;C与A同主族,且与E同周期;E元素的最外层电子数是次外层电子数的0.75倍,D既可与C的最高价氧化物的水化物反应,也可与E的最高价氧化物的水化物反应,均有A元素的单质生成。请回答下列问题:
(1)写出F的元素名称_______________,元素B在周期表中的位置_______________。
(2)判断C、D、E离子半径的从大到小顺序________________,比较B和E的气态氢化物的稳定性大小______________________。
(3)写出单质D与C的最高价氧化物的水化物反应的离子方程式___________________。
(4)写出B与C按1:1形成化合物的电子式______________________,用电子式表示B与C按1:2形成化合物的过程_________________
(5)由A、B、C、E四种元素共同构成的两种化合物在溶液中相互间可发生化学反应,试写出该反应的离子方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能大量共存的是( )
A. H+、SO42-、CO32- B. Na+、Cl-、SO42-
C. Ba2+、CO32-、NO3- D. Ca2+、SO42-、K+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )

A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】M是一种重要材料的中间体,结构简式为:(CH3)2CHCOO ![]() CHO。合成M的一种途径如下:
CHO。合成M的一种途径如下:
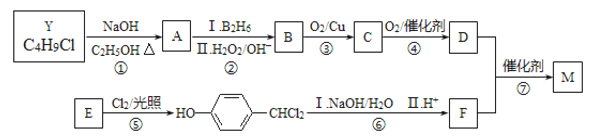
A~F分别代表一种有机化合物,合成路线中的部分产物及反应条件已略去。
已知:①RCH=CH2 ![]() RCH2CH2OH
RCH2CH2OH
两个羟基连接在同一个碳原子上不稳定,易脱水;
请回答下列问题:
(1)若Y的核磁共振氢谱只有1种峰,则Y的结构简式为____________。
(2)A的名称是____________,由B生成C的反应类型为____________。
(3)M中的官能团有____________ (填官能团名称)。
(4)步骤⑥中反应I的化学方程式为___________________________。
(5)步骤⑦的化学反应方程式是_____________________________。
(6)D的同分异构体中,能在碱性条件下水解的有_______种(不包括立体异构),其中能发生银镜反应的同分异构体的结构简式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用右图装置,完成很多电化学实验。下列有关此装置的叙述中,不正确的是
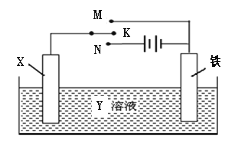
A.若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲阳极的阴极保护法
B.若X为碳棒,Y为NaCl溶液,开关K置于N处,可减缓铁的腐蚀,溶液中的阳离子向铁电极移动
C.若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,铁棒质量将增加,溶液中铜离子浓度将减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“外界条件多化学反应速率的影响”。实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢。该小组设计了如下的方案。
编号 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
浓度/ molL-1 | 体积/mL | 浓度/ molL-1 | 体积/mL | ||
① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(1)已知反应后H2C2O4转化为CO2逸出,KMnO4转化为MnSO4,标况下,每生成89.6L CO2气体,转移 mol 电子。写出H2C2O4与酸性KMnO4溶液反应的离子方程式:
(2)探究温度对化学反应速率影响的实验编号是 (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是 。本实验通过测定 来判断反应的快慢。
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=_______________ molL-1min-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com