
【题目】将一定量的SO2和含0.7mol氧气的空气(忽略CO2)放入一固定体积的密闭容器中,550℃时,在催化剂作用下发生反应:2SO2+O2![]() 2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
2SO3(正反应放热)。反应达到平衡后,将容器中的混合气体通过过量的NaOH溶液,气体体积减少了21.28L;再将剩余气体通过焦性没食子酸的碱性溶液吸收O2,气体的体积又减少了5.6L(以上气体体积均为标准状况下的体积)。请回答下列问题(计算结果保留一位小数):
(1)判断该反应达到平衡状态的标志是 。(填字母)
a.SO2和SO3浓度相等
b.SO2百分含量保持不变
c.容器中气体的压强不变
d.SO3的生成速率与SO2的消耗速率相等
e.容器中混合气体的密度保持不变
(2)欲提高SO2的转化率,下列措施可行的是 。(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.向装置中再充入SO3
(3)求该反应达到平衡时SO2的转化率为(用百分数表示) 。
(4)若将平衡混合气体的5%通入过量的Ba(OH)2溶液,生成沉淀 。
【答案】(1)bc(2)b(3)94.7%(4)10.5g或0.045mol或BaSO4
【解析】
试题分析:(1)a.可逆反应到达平衡时SO2和SO3浓度不一定相等,与二氧化硫的起始浓度以及转化率有关,a错误;b.可逆反应达到平衡状态时,各物质的百分含量不变,SO2百分含量保持不变,说明到达平衡状态,b正确;c.随反应进行气体的物质的量减小,恒温恒容下,容器内气体压强减小,当容器中气体的压强不变,说明到达平衡状态,c正确;d.SO3的生成速率与SO2的消耗速率都表示正反应速率,反应始终二者都按1:1进行,不能说明到达平衡状态,d错误;e.混合气体的质量不变,容器的体积不变,所以密度始终不变,不能说明到达平衡状态,e错误;答案选bc;
(2)a.向装置中再充入N2,反应物和生成物的浓度不变,平衡不移动,所以不能提高转化率,a错误;b.向装置中再充入O2,氧气浓度增大,平衡向正反应方向移动,提高了二氧化硫的转化率,b正确;c.改变反应的催化剂只改变反应速率,不改变平衡,所以不能提高二氧化硫的转化率,c错误;d.向装置中再充入SO3,平衡向逆反应方向移动,降低了二氧化硫的转化率,d错误;答案选b;
(3)混合气体通过过量NaOH溶液时,减少的气体是二氧化硫和三氧化硫,所以三氧化硫和未参加反应的二氧化硫的体积是21.28L,剩余氧气的体积是5.6L,则参加反应的氧气的体积=0.7mol×22.4L/mol-5.6L=10.08L,根据二氧化硫、三氧化硫和氧气的关系式知,参加氧化还原反应的二氧化硫的体积=10.08L×2=20.16L,生成三氧化硫的体积=10.08L×2=20.16L,则未参加氧化还原反应的二氧化硫的体积=21.28L-20.16L=1.12L,原来二氧化硫的体积=20.16L+1.12L=21.28L,所以二氧化硫的转化率=20.16L/21.28L×100%=94.7%;
(4)依据(3)的计算可知混合气体中生成三氧化硫气体物质的量为0.9mol,在给定的条件下,溶液呈强酸性,BaSO3不会沉淀。因此BaSO4的质量=0.9mol×5%×233g/mol=10.5g。


科目:高中化学 来源: 题型:
【题目】用铁片与稀硫酸反应制取氢气时,下列措施不能使反应速率加快的是( )
A. 不用稀硫酸,改用98%浓硫酸B. 加蒸馏水
C. 滴加少量CuSO4溶液D. 不用铁片,改用铁粉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+![]() O2(g)
O2(g)![]() CO(g) ΔH=-110.35kJ·mol-1
CO(g) ΔH=-110.35kJ·mol-1
CO(g)+![]() O2(g)
O2(g)![]() CO2(g) ΔH=-282.57kJ·mol-1
CO2(g) ΔH=-282.57kJ·mol-1
在6 g 碳不完全燃烧所得产物中,CO与CO2的体积比为2∶3, 与6 g碳完全燃烧相比,损失的热量为
A. 282.57 kJ B. 110.35 kJ C. 196.46 kJ D. 56.51 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol·L-1NH4Al(SO4)2溶液的pH随温度变化的关系如曲线1所示,下列说法中正确的是

A. 0.1mol·L-1NH4Al(SO4)2溶液c(NH4+)大于等浓度的NH4HSO4溶液中c(NH4+)
B. 向100mL0.1mol·L-1NH4Al(SO4)2溶液中逐滴滴加80mL0.05 mol·L-1NaOH 溶液时,溶液pH的变化如曲线II
C. 升高温度,NH4Al(SO4)2溶液的pH减小,是因为促进了NH4Al(SO4)2的电离
D. 20℃时,0.1mol·L-1NH4Al(SO4)2溶液中:2c(SO42-)-c(NH4+)-3c(Al3+)=10-3mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型金属氢化物镍电池(MH-Ni电池,MH为贮氢材料)工作原理如图所示。下列有关说法正确的是
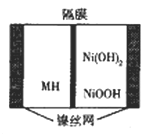
A. 隔膜为阴离子交换膜
B. 电池的电解液可为硫酸
C. 充电时阳极反应为H2O+M+e-=MH+OH-
D. 放电时负极反应为Ni(OH)2+OH—-e-==NiOOH+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com