
| ��+��-4���� |
| 2 |
| 574+1160+4��44 |
| 2 |
| 1 |
| 2 |


 ��ʦ����ָ���ο�ʱϵ�д�
��ʦ����ָ���ο�ʱϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HOCH2CH2COOCH2CH3 |
| B��HOCH2CH2CH2CH2COOH |
| C��CH3CH2CH��OH��CH2COOH |
| D��CH3CH��OH��CH2CH2COOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
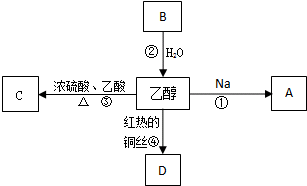 2011��5��1���𣬡��л������̷����������ˣ�����ʽʵʩ�����Ƽ�ʻ��ΪΣ�ռ�ʻ�ﱻ����ʻ���������Σ����Ƽ�ʻ�Ľ綨��Ϊ��ÿ�ٺ���ѪҺ�еľƾ��������ڻ����80���ˣ��൱��3���ͶȰƻ���2ƿơ�ƣ��Ҵ��������г������л���ܽ�����ͼ��ʾ�Ķ��ַ�Ӧ��A��B��C��D���Ǻ�̼���������B������
2011��5��1���𣬡��л������̷����������ˣ�����ʽʵʩ�����Ƽ�ʻ��ΪΣ�ռ�ʻ�ﱻ����ʻ���������Σ����Ƽ�ʻ�Ľ綨��Ϊ��ÿ�ٺ���ѪҺ�еľƾ��������ڻ����80���ˣ��൱��3���ͶȰƻ���2ƿơ�ƣ��Ҵ��������г������л���ܽ�����ͼ��ʾ�Ķ��ַ�Ӧ��A��B��C��D���Ǻ�̼���������B�������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
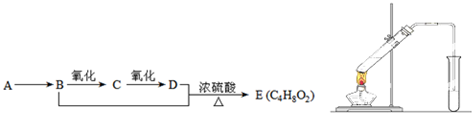
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| X | Y | ||
| Z | W |
| A��Z���ʵ��۵������ֵ�������͵� |
| B��Y������������ˮ����������ǿ |
| C��̼Ԫ�ؿ���W�γ�ֱ���ͷ��� |
| D��ZY4���ɼ��Լ��γɵļ��Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
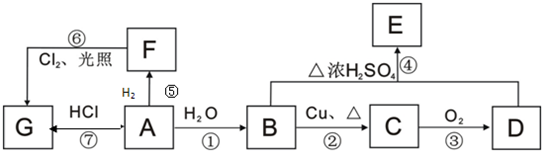
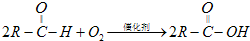 ��R��ʾ����������ش��������⣺
��R��ʾ����������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
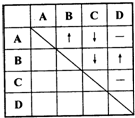 Ϊ��ȷ����ƿʧȥ��ǩ����ɫ��Һ�����Ƿֱ���ϡ���ᡢϡ���ᡢ����������̼������Һ��ijͬѧ������������ϵķ��������ܽ���ƿ��Һ�ֱ���ΪA��B��C��D��Ȼ���ȡ�������Թ���������ϣ����۲쵽�������������ʾ����-����ʾ����������������ʾ�г������ɣ���������ʾ���������ɣ�����
Ϊ��ȷ����ƿʧȥ��ǩ����ɫ��Һ�����Ƿֱ���ϡ���ᡢϡ���ᡢ����������̼������Һ��ijͬѧ������������ϵķ��������ܽ���ƿ��Һ�ֱ���ΪA��B��C��D��Ȼ���ȡ�������Թ���������ϣ����۲쵽�������������ʾ����-����ʾ����������������ʾ�г������ɣ���������ʾ���������ɣ������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��1����һ�������£���ˮ��Һ�� 1molCl-��ClOx-��x=1��2��3��4����������kJ������Դ�С��ͼ��ʾ��
��1����һ�������£���ˮ��Һ�� 1molCl-��ClOx-��x=1��2��3��4����������kJ������Դ�С��ͼ��ʾ��| 1 |
| 2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com