
【题目】用![]() 表示阿伏加得罗常数,下列说法不正确的是
表示阿伏加得罗常数,下列说法不正确的是
A.对于![]() ,每当新形成
,每当新形成![]() 个
个![]() 键,需要断开
键,需要断开![]() 个
个![]() 键
键
B.![]() 熔融的
熔融的![]() 中含有的阳离子数为
中含有的阳离子数为![]()
C.次氯酸光照分解产生![]() 气体
气体![]() 标准状况
标准状况![]() 转移的电子数为
转移的电子数为![]()
D.电解精炼铜时,若阴极析出32g铜,则转移的电子数为![]()
【答案】C
【解析】
A.对于![]() ,每当形成
,每当形成![]() 个
个![]() 键,需要形成
键,需要形成![]() 二氧化硅,反应消耗了
二氧化硅,反应消耗了![]() 硅原子;由于1mol硅原子形成了4个共价键,根据均摊法,1mol硅原子形成了
硅原子;由于1mol硅原子形成了4个共价键,根据均摊法,1mol硅原子形成了![]() 键,所以反应
键,所以反应![]() 硅需断开1mol硅硅键,即断裂
硅需断开1mol硅硅键,即断裂![]() 个
个![]() 键,故A正确;
键,故A正确;
B.![]() 熔融的
熔融的![]() 的物质的量为
的物质的量为![]() ,
,![]() 熔融硫酸氢钠电离出
熔融硫酸氢钠电离出![]() 钠离子和
钠离子和![]() 硫酸氢根离子,所以含有的阳离子数为
硫酸氢根离子,所以含有的阳离子数为![]() ,故B正确;
,故B正确;
C.发生反应![]() ,产生的气体为HCl、
,产生的气体为HCl、![]() ,生成混合气体的物质的量为
,生成混合气体的物质的量为![]() ,故生成氧气的物质的量为
,故生成氧气的物质的量为![]() ,反应中氧元素化合价由
,反应中氧元素化合价由![]() 价升高为0价,故转移电子数目为
价升高为0价,故转移电子数目为![]() ,故C错误;
,故C错误;
D.电解精炼铜时,阴极反应:![]() ,所以当阴极质量增重32g即析出
,所以当阴极质量增重32g即析出![]() 铜时,转移的电子的物质的量为1mol,则阴极得到的电子数为
铜时,转移的电子的物质的量为1mol,则阴极得到的电子数为![]() ,故D正确;
,故D正确;
故选:C。


科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d是淡黄色粉末,m为元素Y的单质,通常为无色无味的气体。上述物质的转化关系如图所示。下列说法错误的是( )
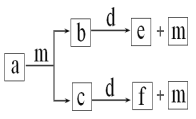
A.简单离子半径:Z<Y
B.简单气态氢化物的热稳定性:Y>X
C.阴离子的还原性:Y>W
D.W2Y2中含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氯化锡(SnCl4)常作有机合成的催化剂,在空气中极易水解生成SnO2·xH2O,实验室用熔融的锡(熔点为231.9℃)与氯气反应来制备(同时有SnCl2生成),该反应是放热反应。可选用的仪器及装置如图所示。
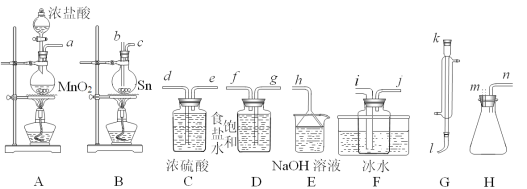
SnCl2、SnCl4有关物理性质如表:
物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
SnCl2 | 无色晶体 | 246 | 623 |
SnCl4 | 无色液体 | -33 | 114 |
(1)已知SnCl2、SnCl4晶体类型相同,SnCl2熔沸点高于SnCl4的原因是:___。
(2)选择装置进行连接(填各接口的字母,装置可重复使用,空格可不填满)。___
a→__,__→__,__→__,__→__,__→__,__→__,__→__,__→__。
(3)反应开始时,应先点燃装置___(填“A”或“B”,下同)的酒精灯,待___时,再点然装置___的酒精灯,并在反应进行中仍持续加热,其目的是___。
(4)该方法制得的SnCl4中含有少量SnCl2,提纯SnCl4的实验名称是___。
(5)测定产品纯度。取ag产品溶于少量浓盐酸,加入蒸馏水稀释至250mL。取20mL稀释溶液于锥形瓶,滴加几滴淀粉溶液,用cmol·L-1I2溶液滴定至终点,消耗滴定溶液V mL。
①该产品中SnCl2含量为___%。(滴定反应:Sn2++I2=Sn4++2I-,SnCl2的相对分子质量为:190)
②若操作时间过长、振荡剧烈,测得产品中SnCl4含量__(填“偏高”或“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸(HOOC-COOH)是一种常见的有机酸,利用淀粉制备草酸的实验流程如图:
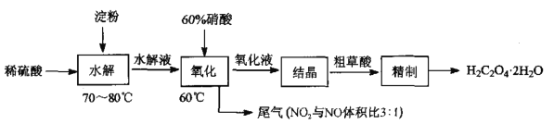
回答下列问题:
(1)“水解”时,检验淀粉是否水解完全,所用的试剂是____;“水解”及“氧化”步骤中适宜的加热方式是________________。
(2)“氧化”时实验装置如图所示(夹持及加热装置已略):
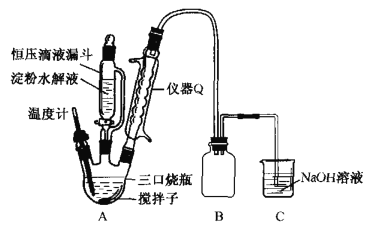
①仪器Q的名称是________.
②三口烧瓶中生成H2C2O4· 2H2O的化学方程式为____________。
③装置B的作用是___________,装置C的作用是_______________。
(3)已知在20℃、70℃时,草酸的溶解度依次为为9. 5 g/(l00g水),84.5g/(l00g水),则粗草酸“精制”需采用的提纯方法为___________________。
(4)探究H2C2O4的性质:
①向NaHCO3溶液中加入草酸溶液,产生大量气体,可得出草酸的酸性比碳酸_____(填“强”或“弱”)。
②向草酸中加入足量C2H5OH和适量浓硫酸加热,产生有芳香气味的油状物。该生成物为___________(写结构简式)。
③向K2Cr2O7溶液中加入H2C2 O4·2H2O析出K[Cr(C2O4)2(H2O)2]晶体,该反应的化学方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上一般采用下列两种反应合成甲醇。反应Ⅰ:CO(g)+2H2(g) ![]() CH3OH(g) ΔH1
CH3OH(g) ΔH1
反应Ⅱ:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH2
CH3OH(g)+H2O(g) ΔH2
下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K):
温度 | 250 ℃ | 300 ℃ | 350 ℃ |
K | 2.0 | 0.27 | 0.012 |
(1)由表中数据判断ΔH1________(填“>”、“<”或“=”)0;反应CO2(g)+H2(g) ![]() CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
CO(g)+H2O(g) ΔH3=___________(用ΔH1和ΔH2表示)。
(2)若容器容积不变,则下列措施可提高反应Ⅰ中CO转化率的是________(填字母序号)
A.充入CO,使体系总压强增大 B.将CH3OH(g)从体系中分离
C.充入He,使体系总压强增大 D.使用高效催化剂
(3)保持恒温恒容条件对于反应Ⅱ:将10 mol CO2和30mol H2放入1 L的密闭容器中,充分反应后测得CO2的转化率为60%,则该反应的平衡常数为____________________。若维持条件不变向该容器中投入10 mol CO2、30mol H2、10 mol CH3OH(g)和 10mol H2O(g),判断平衡移动的方向是________(填“正向移动”、“逆向移动”或“不移动”)。
(4)反应Ⅰ的逆反应速率与时间的关系如图所示。由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:t2时_______________________;t8时______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是___(填编号)。若测定结果偏高其原因可能是__(填字母)。
A.配制标准溶液的固体NaOH中混有Na2O杂质
B.滴定终点读数时,俯视滴定管的刻度,其他操作正确
C.盛装待测液的锥形瓶用蒸馏水洗过后再用待测液润洗
D.滴定到终点读数时,发现滴定管尖嘴处悬挂一滴溶液
(2)判断滴定终点的现象是___。
(3)如图是某次滴定时滴定管中的液面,其读数为___mL。
(4)根据下列数据,请计算待测盐酸的浓度:___molL-1。
滴定次数 | 待测体积(mL) | 标准NaOH溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国化学家研究的一种新型复合光催化剂[碳纳米点(CQDs)/氮化碳(C3N4)纳米复合物]可以利用太阳光实现高效分解水,其原理如图所示。下列说法正确的是

A. C3N4中C的化合价为 -4
B. 反应的两个阶段均为吸热过程
C. 阶段Ⅱ中,H2O2既是氧化剂,又是还原剂
D. 通过该反应,实现了化学能向太阳能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的氯气通入50mL浓度为![]() 的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、
的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、![]() 共存体系。下列判断正确的是
共存体系。下列判断正确的是
A.与NaOH反应的氯气一定为![]() mol
mol
B.![]() :
:![]() 可能为7:3
可能为7:3
C.若反应中转移的电子为n mol,则![]()
D.![]() :
:![]() :
:![]() 可能为11:1:2
可能为11:1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期元素原子半径与原子序数的关系图,下列说法正确的是( )
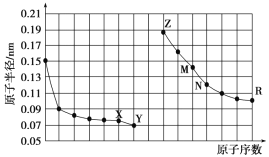
A. M、N的氧化物都能与Z、R的最高价氧化物对应水化物反应
B. Y的单质能从含R简单离子的水溶液中置换出R单质
C. X、M两种元素组成的化合物熔点很高
D. 简单离子的半径:R>M>X
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com