
【题目】早在1913年就有报道说,在400℃以上AgI晶体的导电能力是室温时的上万倍,可与电解质溶液相比。
(1)已知Ag元素的原子序数为47,则Ag元素在周期表中的位置是_____________,属于_____区,基态Ag原子的价电子排布式为__________。
(2)硫代硫酸银(Ag2S2O3)是微溶于水的白色化合物,它能溶于过量的硫代硫酸钠(Na2S2O3)溶液生成[Ag(S2O3)2]3-等络阴离子。在[Ag(S2O3)2]3-中配位原子是______(填名称),配体阴离子的空间构型是______,中心原子采用_____杂化。
(3)碘的最高价氧化物的水化物有HIO4(偏高碘酸,不稳定)和H5IO6(正高碘酸)等多种形式,它们的酸性HIO4_____ H5IO6(填:弱于、等于或强于)。氯、溴、碘的氢化物的酸性由强到弱排序为______(用化学式表示),其结构原因是______。
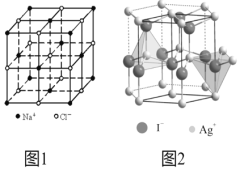
(4)在离子晶体中,当0.414<r(阳离子):r(阴离子)<0.732时,AB型化合物往往采用和NaCl晶体相同的晶体结构(如下图1)。已知r(Ag+):r(I-)=0.573,但在室温下,AgI的晶体结构如下图2所示,称为六方碘化银。I-的配位数为______,造成AgI晶体结构不同于NaCl晶体结构的原因不可能是_______。
a. 几何因素 b. 电荷因素 c. 键性因素
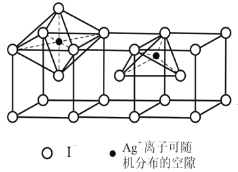
(5)当温度处于146~555℃间时,六方碘化银转化为α–AgI(如下图),Ag+可随机地分布在四面体空隙和八面体空隙中,多面体空隙间又彼此共面相连。因此可以想象,在电场作用下,Ag+可从一个空隙穿越到另一个空隙,沿着电场方向运动,这就不难理解α–AgI晶体是一个优良的离子导体了。则在α–AgI晶体中,n(Ag+)﹕n(八面体空隙)﹕n(四面体空隙)= ______________。
【答案】第五周期IB族 ds 4d105s1 硫 四面体形 sp3 强于 HI>HBr>HCl 氯、溴、碘的原子半径逐渐增大,H—Cl、 H—Br、 H—I的键长逐渐增大,共价键键能逐渐减弱,所以HI更容易电离出H+,酸性更强 4 ab 1﹕3﹕6
【解析】
根据同族元素来确定Ag元素的位置和价电子排布式;由价层电子对互斥理论确定杂化轨道和空间构型;含氧酸中非羟基氧原子个数越多酸性越强;四面体空隙:由四个球体围成的空隙,球体中心线围成四面体;八面体空隙:由六个球围成的空隙,球体中心线围成八面体形;根据均摊法确定离子个数、八面体空隙和四面体空隙的个数。
(1)已知Ag元素的原子序数为47,第四周期有18种元素,47-18=29,29号元素为Cu,则Ag元素在周期表中应在Cu的下方,Cu原子的价电子为3d104s1,Cu元素在第四周期IB族,属于ds区,所以则Ag元素在周期表中的位置是第五周期IB族,属于ds区,基态Ag原子的价电子排布式为4d105s1。
(2) 硫代硫酸根中因为硫比氧半径更大,所以与银离子的亲和性更好,所以[Ag(S2O3)2]3-中配位原子是硫;配体阴离子![]() -的中心原子是硫,另一个硫原子相当于氧原子,则中心原子硫的孤电子对数为
-的中心原子是硫,另一个硫原子相当于氧原子,则中心原子硫的孤电子对数为![]() ,价层电子对数为4+0=4,所以空间构型是四面体形,中心原子采用sp3杂化。
,价层电子对数为4+0=4,所以空间构型是四面体形,中心原子采用sp3杂化。
(3) H5IO6(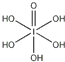 )中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,含非羟基氧原子个数越多酸性越强,所以酸性HIO4强于H5IO6;氯、溴、碘的氢化物为HCl、 HBr、 HI,由于氯、溴、碘的原子半径逐渐增大,H—Cl、 H—Br、 H—I的键长逐渐增大,共价键键能逐渐减弱,所以HI更容易电离出H+,酸性更强,故酸性由强到弱排序为HI>HBr>HCl;
)中含有5个羟基氢,为五元酸,含非羟基氧原子1个,HIO4为一元酸,含有1个羟基氢,含非羟基氧原子3个,含非羟基氧原子个数越多酸性越强,所以酸性HIO4强于H5IO6;氯、溴、碘的氢化物为HCl、 HBr、 HI,由于氯、溴、碘的原子半径逐渐增大,H—Cl、 H—Br、 H—I的键长逐渐增大,共价键键能逐渐减弱,所以HI更容易电离出H+,酸性更强,故酸性由强到弱排序为HI>HBr>HCl;
(4) 如下图2, 离I-最靠近的Ag+的有四个,所以I-配位数为4;由于r(Ag+):r(I-)=0.573,在0.414<r(阳离子):r(阴离子)<0.732范围内,但是晶体结构和NaCl晶体不同,所以a几何因素不可以作为晶体结构的原因;AgI和NaCl的阴阳离子的电荷比相同,所以b电荷因素不可以作为晶体结构的原因;Ag+和I-离子半径大,受相反电荷离子的电场作用变成椭球形,不再维持原来的球形,离子键就向共价键过渡,它们的成键具有离子键和共价键的双重特性,其离子键的纯粹程度不高,离子键的纯粹程度简称键性因素,所以造成AgI晶体结构不同于NaCl晶体结构的原因是键性因素,答案选ab。
离I-最靠近的Ag+的有四个,所以I-配位数为4;由于r(Ag+):r(I-)=0.573,在0.414<r(阳离子):r(阴离子)<0.732范围内,但是晶体结构和NaCl晶体不同,所以a几何因素不可以作为晶体结构的原因;AgI和NaCl的阴阳离子的电荷比相同,所以b电荷因素不可以作为晶体结构的原因;Ag+和I-离子半径大,受相反电荷离子的电场作用变成椭球形,不再维持原来的球形,离子键就向共价键过渡,它们的成键具有离子键和共价键的双重特性,其离子键的纯粹程度不高,离子键的纯粹程度简称键性因素,所以造成AgI晶体结构不同于NaCl晶体结构的原因是键性因素,答案选ab。
(5)如图取最小的单元,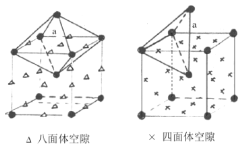 八面体空隙在面心(6个)和棱上(12个),有
八面体空隙在面心(6个)和棱上(12个),有![]() 个,四面体空隙在面心,每个面心四个,有
个,四面体空隙在面心,每个面心四个,有![]() 个,每个晶胞含有
个,每个晶胞含有![]() 个离子,则n(Ag+)﹕n(八面体空隙)﹕n(四面体空隙)=2﹕6﹕12= 1﹕3﹕6。
个离子,则n(Ag+)﹕n(八面体空隙)﹕n(四面体空隙)=2﹕6﹕12= 1﹕3﹕6。


 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:
【题目】用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
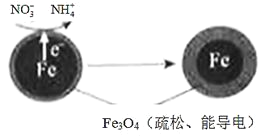
①作负极的物质是_________。
②正极的电极反应式是_________。
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 接近100% | <50% |
24小时pH | 接近中性 | 接近中性 |
铁的最终物质形态 |
|
|
pH=4.5时,NO3-的去除率低。其原因是_________。
(3)其他条件与(2)相同,经1小时测定NO3-的去除率和pH,结果如下:
初始pH | pH=2.5 | pH=4.5 |
NO3-的去除率 | 约10% | 约3% |
1小时pH | 接近中性 | 接近中性 |
与(2)中数据对比,解释(2)中初始pH不同时,NO3-去除率和铁的最终物质形态不同的原因:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在学校科技节活动中表演了“滴水生火”、“吹气生火”的小魔术。如图所示,在蒸发皿上放一小团脱脂棉,在里面裹入一种淡黄色的化合物,对着脱脂棉吹气或者用胶头滴管滴几滴水,一会儿脱脂棉会燃烧起来。
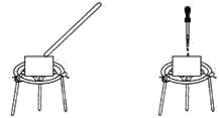
(1)淡黄色的化合物为___。
(2)由“滴水生火”的小魔术可以得出Na2O2和H2O发生反应的依据:a.有氧气生成;b.__。该反应的化学方程式是___。
(3)“吹气生火”的过程中发生的化学反应方程式为__,用双线桥标出反应中电子转移的方向和数目:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一包白色粉末,由BaCl2、K2SO4、CaCO3、NaOH、CuSO4中的一种或几种组成,为了探究它的成份,进行了如下实验:下列判断正确的是( )
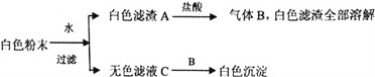
A.BaCl2、CaCO3一定存在,NaOH可能存在
B.K2SO4、CuSO4一定不存在
C.K2SO4、NaOH、CaCO3、BaCl2一定存在,K2SO4可能存在
D.C为单一溶质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。
2NO2(g),随温度升高,混合气体的颜色变深。
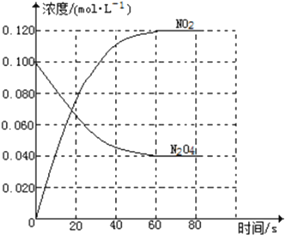
回答下列问题:
(1)反应的△H______0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如上图所示。在0~60s时段,反应速率v(N2O4)为___________molL-1s-1反应的平衡常数K1为___________。
(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_______100℃(填“大于”“小于”),判断理由是_____。
②列式计算温度T是反应的平衡常数K2___________
(3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向___________(填“正反应”或“逆反应”)方向移动,判断理由是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在Na2SO4和Al2(SO4)3的混合溶液中,测得Al3+浓度为0.1mol·L-1,加入等体积0.3 mol·L-1的BaCl2溶液恰好使SO42-完全沉淀,则混合溶液中Na+的浓度为____。
(2)将0.1mol·L-1的K2SO4溶液、0.2mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、SO42-的浓度分别为0.1mol·L-1、0.1mol·L-1、0.2mol·L-1,则K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比___。(忽略体积的变化)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有以下合成路线(部分反应条件已省略),下列有关说法错误的是

A.物质A的名称为乙炔,其电子式为![]()
B.物质B中所有原子可能共平面
C.物质C的同分异构体中含有苯环且苯环上有两个取代基的有3种
D.反应③的反应条件为O2、Cu加热,反应类型为氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)接触法制硫酸工艺中,其主反应是在恒容、温度为450℃并有催化剂存在的条件下进行:
2SO2(g)+O2(g) ![]() 2SO3(g) ΔH=-190Kj/mol
2SO3(g) ΔH=-190Kj/mol
①下列描述中能说明上述反应已达平衡的是____________。
a. ![]() (O2)正=2
(O2)正=2![]() (SO3)逆 b.容器中气体的密度不随时间而变化
(SO3)逆 b.容器中气体的密度不随时间而变化
c.容器中气体的平均相对分子质量不随时间而变化 d.容器中气体的分子总数不随时间而变化
②在一个固定容积为5L的密闭容器中充入0.20molSO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则![]() (O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
(O2)=__________mol·L-1·min-1,若继续通入0.40 mol SO2和0.20molO2则平
衡______移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡后,________mol3) <_____mol。
(2)工业生成尿素的原理是以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3 (g)+ CO2(g) ![]() CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
T/℃ | 165 | 175 | 185 | 195 |
K | 111.9 | 74.1 | 50.6 | 34.8 |
①ΔH_______0(填“>”、“<”或“=”)
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)![]() =x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。
=x,下图是氨碳比(x)与CO2平衡转化率(α)的关系,α随着x增大而增大的原因是___________。

③右图中的B点对应的NH3的平衡转化率为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吉林某化工厂发生爆炸,导致1个硝基苯储罐、2个苯储罐报废,导致苯酚、苯胺停产。爆炸过程还产生了大量的浓烟和强烈的刺激性气味,造成了空气污染。
(1)写出上述材料中提到的4种有机物中,任意两种有机物的结构简式①_______,②_________。
(2)爆炸过程中,产生了大量黑烟,其原因是_____________
(3)上述爆炸事故附近的江水有强烈苦杏仁气味,苯、硝基苯、二甲苯等主要污染物指标均超过国家标准。具有苦杏仁味的有机物是________,它在江水中的主要存在形式是___________。
(4)硝基苯是制造染料的重要原料,但是硝基苯进入人体,严重危害人体健康,写出实验室由苯制取硝基苯反应的化学方程式_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com