
【题目】下列说法正确的是( )
A. 物质发生化学反应时必然伴随着能量变化
B. 金属铜导电,故金属铜是电解质
C. 自发反应都是熵增大的反应
D. 增大反应物浓度,可增大单位体积内活化分子的百分数,从而使反应速率增大
科目:高中化学 来源: 题型:
【题目】综合利用CO2、CO对构建低碳社会有重要意义。
(1) H2 和CO合成甲醇反应为:CO(g)+2H2(g)![]() CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为_______;10min内用H2表示的化学反应速率为_______;若要加快CH3OH的生成速率并提高CO的转化率,可采取的措施有_______(填一种合理的措施)。
CH3OH(g)(正反应是放热反应)。在恒温,体积为2L的密闭容器中分别充入1.2mol CO和1mol H2,10min后达到平衡,测得含有0.4mol CH3OH(g)。则达到平衡时CO的浓度为_______;10min内用H2表示的化学反应速率为_______;若要加快CH3OH的生成速率并提高CO的转化率,可采取的措施有_______(填一种合理的措施)。

(2) 二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:CO2(g) +3H2(g) ![]() CH3OH(g) +H2O(g)+Q。
CH3OH(g) +H2O(g)+Q。
①该反应的平衡常数表达式为K=________。②在恒容密闭容器中使CO2和H2(物质的量之比为1∶3)发生上述反应,反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如下图所示,则Q_________0(填“大于”或“小于”)
(3) 如下图所示,利用缺铁氧化物[如Fe0.9O]可实现CO2的综合利用。请说明该转化的2个优点_____________。若用1 mol缺铁氧化物[Fe0.9O]与足量CO2完全反应可生成________mol C(碳)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用吸附了氢气的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是 ( )
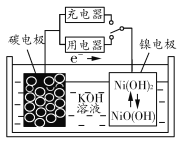
A.放电时,负极的电极反应式为H2-2e-+2OH-=2H2O
B.充电时,阳极的电极反应式为Ni(OH)2+OH--e-=NiO(OH)+H2O
C.放电时,OH-移向镍电极
D.充电时,将电池的碳电极与外电源的正极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于胶体的叙述中,错误的是
A.胶体的本质特征是其分散质粒子直径为1-100nm
B.胶体是胶状的纯净化合物
C.利用丁达尔效应可区分溶液和胶体
D.将饱和FeCl3溶液滴入沸水中,再煮沸可形成红褐色的胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宋代著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载,“银针验毒”的原理是4Ag+2H2S+O2=2X+2H2O,其中H2S是
A.既不是氧化剂又不是还原剂 B.还原剂
C.既是氧化剂又是还原剂 D.氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Ca(OH)2的饱和溶液中存在平衡:Ca(OH)2(s) ![]() Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
Ca2+(aq)+2OH-(aq) ΔH<0,下列有关该平衡体系的说法正确的是( )
A. 升高温度,平衡正向移动
B. 向溶液中加入少量碳酸钠粉末能增大钙离子浓度
C. 恒温下向溶液中加入CaO,溶液的pH不变
D. 向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关![]() 分子结构的下列叙述中正确的是
分子结构的下列叙述中正确的是
①除苯环外的其余碳原子有可能都在一条直线上
②除苯环外的其余碳原子不可能都在一条直线上
③12个碳原子不可能都在同一平面上
④12个碳原子有可能都在同一平面上
A. ①② B. ②③ C. ①③ D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com