
【题目】芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素。相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子个数之和是氧原子数的5倍。已知:各有机物间存在如下转化关系:
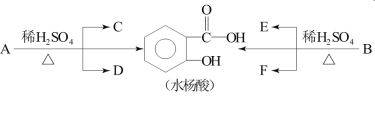
其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类有机物。
(1)A的分子式是________。
(2)E中所含官能团的名称是________;完全燃烧时,1 mol D与1 mol下列________的耗氧量相同(填字母代号)。
a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(3)写出水杨酸与小苏打反应的化学方程式是___________;写出C与F反应的化学方程式是_________。
(4)同时符合下列要求的同分异构体有___________种。
①与A互为同分异构体;
②能发生水解反应;
③苯环上有两个取代基,且苯环上的一氯代物只有1种。
(5)1 mol 上述(4)中的一种有机物X,能与4 mol NaOH发生反应,写出此反应的化学方程式__________
【答案】C10H10O4 羧基 ac 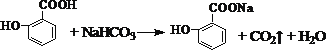 CH3OH+HCOOH
CH3OH+HCOOH ![]() HCOOCH3+H2O 3
HCOOCH3+H2O 3 ![]() +4NaOH
+4NaOH![]() 2CH3COONa+
2CH3COONa+![]() +2H2O
+2H2O
【解析】
A、B蒸气对氢气的相对密度是97,则相对分子质量为194,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍,设C原子数为n,则H原子数为n,O原子数为![]() ,则12n+n+
,则12n+n+![]() ×16=194,n=10,分子式为C10H10O4,C能发生银镜反应,应含有醛基,F经连续氧化可生成C,说明F为醇,C为酸且含有醛基,应为HCOOH,则F为CH3OH;C与D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,由此可知A为
×16=194,n=10,分子式为C10H10O4,C能发生银镜反应,应含有醛基,F经连续氧化可生成C,说明F为醇,C为酸且含有醛基,应为HCOOH,则F为CH3OH;C与D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,由此可知A为![]() ,E为CH3COOH,B为
,E为CH3COOH,B为![]() ,据此分析。
,据此分析。
A、B蒸气对氢气的相对密度是97,则相对分子质量为194,分子中C、H原子个数相同,且C、H原子总数是氧原子数的5倍,设C原子数为n,则H原子数为n,O原子数为![]() ,则12n+n+
,则12n+n+![]() ×16=194,n=10,分子式为C10H10O4,C能发生银镜反应,应含有醛基,F经连续氧化可生成C,说明F为醇,C为酸且含有醛基,应为HCOOH,则F为CH3OH;C与D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,由此可知A为
×16=194,n=10,分子式为C10H10O4,C能发生银镜反应,应含有醛基,F经连续氧化可生成C,说明F为醇,C为酸且含有醛基,应为HCOOH,则F为CH3OH;C与D是相对分子质量相同的不同类有机物,则D应为CH3CH2OH,由此可知A为![]() ,E为CH3COOH,B为
,E为CH3COOH,B为![]() 。
。
(1)由以上分析可知A的分子式为C10H10O4;
(2)E为CH3COOH,所含官能团的名称是羧基;
D为CH3CH2OH,1molCH3CH2OH完全燃烧消耗(2+![]() -
-![]() )mol=3mol氧气,
)mol=3mol氧气,
a消耗氧气为3+![]() -
-![]() -
-![]() =4.5mol,c消耗氧气为2+
=4.5mol,c消耗氧气为2+![]() =3mol,d消耗氧气为2+
=3mol,d消耗氧气为2+![]() -
-![]() =2.5mol,
=2.5mol,
答案选ac;
(3)水杨酸含有-COOH,可与碳酸氢钠反应,但酚羟基不反应,则反应的方程式为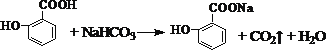 ;
;
C为HCOOH,F为CH3OH,二者可发生酯化反应,反应的方程式为CH3OH+HCOOH ![]() HCOOCH3+H2O;
HCOOCH3+H2O;
(4)A为![]() ,对应的同分异构体能水解,说明含有酯基,苯环上有两个取代基,且苯环上的一氯代物只有1种,说明取代基相同,且位于对位,可能的同分异构体有
,对应的同分异构体能水解,说明含有酯基,苯环上有两个取代基,且苯环上的一氯代物只有1种,说明取代基相同,且位于对位,可能的同分异构体有![]() 、
、![]() 、
、![]() 共3种;
共3种;
(5)1 mol 上述(4)中的一种有机物X,能与4 mol NaOH发生反应,则X为![]() ,此反应的化学方程式为
,此反应的化学方程式为![]() +4NaOH
+4NaOH![]() 2CH3COONa+
2CH3COONa+![]() +2H2O。
+2H2O。


科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)画出Mg原子结构示意图:________。
(2)![]() 微粒中的中子数为________。
微粒中的中子数为________。
(3)11.0g由 ![]() H和
H和 ![]() O组成的水分子,其中含电子的物质的量为________mol。
O组成的水分子,其中含电子的物质的量为________mol。
(4)以下7种物质 ①NaCl溶液 ②Cu ③酒精(C2H5OH) ④熔融KNO3 ⑤BaSO4固体 ⑥干冰 ⑦稀硫酸 其中:属于电解质的是________(填序号,下同);属于非电解质的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯酸钾和亚硫酸氢钾溶液能发生氧化还原反应:ClO3-+3HSO3-=3SO42-+ Cl-+3H+。己知该反应的速率随c(H+)的增大而加快。右图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法中不正确的是 ( )

A. 反应开始时速率增大可能是c(H+)所致
B. 纵坐标为v(Cl-)的v-t曲线与图中曲线完全重合
C. 图中阴影部分的面积表示t1~t2时间内ClO3-的物质的量的减少量
D. 后期反应速率下降的主要原因是反应物浓度减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】临床证明磷酸氯喹对治疗“新冠肺炎”有良好的疗效。磷酸氯喹的结构如图所示。下列有关磷酸氯喹的说法错误的是( )
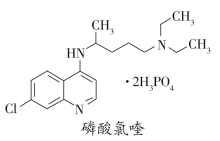
A.分子式是C18H32ClN3O8P2
B.能发生取代、加成和消去反应
C.1mol磷酸氯喹最多能与5molH2发生加成反应
D.分子中的—C1被—OH取代后的产物能与溴水作用生成沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH____NaOH溶液的pH(填“>”“=”或“<”)。
(2)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c(NH4+)=c(Cl-),则盐酸的体积___氨水的体积(填“>”“=”或“<”)。
(3)将0.2 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积变化忽略不计),测得混合溶液中c(Na+)>c(A-),则:
①混合溶液中,c(A-)________c(HA)(填“>”“<”或“=”,下同);
②混合溶液中,c(HA)+c(A-)________0.1 mol·L-1。
(4)常温时,取0.1 mol·L-1HX溶液与0.1 mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1 mol·L-1NaOH溶液中由水电离出的c(OH-)之比为________。
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH____7(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是![]()
A.在![]()
![]() 溶液中,
溶液中,![]()
B.在![]() 某二元弱酸强碱盐NaHA溶液中,
某二元弱酸强碱盐NaHA溶液中,![]()
C.![]() 和
和![]() 的混合溶液中,若
的混合溶液中,若![]() 大于
大于![]() ,则溶液显酸性
,则溶液显酸性
D.10mL![]() HCl溶液与10mL
HCl溶液与10mL![]()
![]() 溶液充分混合,若混合后溶液的体积为20mL,则溶液的
溶液充分混合,若混合后溶液的体积为20mL,则溶液的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,0.1 mol![]() 与盐酸混合所得的一组体积为1 L的溶液,溶液中部分粒子与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是
与盐酸混合所得的一组体积为1 L的溶液,溶液中部分粒子与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是
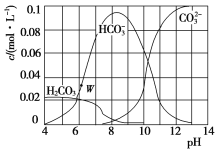
A.W点所示的溶液中:![]()
B.![]() 的溶液中:
的溶液中:![]()
C.![]() 的溶液中:
的溶液中:![]()
D.![]() 的溶液中:
的溶液中:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的位置关系如图所示,已知在同周期元素的常见简单离子中,W的简单离子半径最小,X、Y、Z、W的单质及其化合物在日常生活中用途极其广泛.
X | Y | Z | |
W |
(1)X元素在元素周期表中的位置_____________________.
(2)X 、Y、Z元素的氢化物均有两种或两种以上,其中一定条件下,液态YH3与液态H2Z可以发生类似方式电离,则液态YH3中阴离子的电子式为____________.
(3)超细WY粉末被应用于大规模集成电路领域.其制作原理为W2Z3、Y2、X在高温下反应生成两种化合物,这两种化合物均由两种元素组成,且原子个数比均为1:1;其反应的化学方程式为______.
(4)以W为材料制成的容器在空气中具有自我保护作用,这种容器______![]() 填“能”或“不能”
填“能”或“不能”![]() 用来腌制咸菜,原因是______.
用来腌制咸菜,原因是______.
(5)某汽车尾气分析仪以燃料电池为工作原理测定XZ的浓度,其装置如图所示,该电池中电解质为氧化钇![]() 氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式______
氧化钠,其中Z2-可以在固体介质NASICON中自由移动.则负极的反应式______![]() 关于该电池的下列说法,正确的是______
关于该电池的下列说法,正确的是______
A 工作时电极b作正极,Z2-通过固体介质NASICON由电极b流向电极a
B 工作时电流由电极a通过传感器流向电极b
C 传感器中通过的电流越大,尾气中XZ的含量越高
(6)由元素X与元素Z组成的某种阴离子具有还原性,能被酸性KMnO4氧化,请填写相应的离子,并给予配平:____________![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]() ______
______![]()

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com