
【题目】(1)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH____NaOH溶液的pH(填“>”“=”或“<”)。
(2)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c(NH4+)=c(Cl-),则盐酸的体积___氨水的体积(填“>”“=”或“<”)。
(3)将0.2 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积变化忽略不计),测得混合溶液中c(Na+)>c(A-),则:
①混合溶液中,c(A-)________c(HA)(填“>”“<”或“=”,下同);
②混合溶液中,c(HA)+c(A-)________0.1 mol·L-1。
(4)常温时,取0.1 mol·L-1HX溶液与0.1 mol·L-1NaOH溶液等体积混合,测得混合溶液的pH=8。
①混合溶液中由水电离出的c(OH-)与0.1 mol·L-1NaOH溶液中由水电离出的c(OH-)之比为________。
②已知NH4X溶液呈中性,又知将HX溶液加入到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH____7(填“>”“<”或“=”)。
【答案】> < < = 107:1 >
【解析】
(1)pH相等的NaOH溶液与CH3COONa溶液中c(OH-)相等,分别加热到相同的温度后,NaOH溶液中n(OH-)不变,而CH3COONa溶液中CH3COO-的水解平衡正向移动,n(OH-)增大,则CH3COONa溶液中c(OH-)大于NaOH溶液中c(OH-),故CH3COONa溶液的pH大。
(2)物质的量浓度相同的盐酸与氨水混合后,溶液中的c(NH![]() )=c(Cl-),据电荷守恒可得c(NH
)=c(Cl-),据电荷守恒可得c(NH![]() )+c(H+)=c(Cl-)+c(OH-),则有c(H+)=c(OH-),此时溶液呈中性;若两溶液恰好完全反应则生成NH4Cl,所得溶液呈酸性,若使溶液呈中性,则有V(HCl)<V(氨水)。
)+c(H+)=c(Cl-)+c(OH-),则有c(H+)=c(OH-),此时溶液呈中性;若两溶液恰好完全反应则生成NH4Cl,所得溶液呈酸性,若使溶液呈中性,则有V(HCl)<V(氨水)。
(3)①0.2 mol·L-1HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,二者充分反应后得到等浓度的HA和NaA混合液,据电荷守恒可得c(Na+)+c(H+)=c(A-)+c(OH-),测得混合溶液中c(Na+)>c(A-),则有c(H+)<c(OH-),溶液呈碱性,说明A-的水解程度大于HA的电离程度,故溶液中c(A-)<c(HA);
②据物料守恒可得,混合溶液中c(HA)+c(A-)=0.1 mol·L-1。
(4)0.1 mol·L-1 HX溶液与0.1 mol·L-1NaOH溶液等体积混合,二者恰好完全反应生成NaX,测得混合溶液的pH=8,说明X-发生了水解反应,则HX为一元弱酸。
①混合溶液中NaX发生水解反应,促进了水的电离,则由水电离出的c(OH-)=10-6 mol·L-1;0.1 mol·L-1NaOH溶液中OH-抑制了水的电离,则由水电离出的c(OH-)=10-13 mol·L-1,故两溶液中由水电离出的c(OH-)之比为(10-6 mol·L-1) :(10-13 mol·L-1)=107:1。
②HX为弱酸,NH4X溶液呈中性,说明NH![]() 和X-的水解程度相同;将HX溶液加入到Na2CO3溶液中有气体放出,说明HX的酸性强于H2CO3,根据盐类“越弱越水解”的规律可知,CO
和X-的水解程度相同;将HX溶液加入到Na2CO3溶液中有气体放出,说明HX的酸性强于H2CO3,根据盐类“越弱越水解”的规律可知,CO![]() 的水解程度大于X-,从而推知(NH4)2CO3溶液中CO
的水解程度大于X-,从而推知(NH4)2CO3溶液中CO![]() 的水解程度大于NH
的水解程度大于NH![]() ,故该溶液呈碱性,即pH>7。
,故该溶液呈碱性,即pH>7。


科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四氧化三铁(Fe3O4)磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具![]() 水热法制备Fe3O4纳米颗粒的反应是:3Fe2+ + 2S2O32-+ O2 + xOH- = Fe3O4↓+ S4O62- + 2H2O 。下列说法不正确的是
水热法制备Fe3O4纳米颗粒的反应是:3Fe2+ + 2S2O32-+ O2 + xOH- = Fe3O4↓+ S4O62- + 2H2O 。下列说法不正确的是![]()
![]()
A.参加反应的氧化剂与还原剂的物质的量之比为1:5
B.若有2molFe2+ 被氧化,则被Fe2+还原的O2的物质的量为0.5mol
C.每生成1molFe3O4,反应转移的电子为4mol
D.O2是氧化剂,S2O32-与Fe2+是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、M、R为6种短周期元素。W原子的核电荷数等于其周期数,X+与Ne具有相同的电子层结构,Y原子与Z原子的最外层电子数之和与R原子的最外层电子数相等;Y、Z、M、R在周期表中的相对位置如图所示。
Z | M | R | ||
Y |
(1)Z元素在周期表的位置为________。
(2)R离子的结构示意图为_________。
(3)X与M以1:1形成的化合物中存在的化学键类型为____________。
(4)Y的最高价氧化物与X的最高价氧化物的水化物在水溶液中发生反应的离子方程式为_________________________________。
(5)Y与Z 形成相对分子量为144的化合物与M的简单氢化物反应,生成最简单的烃和Y的最高价氧化物的水化物,该反应的化学方程式为__________________________。
(6)M与R可形成M2R2分子,该分子中各原子均达到8电子稳定结构,则M2R2的电子式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:
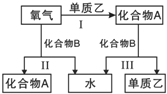
![]() 如图三个反应中,属于氧化还原反应的有______个.
如图三个反应中,属于氧化还原反应的有______个.
![]() 若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
A.还原性:![]() B.酸性:
B.酸性:![]()
C.稳定性:![]() C.沸点:
C.沸点:![]()
![]() 若化合物B常温下为气体,其水溶液呈碱性
若化合物B常温下为气体,其水溶液呈碱性![]() 答题必须用具体物质表示
答题必须用具体物质表示![]() .
.
![]() 化合物B的电子式为______;其水溶液呈碱性的原因是______
化合物B的电子式为______;其水溶液呈碱性的原因是______![]() 用离子方程式表示
用离子方程式表示![]() .
.
![]() 化合物B可与
化合物B可与![]() 组成燃料电池
组成燃料电池![]() 氢氧化钾溶液为电解质溶液
氢氧化钾溶液为电解质溶液![]() ,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
![]() 当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为
当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为![]() 和
和![]() ,则反应Ⅰ的热化学方程式为______
,则反应Ⅰ的热化学方程式为______![]() 注:反应条件相同、所有物质均为气体
注:反应条件相同、所有物质均为气体![]() .
.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芳香酯类化合物A、B互为同分异构体,均含C、H、O三种元素。相同状况下,A、B蒸气对氢气的相对密度是97,分子中C、H原子个数相同,且C、H原子个数之和是氧原子数的5倍。已知:各有机物间存在如下转化关系:
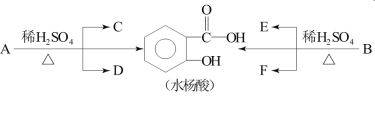
其中C能发生银镜反应,F经连续氧化可生成C;C与D是相对分子质量相同的不同类有机物。
(1)A的分子式是________。
(2)E中所含官能团的名称是________;完全燃烧时,1 mol D与1 mol下列________的耗氧量相同(填字母代号)。
a.C3H6O3 b.C3H8O c.C2H4 d.C2H6O2
(3)写出水杨酸与小苏打反应的化学方程式是___________;写出C与F反应的化学方程式是_________。
(4)同时符合下列要求的同分异构体有___________种。
①与A互为同分异构体;
②能发生水解反应;
③苯环上有两个取代基,且苯环上的一氯代物只有1种。
(5)1 mol 上述(4)中的一种有机物X,能与4 mol NaOH发生反应,写出此反应的化学方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 38.4g 铜与适量浓硝酸恰好反应生成氮的氧化物,这些氧化物恰好溶解在NaOH溶液中得到NaNO3和NaNO2的混合溶液,反应过程及有关数据如下图所示:

下列有关判断正确的是( )
A. 若浓硝酸体积为 200mL,则其物质的量浓度为 11mol/L
B. NO、NO2、N2O4 和 NaOH 溶液反应时, NO2、N2O4 仅作还原剂
C. 生成 0.2 mol NaNO3 和 0.8 mol NaNO2
D. 硝酸在反应中仅体现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“中和滴定”原理在实际生产生活中应用广泛。用I2O5可定量测定CO的含量,该反应原理为5CO+I2O5![]() 5CO2+I2。其实验步骤如下:
5CO2+I2。其实验步骤如下:
①取250 mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管中在170 ℃下充分反应;
②用水一乙醇液充分溶解产物I2,配制100 mL溶液;
③量取步骤②中溶液25.00 mL于锥形瓶中,然后用0.01 mol·L-1的Na2S2O3标准溶液滴定。消耗标准Na2S2O3溶液的体积如表所示。
第一次 | 第二次 | 第三次 | |
滴定前读数/mL | 2.10 | 2.50 | 1.40 |
滴定后读数/mL | 22.00 | 22.50 | 21.50 |
(1)步骤②中配制100 mL待测溶液需要用到的玻璃仪器的名称是烧杯、量筒、玻璃棒、胶头滴管和____________________。
(2)Na2S2O3标准液应装在__________(填字母)中。

(3)指示剂应选用__________,判断达到滴定终点的现象是____________________________________。
(4)气体样品中CO的体积分数为__________(已知:气体样品中其他成分不与I2O5反应:2Na2S2O3+I2=2NaI+Na2S4O6)
(5)下列操作会造成所测CO的体积分数偏大的是__________(填字母)。
a.滴定终点俯视读数
b.锥形瓶用待测溶液润洗
c.滴定前有气泡,滴定后没有气泡
d.配制100 mL待测溶液时,有少量溅出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水中含有大量Na+、C1-及少量Ca2+、Mg2+、SO42-,用电渗析法对该海水样品进行淡化处理,如右图所示。下列说法正确的是

A. b膜是阳离子交换膜
B. A极室产生气泡并伴有少量沉淀生成
C. 淡化工作完成后A、B、C三室中pH大小为pHA<pHB<pHC
D. B极室产生的气体可使湿润的KI淀粉试纸变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com