
 ;
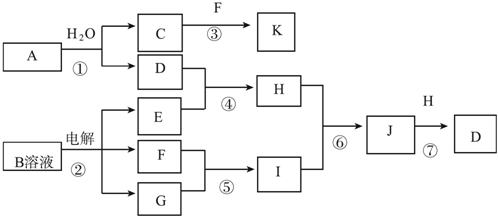
;分析 K为有机非极性溶剂,密度大于水,判断K为CCl4,由C和气体单质F生成,判断F为Cl2,而C为CH4,两者发生取代反应生成CCl4;F由B溶液电解生成,同时生成非金属气体单质G,判断G为H2,而所有元素均为短周期元素,判断B为NaCl,由此得E为NaOH,能与其反应的白色不溶于水的固体,又来自于①反应,①反应中A为两种元素组成,与水反应后生成CH4,则A中含有C元素,联想到CaC2与水的反应,确定A为金属碳化物,根据生成C和D的比例,确定A为Al4C3,则D为Al(OH)3,与E(NaOH) 反应生成的H为NaAlO2,G与F生成I为HCl,H与I(HCl)反应生成J为AlCl3,J与H反应是Al3+与AlO2-离子发生双水解生成Al(OH)3的反应.
解答 解:K为有机非极性溶剂,密度大于水,判断K为CCl4,由C和气体单质F生成,判断F为Cl2,而C为CH4,两者发生取代反应生成CCl4;F由B溶液电解生成,同时生成非金属气体单质G,判断G为H2,而所有元素均为短周期元素,判断B为NaCl,由此得E为NaOH,能与其反应的白色不溶于水的固体,又来自于①反应,①反应中A为两种元素组成,与水反应后生成CH4,则A中含有C元素,联想到CaC2与水的反应,确定A为金属碳化物,根据生成C和D的比例,确定A为Al4C3,则D为Al(OH)3,与E(NaOH) 反应生成的H为NaAlO2,G与F生成I为HCl,H与I(HCl)反应生成J为AlCl3,J与H反应是Al3+与AlO2-离子发生双水解生成Al(OH)3的反应.
(1)反应③是甲烷与氯气发生取代反应生成四氯化碳,故答案为:取代反应;
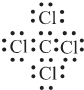
(2)A化学式是Al4C3;K是CCl4,电子式为 ,故答案为:Al4C3;
,故答案为:Al4C3; ;
;
(3)①反应的化学方程式:Al4C3+12H2O═4Al(OH)3+3CH4↑,故答案为:Al4C3+12H2O═4Al(OH)3+3CH4↑;
(4)组成F的元素为Cl,在元素周期表中的位置是:第三周期ⅦA族,故答案为:第三周期ⅦA族;
(5)E(NaOH)金属阳离子的检验方法:取E的溶液进行焰色反应,若火焰颜色为黄色,则证明有Na+,故答案为:取E的溶液进行焰色反应,若火焰颜色为黄色,则证明有Na+;
(6)反应⑦的离子方程式:Al3++AlO2-+6H2O═4Al(OH)3↓,故答案为:Al3++AlO2-+6H2O═4Al(OH)3↓;
(7)用离子方程式表示H(NaAlO2)溶液显碱性的原因:AlO2-+2H2O?Al(OH)3+OH-,故答案为:AlO2-+2H2O?Al(OH)3+OH-.
点评 本题是无机物框图推断题,考查学生对元素化合物知识的掌握和推理能力,K为推断突破口,关键是联想到CaC2与水的反应,确定A为金属碳化物,难度较大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 有A、B、C、D、E、F六种短周期元素,其元素特征信息如下:
有A、B、C、D、E、F六种短周期元素,其元素特征信息如下:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
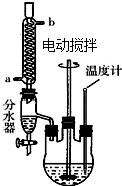 草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC-COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下:
草酸二乙酯可用于苯巴比妥等药物的中间体,实验室以草酸(HOOC-COOH)和乙醇为原料制备草酸二乙酯的实验步骤如下: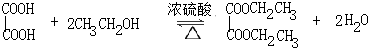 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可逆反应就是既能向正反应方向进行,又能向逆反应方向进行的化学反应 | |
| B. | 在催化剂的作用下,二氧化硫与氧气反应生成三氧化硫的同时,三氧化硫又分解生成二氧化硫和氧气,因此该反应是可逆反应 | |
| C. | 对于合成氨的反应,如果调控好反应条件,可使一种反应物的转化率达到100% | |
| D. | 碳酸钙在高温下分解生成氧化钙和二氧化碳,氧化钙和二氧化碳在常温下生成碳酸钙,因此这两个反应是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度相等的CH3COOH和CH3COONa溶液等体积混合:2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) | |
| B. | 0.1mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) | |
| D. | pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | MgCl2 | B. | NaF | C. | MgO | D. | K2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.48L | B. | 5.6L | C. | 6.72L | D. | 8.96L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子数的数目为0.1NA | |
| B. | 1molFeI2与足量氯气反应时转移的电子数为2NA | |
| C. | 1mol Na2O2固体中含离子总数为4 NA | |
| D. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com