
将锌片和铜片以下图所示两种方式分别插入同浓度稀硫酸中。
(1)以下叙述中,正确的是 (填标号)。
| A.装置甲、乙中铜片表面均无气泡产生 |
| B.装置甲、乙中稀硫酸的浓度均减小 |
| C.装置乙中锌片是正极,铜片是负极 |
| D.装置乙中产生气泡的速率比装置甲快 |
(6分,每空2分)(1)B D (2)Zn + 2H+ =Zn2+ + H2↑ ; 6.5
解析试题分析:(1)根据装置图可判断,乙装置是原电池,发生电化学腐蚀。其中锌是负极,铜是正极。甲装置发生化学腐蚀,锌直接与稀硫酸反应,而铜不能反应,据此可以解答。
乙是原电池,其中铜是正极,溶液中的氢离子在正极放电放出氢气,故A错误;两个烧杯中都产生氢气,氢离子浓度都降低,所以溶液的pH均增大,故B正确;乙是原电池,其中铜是正极,锌是负极,C不正确;通过原电池发生的反应速率要快于化学反应,选项D正确,因此答案选BD。
(2)装置乙中,总反应的离子方程式为Zn + 2H+ =Zn2+ + H2↑。若导线上通过0.2 mol电子,则根据电极反应式Zn-2e-=Zn2+可知,消耗锌的物质的量是0.1mol,质量为0.1mol×65g/mol=6.5g。
考点:考查原电池原理的有关判断、应用和计算
点评:该题是基础性试题的考查,难度不大。该题的关键是明确原电池的工作原理,特别是电极名称、电极反应式的书写,并能结合题意和装置图灵活运用即可。


科目:高中化学 来源: 题型:填空题
为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。

I.用图甲所示装置进行第一组实验时:
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是 (填序号)。
| A.石墨 | B.镁 | C.银 | D.铂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某研究性学习小组欲探究原电池的形成条件,按下图所示装置进行实验
| 序号 | A | B | 烧杯中的液体 | 指针是否偏转 |
| 1 | Zn | Cu | 稀硫酸 | 有 |
| 2 | Zn | Zn | 稀硫酸 | 无 |
| 3 | Cu | C | 氯化钠溶液 | 有 |
| 4 | Mg | Al | 氢氧化钠溶液 | 有 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
化工中把电解饱和食盐水的工业生产叫氯碱工业,其生产流程如下:
除去食盐水中的Ca2+、Mg2+、SO42—,应分别加入下列沉淀剂:①NaOH(aq)、
②Na2CO3(aq)、③BaCl2(aq),加入沉淀剂的顺序为 (填序号);加入盐酸的作用为 。
(2)下图为实验室电解饱和食盐水的实验装置。X、Y均为石墨电极,两极周围溶液均滴有几滴酚酞试液。
①电解一段时间后,X电极及附近溶液能观察到的现象是 ;
Y电极上的电极反应式为 ,检验该极产生的气体的方法是 。
②电解饱和食盐水的离子方程式为 ;若饱和食盐水体积为200mL,且忽略电解过程中的体积变化及气体溶解,当两极共收集到气体(共两种)44.8mL(标准状况)时,溶液的pH= 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
(1)甲中负极的电极反应式为____ 。
(2)乙中A极析出的气体在标准状况下的体积为____ 。
(3)丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系右图,则图中②线表示的是 离子的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要 mL 5.0 mol/L NaOH溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
如图所示表示的是电解饱和食盐水的装置,阴极材料、阳极材料都是碳棒,饱和食盐水中含有少量酚酞。
(1)接通电源后,饱和食盐水中的阳离子的移动方向是:向 极移动。
(2)电极上生成了气体A和B,生成气体A的电极反应式是 。
(3)随着气体的生成,饱和食盐水中产生了两种不同的颜色:一种是 色,其产生的位置是 (填“阴极区”或“阳极区”);另一种是 色,其产生的位置是 (填“阴极区”或“阳极区”)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe (OH)2沉淀。两电极材料分别为石墨和铁。
(1)b电极材料应为____,电极反应式为________________。
(2)电解液C可以是__________。
| A.纯净水 | B.NaCl溶液 | C.NaOH溶液 | D.CuCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
某课外活动小组同学用如图装置进行实验,试回答下列问题。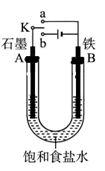
(1)若开始时开关K与b连接,则B极的电极反应式为 ,总反应的离子方程式为 ,有关上述实验,下列说法正确的是(填序号) 。
①溶液中Na+向A极移动
②从A极处逸出的气体能使湿润KI淀粉试纸变蓝
③反应一段时间后加适量盐酸可恢复到电解前电解质的浓度
④若标准状况下B极产生2.24 L气体,则溶液中转移0.2 mol电子
(2)上述实验反应一小段时间后,再把开关K与a连接,则B极的电极反应式为 。
(3)该小组同学认为如果模拟工业上离子交换膜法制烧碱的方法,则可以设想用如下图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。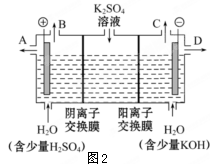
①该电解槽的阳极反应式为 。此时通过阴离子交换膜的离子数 (填”大于”或”小于”或”等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口 (填写“A”、“B”、“C”、“D”)导出。
③通电开始后,阴极附近溶液pH会增大,请简述原因 。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池,则电池正极的电极反应式为 。
⑤燃料电池所用燃料可以是氢气,也可以是其他燃料,如甲醇、肼等。液态肼(分子式N2H4)可以在氟气中燃烧生成氮气和氟化氢。利用肼、氟气与KOH溶液组成碱性燃料电池,请写出该电池负极的电极反应式? ? 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关实验的叙述正确是( )
| A.将SO2通入溴水溶液中溴水褪色,可以说明SO2有漂白性 |
| B.将淀粉和稀硫酸混合后加热,再加入银氨溶液加热,可以检验淀粉水解后的产物 |
| C.将C2H5OH与浓硫酸170℃共热,制得的气体直接通入酸性KMnO4溶液,可以检验生成的乙烯气体 |
| D.向AgCl浊液中滴加KI溶液,白色沉淀转化为黄色沉淀,可以说明AgI比AgCl更难溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com