
����Ŀ����Ҫ����գ�
��1����ϵͳ�����������������ʻ��߸�������д����Ӧ�Ľṹ��ʽ��
 _________________________
_________________________
3��4��4-����-1-��Ȳ_________________________________
��2��д�����������еĹ����ŵ����ơ�
![]() _________
_________
��3�������Ϻ� -C2H5��-CH3��-Br����ȡ������ͬ���칹����_____�֡�
��4��ij�о���ѧϰС��Ϊȷ��һ�ִ�ú����ȡ��Һ̬��X�Ľṹ���������̽����

����һ������̼�⻯��������ͨ���ȵ�����ͭ(����)�������ɶ�����̼��ˮ������װ����ˮ�Ȼ��ƺ����������Ƶ����չ���ȫ���ա�2.12g�л���X��������������7.04g������̼��1.80gˮ��
�������ͨ������������֪X����Է�������Ϊ106��
���������ú˴Ź����Dz��X��1H�˴Ź�������2���壬�����֮��Ϊ2��3 ����ͼ������
�����ģ����ú�������Dz��X���ӵĺ��������ͼ��������գ�
��X�ķ���ʽΪ___________��X��ϰ������Ϊ___________��
��������е���������������Ϊ___________��
���𰸡�5-��-2-��ϩ CH![]() CCH(CH3)C(CH3)3 ���ӣ��ǻ� �Ȼ� ���� 10 C8H10 �Զ��ױ� ����
CCH(CH3)C(CH3)3 ���ӣ��ǻ� �Ȼ� ���� 10 C8H10 �Զ��ױ� ����
��������
��1��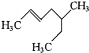 ��ϵͳ����Ϊ5-��-2-��ϩ��3��4��4-����-1-��Ȳ�Ľṹ��ʽΪCH
��ϵͳ����Ϊ5-��-2-��ϩ��3��4��4-����-1-��Ȳ�Ľṹ��ʽΪCH![]() CCH(CH3)C(CH3)3��
CCH(CH3)C(CH3)3��
��2��![]() �к��еĹ�����Ϊ�ǻ����Ȼ���������
�к��еĹ�����Ϊ�ǻ����Ȼ���������
��3�������Ϻ� -C2H5��-CH3��-Br������ͬ��ȡ������Ѱ��ͬ���칹����Է�Ϊ���࣬һ������ȡ��������λ�������֣�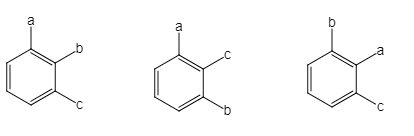 ����ƫλ����6�֣�
����ƫλ����6�֣�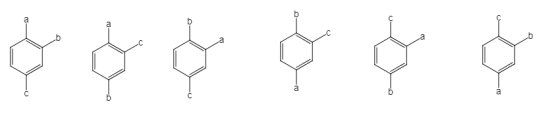 ���ڼ�λ����1�֣�
���ڼ�λ����1�֣� ������10�֣�
������10�֣�
��4������X�����ʵ���Ϊ![]() ,���ɶ�����̼Ϊ
,���ɶ�����̼Ϊ![]() ,����ˮΪ
,����ˮΪ![]() ,�������
,�������![]() ��
��![]() ,��X�ķ���ʽΪ
,��X�ķ���ʽΪ![]() ,X�ĺ�����ײⶨ���б���,���ڱ���ͬϵ��,��
,X�ĺ�����ײⶨ���б���,���ڱ���ͬϵ��,��![]() �˴Ź�������2����,�����֮��Ϊ2:3,��XΪ
�˴Ź�������2����,�����֮��Ϊ2:3,��XΪ![]() ,����Ϊ�Զ��ױ���
,����Ϊ�Զ��ױ���
�ڲ����ͨ������������֪X����Է�������,�÷�����Ϊ������


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˺������û�ѧ�ܣ�ȷ����ȫ���������������Ҫ��ֿ��ǻ�ѧ��Ӧ�ķ�Ӧ�ȣ�����ȡ��Ӧ��ʩ����ѧ��Ӧ�ķ�Ӧ��ͨ����ʵ����вⶨ��Ҳ�ɽ����������㣮
��1��ʵ���ã�5g�״���CH3OH��Һ���������г��ȼ�����ɶ�����̼�����Һ̬ˮʱ�ͷų�113.5kJ�����������ʾ�״���ȼ���ȵ��Ȼ�ѧ����Ϊ��________________��
��2���������������Ȼ�ѧ����ʽ����a_________b��������������=������������
2H2��g��+O2��g��=2H2O��g����H1=a kJmol��1
2H2��g��+O2��g��=2H2O��l����H2=b kJmol��1
��3����֪��ӦN2��g��+3H2��g���T2NH3��g����H=a kJmol��1���Ը��ݱ������м������ݹ���a ��ֵ��________________________��ע����+��������������
��ѧ�� | H��H | N��H | N��N |
����/kJmol��1 | 436 | 391 | 945 |
��4�����ݸ�˹���ɿ��Զ�ijЩ����ͨ��ʵ��ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�Ƚ������㣮����ˮú���ϳɶ����ѵ�������Ӧ���£�
��2H2��g��+CO��g���TCH3OH��g����H=��90.8kJmol��1
��2CH3OH��g���TCH3OCH3��g��+H2O��g����H=��23.5kJmol��1
��CO��g��+H2O��g���TCO2��g��+H2��g����H=��41.3kJmol��1
�ܷ�Ӧ��3H2��g��+3CO��g���TCH3OCH3��g��+CO2��g������H=_________��
��5����֪H+��aq��+OH��(aq) =H2O(l) ��H=��57.3 kJ��mol-1��
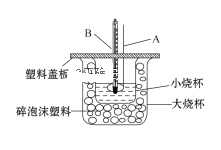
������A������___________________������ĭ���ϵ�������___________________��
������A������ͭ�ʽ�������棬��ԭ����________________________��
����ͨ��ʵ��ⶨ�к��ȵ���H�ľ���ֵ����С��57.3 kJ/mol����ԭ�������_______
a��ʵ��װ�ñ��¡�����Ч����
b����ȡNaOH��Һ�����ʱ���Ӷ���
c���ֶ�ΰ�NaOH��Һ����ʢ�������С�ձ���
d�����¶ȼƲⶨ�����ʼ�¶Ⱥ�ֱ�Ӳⶨ����������Һ���¶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ӦA(g)��3B(g) ![]() 2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ
2C(g)��2D(g)�����ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ
��v(A)��0.45 mol��L��1��min��1 ��v(B)��0.6 mol��L��1��s��1 ��v(C)��0.4 mol��L��1��s��1 ��v(D)��0.45 mol��L��1��s��1���÷�Ӧ���еĿ���˳��Ϊ
A. ��>�ۣ���>�� B. ��<�ۣ���<�� C. ��>��>��>�� D. ��>��>��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����������ͼװ�ô�����ʯȼ�Ͽ��ɡ��ӹ����̲�����H2S��������֪�����е������缫��Ϊ���Ե缫������˵������ȷ���ǣ� ��

A.�缫 a Ϊ����
B.������ĤΪ�����ӽ���Ĥ��b �缫����������ɫ����
C.��Ӧ���д���H2S�ķ�Ӧ��H2S +2Fe3+ = 2Fe2+ +S��+2H+
D.������ĤΪ���ӽ���Ĥ����NaOH��Һ��Ũ�������Ҫ���ڸ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ĵ��ʼ��仯����������ɱ������������������ϵȷ�����;�㷺��
��1����2��������������Һ��ͨ�������������Ӧ��2F2��2NaOH�T2NaF��H2O��OF2���÷�Ӧ�������뻹ԭ�������ʵ���֮��Ϊ____��OF2�ĵ���ʽΪ___��
��2��SF6��һ�������ľ�Ե������ϣ����ӽṹ��ֻ����S-F������֪1molS��s��ת��Ϊ��̬��ԭ��ʱ��������280kJ���γ�1molF-F��S-F����ų��������ֱ�Ϊ160kJ��330kJ����д����̬S���ʺͷ�����Ӧ����SF6������Ȼ�ѧ����ʽ______��
��3���ú�������ˢ���������ӻ���������[��Ҫ�ɷ�ΪCa5��PO4��3OH]������Ӧ�� Ca5��PO4��3OH��s��+F-��aq��![]() Ca5��PO4��3F��s��+OH-��aq�����÷�Ӧ��ƽ�ⳣ��K=_____����֪Ksp[Ca5��PO4��3OH]=7��l0-37��Ksp[Ca5��PO4��3F]=2.8��l0-61����
Ca5��PO4��3F��s��+OH-��aq�����÷�Ӧ��ƽ�ⳣ��K=_____����֪Ksp[Ca5��PO4��3OH]=7��l0-37��Ksp[Ca5��PO4��3F]=2.8��l0-61����
��4�����ķ���ϩ�����ڴ��ߵġ���ճͿ�㡱���Ʊ��ķ���ϩ�ķ�Ӧԭ��Ϊ��2CHClF2��g��![]() C2F4��g��+2HCl��g����H1����ӦI��������ӦΪ��3CHClF��g��
C2F4��g��+2HCl��g����H1����ӦI��������ӦΪ��3CHClF��g��![]() C3F6��g��+3HCl��g����H2����ӦII������Ӧ�ﵽƽ��ʱ����������ʵ����������¶ȵı仯��ͼ��ʾ��
C3F6��g��+3HCl��g����H2����ӦII������Ӧ�ﵽƽ��ʱ����������ʵ����������¶ȵı仯��ͼ��ʾ��
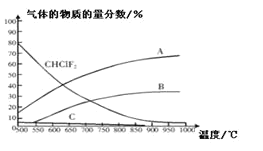
�� �ں��º��ݵ������£������ܹ�˵����ӦI�ﵽ��ѧƽ��״̬���ǣ�_________�����ţ���
A.��������ܶȲ��ٸı� B.�������ƽ����Է����������ٸı�
C.v����C2F4��=2V����HCl�� D.c��C2F4����c��HCl����ֵ���ֲ���
�� ͼ������A��ʾ�������ǣ�______���ѧʽ����
�۷�Ӧ2CHClF2��g��![]() C2F4��g��+2HCl��g���ġ�H_____0���������������
C2F4��g��+2HCl��g���ġ�H_____0���������������
�ܹ�ҵ�ϳ���900������ͨ���ѽ�CHClF2����ȡC2F4����ԭ����______��
��5��25��ʱ����amol/L��NaF��Һ�еμӵ����bmol/L������ʹ��Һ�����ԣ������������������Ļӷ���������Һ����仯������HF�ĵ���ƽ�ⳣ��Ka=______�����ú�a��b�Ĵ���ʽ��ʾ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������н������·�Ӧ�� X2(g)+Y 2(g) ![]() 2Z(g) ����֪ X 2��Y2��Z ����ʼŨ�ȷֱ�Ϊ0.1mol/L ��0.3mol/L ��0.2mol/L ����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� ( )
2Z(g) ����֪ X 2��Y2��Z ����ʼŨ�ȷֱ�Ϊ0.1mol/L ��0.3mol/L ��0.2mol/L ����һ�������£�����Ӧ�ﵽƽ��ʱ�������ʵ�Ũ���п����� ( )
A.Z Ϊ 0.3mol/LB.Y2 Ϊ 0.4mol/LC.X2 Ϊ 0.2mol/LD.Z Ϊ 0.4mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ���ǣ� ��
A.��ˮϡ��0.1mol��L-1�İ�ˮ������Һ��![]() ����
����
B.��ѧ��Ӧ�ķ�Ӧ��ֻ�뷴Ӧ;���йأ����뷴Ӧ��ϵ��ʼ̬����̬��
C.�ڵ������pH������ʹ�������Һ�зֱ�������������ͬп������ֻ��һ����Һ�е�п����ʣ�࣬�����Һһ��������
D.���ְ�ˮ�����ʵ���Ũ�ȷֱ�Ϊc1��c2��pH�ֱ�Ϊa��a��1����c2��10c1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�ⶨʯ��ʯ��Ʒ��̼��Ƶ�����������ijѧϰС�����������ʵ��̽����ȡ10gʯ��ʯ��Ʒ�����ձ��У�����ϡ���������ٲ�������Ϊֹ(ʯ��ʯ�е����ʲ�����ˮ��Ҳ����Ӧ)���������˼���ϡ�����������ų���������������ͼ(��ͼ)��
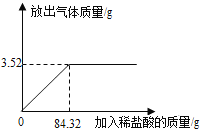
(1)̼�����ȫ��Ӧ��ȥϡ���������Ϊ__________g��
(2)��ʯ��ʯ��Ʒ��̼��Ƶ���������Ϊ_________��
(3)�������ʯ��ʯǡ����ȫ��Ӧ��������Һ����������������_____________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ö��Ե缫���һ��Ũ�ȵ�CuSO4��Һ��ͨ��һ��ʱ��������õ���Һ�м���0.1 mol Cu(OH)2��ǡ�ûָ������ǰ��Ũ�Ⱥ�pH��������˵����ȷ����( )
A��������������û����������
B����������ת�Ƶĵ��ӵ����ʵ���Ϊ0.4 mol
C��ԭCuSO4��Һ��Ũ��Ϊ0.1 mol��L��1
D���������������ռ������������Ϊ1.12 L(�����)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com