
X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为1:2,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。
请回答下列问题:
(1)元素X的最高价氧化物的电子式为__________________;元素Z的离子结构示意图为________________。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为________________。
(3)元素W位于周期表的第________族,其非金属性比R弱,用原子结构的知识解释原因:________________。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液作该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:____________________________。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为1:3,则该反应的化学方程式为_____。
解析:本题考查了原子结构、元素周期表以及元素周期律的知识,意在考查考生运用所学知识综合分析问题的能力。由X原子核外各层电子数之比为1:2,推出X为C;由Y的氧化物和R的氧化物均能形成酸雨且R的原子序数大干Y,推出Y和R分别为N和S;由W和R是同周期相邻元素且R的原子序数大于W,推出W为P;由Y原子和Z原子的核外电子数之和为20,推出Z为Al。(4)氨水与足量SO2反应生成NH4HSO3。
答案:(1)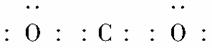 (1分)
(1分) 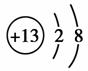 (1分)
(1分)
(2)8HNO3(稀)+3Cu===2NO↑+3Cu(NO3)2+4H2O(2分,写加热符号或不写“稀”不扣分)
(3)ⅤA(1分)P原子和S原子的电子层数相同,P原子半径较大,得电子能力较弱(2分,层数、半径和能力答对两点给1分)
(4)SO2+NH3·H2O===HSO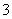 +NH
+NH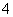 (2分,反应物写成SO2+NH3+H2O不扣分)
(2分,反应物写成SO2+NH3+H2O不扣分)
(5)Al2O3+3C+N2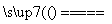 2AlN+3CO(2分)
2AlN+3CO(2分)


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
对于反应A2+3B2=2C来说,以下表示中,反应速率最快的是 ( )
A. v(B2)=0.8 mol/ (L·s) B. v(A2)=0.4 mol/ (L·s)
C. v(C)=0.6 mol/ (L·s) D. v(B2)=1.8 mol/ (L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是( )
A.元素非金属性:Z>Y>X
B.最高价氧化物对应水化物的酸性:Z>Y
C.原子半径:Z<Y<X
D.气态氢化物的稳定性:Z<Y<X
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法一定不正确的是( )
A.某些花岗石产生氡(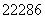 Rn),从而对人体产生伤害,
Rn),从而对人体产生伤害,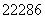 Rn的质量数是222
Rn的质量数是222
B.Se是人体必需的微量元素, Se和
Se和 Se互为同位素
Se互为同位素
C. U的浓缩一直被国际社会关注,
U的浓缩一直被国际社会关注, U与
U与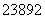 U是两种不同的核素
U是两种不同的核素
D. C-NMR(核磁共振)可用于含碳化合物的结构分析,
C-NMR(核磁共振)可用于含碳化合物的结构分析, C的中子数为6
C的中子数为6
查看答案和解析>>
科目:高中化学 来源: 题型:
元素性质呈周期性变化的决定因素是 ( )
A.元素原子半径大小呈周期性变化 B.元素的相对原子质量依次递增
C.元素的最高正化合价呈周期性变化D.元素原子核外电子排布呈周期性变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列比较中正确的是( )
A.离子还原性:S2- > Cl- > Br - > I- B. 氧化性:F2 > Cl2 > Br2 >S
C.酸性:H2SO4 > HClO4 > H3PO4 D.非金属性:F > Cl > S > O
查看答案和解析>>
科目:高中化学 来源: 题型:
对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g) ,400℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是
2NH3(g) ,400℃,30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是

A.点a的正反应速率比点b的大 B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 D.点d(t1时刻)3v正(H2)= v逆(N2)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com