
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是__;
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学队为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用___(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中SO2的体积分数为__。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中除SO2外还可能含有Q1和Q2两种气体,其中Q1气体,存标准状况下密度为0.0893g/L。为此设计了下列探究实验装置(假设有关气体完全反应)。
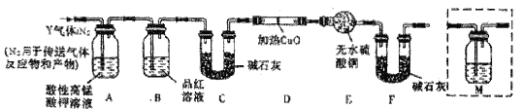
(3)装置B中试剂的作用是___。
(4)分析Y气体中的Q2气体是如何生成的___(用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加M于____(填序号)。
A.A之前 B.A—B间 C.B—C间 D.C—D间
(6)确认Q1气体存在的实验现象是____。
[探究三]如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
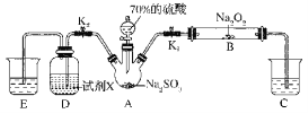
(7)下列有关说法不正确的是___
A.关闭K2,打开Kl,滴加硫酸,则装置B中每消耗1molNa2O2,转移电子数为2NA
B.关闭Kl,打丌K2,试剂X是酸性KmnO4或FeCl3溶液,均可证明SO2有还原性
C.为防止环境污染,装置C和E中的试剂均取用NaOH溶液
D.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性
【答案】常温下,铁在浓硫酸中表面被钝化 D 0.80 检验SO2是否除尽 C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O C D中固体由黑变红,E中固体由白变蓝 D
CO2↑+2SO2↑+2H2O C D中固体由黑变红,E中固体由白变蓝 D
【解析】
(1)常温下,铁遇冷的浓硫酸发生氧化还原反应,在铁表面生成一层致密的氧化物薄膜而阻止了进一步的反应,即发生钝化现象,
故答案为:常温下,铁遇浓硫酸发生钝化现象;
(2)①亚铁离子具有还原性,而酸性高锰酸钾有氧化性,发生氧化还原反应使高锰酸钾溶液褪色,铁离子和亚铁离子同时存在时,应该用酸性高锰酸钾溶液检验亚铁离子,故D正确,
故答案为:D;
②SO2+Br2+2H2O=2HBr+H2SO4,H2SO4+BaCl2=BaSO4↓+2HCl,
所以硫酸钡和二氧化硫之间的关系式为SO2~BaSO4,设二氧化硫的体积为V,
SO2~BaSO4,
22.4L 233g
V 4.66g
则:V=![]() =0.448L,所以二氧化硫的体积分数为:
=0.448L,所以二氧化硫的体积分数为:![]() ×100%=80%,
×100%=80%,
故答案为:80%;
(3)二氧化硫能使品红溶液褪色,所以用品红溶液检验二氧化硫是否除尽,
故答案为:检验SO2是否除尽;
(4)碳素钢中含有碳,加热条件下,碳能和浓硫酸反应生成二氧化硫、二氧化碳和水,反应方程式为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O,
CO2↑+2SO2↑+2H2O,
故答案为:C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O;
CO2↑+2SO2↑+2H2O;
(5)二氧化硫和二氧化碳都能使澄清石灰水变浑浊,但二氧化硫还能使品红溶液褪色,所以要检验二氧化碳必须排除二氧化硫的干扰,B装置是检验二氧化硫是否除尽,所以澄清石灰水应放置在B和C之间,即在通入碱石灰之前检验,
故答案为:c;
(6)Q1是密度最小的气体,所以Q1是氢气,氢气具有还原性,能还原黑色的氧化铜生成红色的铜单质,同时生成水,水能使无水硫酸铜变蓝色,这是检验水的特征反应,所以如果D中氧化铜变红,E中无水硫酸铜变蓝,则证明含有氢气,
故答案为:D中固体由黑色变红色和E中固体由白色变蓝色;
(7)
A.关闭K2,打开K1,滴加硫酸,则装置B中发生SO2+Na2O2=Na2SO4,每消耗1molNa2O2,转移电子数为2NA,故A正确;
B.关闭K1,打开K2,酸性KMnO4或FeCl3溶液具有强氧化性,可与二氧化硫发生氧化还原反应,均可证明SO2有还原性,故B正确;
C.饱和石灰水浓度低,不能用于尾气吸收,装置C和E中的试剂均为NaOH溶液,故C正确;
D.实验过程中体现了硫酸的酸性、难挥发性,不能体现强氧化性以及吸水性,故D错误。
答案选D。


科目:高中化学 来源: 题型:
【题目】我国第二代身份证采用的是具有绿色环保性能的PETG新材料,PETG新材料可以回收再利用,而且对周边环境不构成任何污染。PETG的结构简式如下:

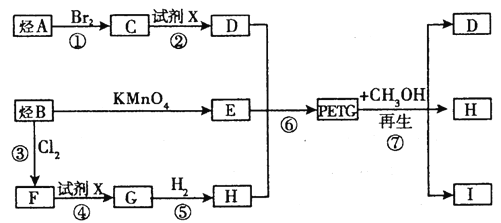
这种材料可采用如图所示的合成路线
(1)![]()
(2)RCOORl+R2OH→RCOOR2+R1OH(R、R1、R2表示烃基)
试回答下列问题:
(1) ⑦的反应类型是________________。
(2) 写出I的结构简式:___________________。
(3) 合成时应控制的单体的物质的量:n(H)∶n(E)∶n (D)=____________(用m、n表示)。
(4) 写出反应②的化学方程式:______________________
(5) 写出同时符合下列两项要求的E的所有同分异构体的结构简式。
①该同分异构体的苯环上相邻的三个碳原子上都连有取代基。
②该同分异构体在一定条件下能发生银镜反应和水解反应,遇到FeCl3溶液显紫色。
______________、_________________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀。则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )

A. Cu和浓硝酸 B. CaO和浓氨水
C. 大理石和稀盐酸 D. 高锰酸钾溶液和浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列属于非氧化还原反应的是
A. 2Mg+CO2![]() 2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
2MgO+CB. Cu(OH)2+2HCl=CuCl2+2H2O
C. SO2+H2O2=H2SO4D. Br2+2NaI=2NaBr+I2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。
(1)X、Y、Z、W、R均是1-18号元素,原子序数依次增大。X是所有元素中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R电子层数相同,R与Y最外层电子数相同,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相同。请回答下列问题:
①W的原子结构示意图___,R的简单离子的电子式___。
②X与Y元素可形成一种常用的消毒剂,其结构式为__。
③Y、Z、W、R形成的简单离子半径由大到小顺序为___(用化学符号表示)。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。根据材料回答下列问题:
①铷在元素周期表中的位置___。
②关于铷的下列说法中不正确的是___(填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(3)为验证第ⅦA族部分元素非金属性的递变规律,设计如图装置进行实验,请回答:
![]()
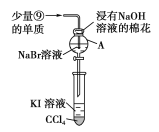
①棉花中浸有NaOH溶液的作用是___(用离子方程式表示)。
②验证溴与碘的非金属性强弱:通入少量氯气,充分反应后,将A中液体滴入试管内,取下试管,充分振荡、静置,可观察到___;该实验必须控制氯气的加入量,否则得不出溴的非金属性比碘强的结论,理由是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效、广谱、安全的杀菌、消毒剂,易溶于水。制备方法如下:
(1)步骤Ⅰ:电解食盐水制备氯酸钠。用于电解的食盐水需先除去其中的 Ca2+、Mg2+、SO42-等杂质。在除杂操作时,往粗盐水中先加入过量的________(填化学式),至沉淀不再产生后,再加入过量的________和NaOH,充分反应后将沉淀一并滤去。
(2)步骤Ⅱ:将步骤Ⅰ得到的食盐水在特定条件下电解得到氯酸钠(NaClO3),再将它与盐酸反应生成ClO2与Cl2,ClO2与Cl2的物质的量比是____________。
(3)学生拟用左下图所示装置模拟工业制取并收集ClO2,用NaClO3和草酸(H2C2O4)恒温在60℃ 时反应制得。

反应过程中需要对A容器进行加热,加热的方式为____________;加热需要的玻璃仪器除酒精灯外,还有_________________;
(4)反应后在装置C中可得亚氯酸钠(NaClO2)溶液。已知NaClO2饱和溶液在温度低于38℃时,析出的晶体是NaClO2·3H2O,在温度高于38℃时析出的是NaClO2。根据右上图所示NaClO2的溶解度曲线,请完成从NaClO2溶液中制得NaClO2·3H2O的操作步骤:
①_____________;②_______________;③洗涤;④干燥。
(5)目前我国已成功研制出利用NaClO2制取二氧化氯的新方法,将Cl2通入到NaClO2溶液中。现制取270kg二氧化氯,需要亚氯酸钠的质量是________。
(6)ClO2和Cl2均能将电镀废水中的剧毒CN-氧化为无毒物质,自身被还原为Cl-。处理含CN-相同量的电镀废水,所需Cl2的物质的量是ClO2的_______倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 4NH3+5O2 = 4NO+6H2O(g),若反应速率分别用 v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
A.v(O2)=![]() v(NH3)B.v(H2O)=
v(NH3)B.v(H2O)= ![]() v(O2)C.v(H2O)=
v(O2)C.v(H2O)=![]() v(NH3)D.v(NO)=
v(NH3)D.v(NO)= ![]() v(O2)
v(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(H2NCH2COO)2Fe],有关物质性质如下:
甘氨酸(H2NCH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含 0.10molFeSO4 的绿矾溶液。
II.制备 FeCO3: 向配制好的绿矾溶液中,缓慢加入 200mL1.1mol/LNH4HCO3 溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(H2NCH2COO)2Fe: 实验装置如下图(夹持和加热仪器已省略),将实验 II 得到的沉淀和含 0.20mol 甘氨酸的水溶液混合后加入 C 中,然后利用 A 中反应产生的气体将 C 中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。

回答下列问题:
(1)实验 I 中:配制绿矾溶液时,为防止 FeSO4 被氧化变质,应加入试剂为_________ (写化学式)。
(2)实验 II 中:生成沉淀的离子方程式为_______________________________________。
(3)实验 III 中:
①装置 A中所盛放的药品是_______ (填序号)。
a.Na2CO3 和稀 H2SO4 b.CaCO3 和稀 H2SO4 c.CaCO3 和稀盐酸
②确认 C 中空气排尽的实验现象是___________________________________________。
③加入柠檬酸溶液一方面可调节溶液的 pH 促进 FeCO3 溶解,另一个作用是________。
④洗涤实验 III 中得到的沉淀,所选用的最佳洗涤试剂是__________ (填序号)。
a.热水 b.乙醇溶液 c.柠檬酸溶液
⑤若产品的质量为 17.34g,则产率为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有____个原子共平面。
(2)金刚烷的分子式为_______,其分子中的-CH2-基团有____个。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:

其中,反应①的产物名称是_______,反应②的反应试剂和反应条件是________。
(4)已知烯烃能发生如下反应:

![]()
![]() RCHO +
RCHO + ![]()
请写出下列反应产物的结构简式:
![]()
![]() _____
_____
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com