
【题目】金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
(1)环戊二烯分子中最多有____个原子共平面。
(2)金刚烷的分子式为_______,其分子中的-CH2-基团有____个。
(3)下面是以环戊烷为原料制备环戊二烯的合成路线:

其中,反应①的产物名称是_______,反应②的反应试剂和反应条件是________。
(4)已知烯烃能发生如下反应:

![]()
![]() RCHO +
RCHO + ![]()
请写出下列反应产物的结构简式:
![]()
![]() _____
_____
【答案】9 C10H16 6 氯代环戊烷(或一氯环戊烷) NaOH醇溶液,加热 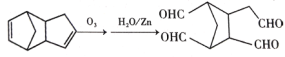
【解析】
(1)由碳碳双键为平面结构分析共平面的原子;
(2)根据C原子形成4个共价键分析;
(3)由合成路线可知,反应①为光照条件下的取代反应,反应②为卤代烃的消去反应,以此来解答;
(4)根据
![]()
![]() RCHO +
RCHO + ![]() 可知,碳碳双键两端的碳原子在
可知,碳碳双键两端的碳原子在![]()
![]() 条件下氧化为醛基。
条件下氧化为醛基。
(1)碳碳双键为平面结构,则5个C原子与4个H原子(![]() 除红圈标出的碳原子上的2个H原子外)可共面,即最多9个原子共面;
除红圈标出的碳原子上的2个H原子外)可共面,即最多9个原子共面;
(2)C原子形成4个共价键,由结构简式可知金刚烷的分子中有6个-CH2-,4个-CH-结构,分子式为C10H16;
(3)由合成路线可知,反应①为光照条件下的取代反应,产物![]() 的名称是一氯环戊烷;反应②为卤代烃的消去反应,反应条件为NaOH/醇溶液加热;
的名称是一氯环戊烷;反应②为卤代烃的消去反应,反应条件为NaOH/醇溶液加热;
(4)碳碳双键两端的碳原子在![]()
![]() 条件下氧化为醛基,所以
条件下氧化为醛基,所以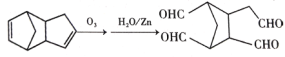 。
。


科目:高中化学 来源: 题型:
【题目】为研究铁质材料与热浓硫酸的反应,某学习小组用碳素钢(即铁和碳的合金)进行了以下探究活动:
[探究一]
(1)常温下,可以用铁质容器盛放冷的浓硫酸,其原因是__;
(2)称取碳素钢6g放入15mL浓硫酸中,加热,充分反应后得到溶液X并收集到混合气体Y。
①甲同学队为X中除Fe3+之外还可能含有Fe2+。若要确认其中的Fe2+,应选用___(选填序号)。
A.KSCN溶液和氯水 B.铁粉和KSCN溶液 C.浓氨水 D.酸性KMnO4溶液
②乙同学取560mL(标准状况)气体Y通入足量溴水中,发生SO2+Br2+2H2O=2HBr+H2SO4反应,然后加入足量BaCl2溶液,经适当操作后得干燥固体4.66g,由此推知气体Y中SO2的体积分数为__。
[探究二]根据上述实验中SO2体积分数的分析,丙同学认为气体Y中除SO2外还可能含有Q1和Q2两种气体,其中Q1气体,存标准状况下密度为0.0893g/L。为此设计了下列探究实验装置(假设有关气体完全反应)。
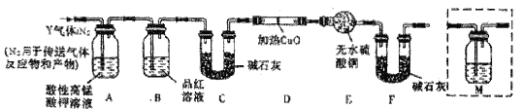
(3)装置B中试剂的作用是___。
(4)分析Y气体中的Q2气体是如何生成的___(用化学方程式表示)。
(5)已知洗气瓶M中盛装澄清石灰水,为确认Q2的存在,需在装置中添加M于____(填序号)。
A.A之前 B.A—B间 C.B—C间 D.C—D间
(6)确认Q1气体存在的实验现象是____。
[探究三]如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
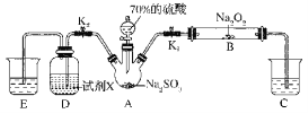
(7)下列有关说法不正确的是___
A.关闭K2,打开Kl,滴加硫酸,则装置B中每消耗1molNa2O2,转移电子数为2NA
B.关闭Kl,打丌K2,试剂X是酸性KmnO4或FeCl3溶液,均可证明SO2有还原性
C.为防止环境污染,装置C和E中的试剂均取用NaOH溶液
D.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“试剂”和“试管中的物质”不能完成“实验目的”的是

实验目的 | 试剂 | 试管中的物质 | |
A | 羟基对苯环的活性有影响 | 饱和溴水 | ①苯②苯酚溶液 |
B | 甲基对苯环活性有影响 | 酸性KMnO4溶液 | ①苯②甲苯 |
C | 苯分子中没有碳碳双键 | Br2的CCl4溶液 | ①苯②己烯 |
D | 碳酸的酸性比苯酚强 | 石蕊溶液 | ①苯酚溶液②碳酸溶液 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
A.方案①用于分离I2和NH4I固体
B.方案②用于比较CuSO4和MnO2的催化活性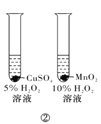
C.方案③用于测定中和热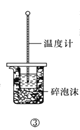
D.方案④用于比较醋酸和硼酸的酸性强弱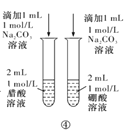
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常情况下,NCl3是一种油状液体,其分子空间构型与NH3相似,下列对NCl3和NH3的有关叙述正确的是( )
A. 分子中N—Cl键键长与CCl4分子中C—Cl键键长相等
B. NCl3分子是非极性分子
C. NBr3比NCl3易挥发
D. 在氨水中,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子,则NH3·H2O的结构式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中正确的是( )
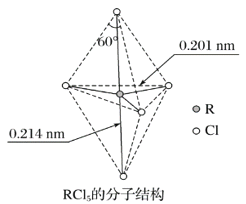
A. 每个原子都达到8电子稳定结构
B. 键角(Cl—R—Cl)有90°、120°、180°几种
C. RCl5受热后会分解生成分子RCl3,RCl5和RCl3都是极性分子
D. 分子中5个R—Cl键键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组设计如图所示的装置来验证元素非金属性的强弱:
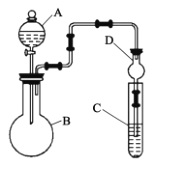
(1)仪器B的名称为___,干燥管D的作用是___。
(2)甲组同学的实验目的:证明非金属性:Cl>I。C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为___,观察到C中溶液___(填现象),即可证明。但乙组同学认为该装置有明显的缺陷,改进方案是___。
(3)丙组同学的实验目的:证明非金属性:S>C>Si。在A中加稀硫酸、B中加Na2CO3溶液、C中加Na2SiO3溶液。观察到___(填现象),即可证明。C中发生反应的化学方程式为___。
(4)丁组同学的实验目的:证明非金属性:N>C>Si。实验方案与丙组同学的相似。在A中加稀硝酸、B中加Na2CO3溶液、C中加Na2SiO3溶液。观察到与丙组同学相同的实验现象,即可证明。但丙组同学认为该方案能证明非金属性:N>C,但不能证明非金属性:C>Si,理由是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C3H7Br的有机物甲在适宜的条件下能发生如下一系列转化:

(1)若B能发生银镜反应,请回答下列问题:
①试确定有机物甲的结构简式:__________________;
②用化学方程式表示下列转化过程:
甲+NaOH![]() ________________________________________________________;
________________________________________________________;
B+Ag(NH3)2OH―→_______________________________________________________。
(2)若B不能发生银镜反应,请回答下列问题:
①试确定A的结构简式:_______________________________________________________。
②用化学方程式表示下列转化过程:
甲+NaOH![]() __________________________________________________;
__________________________________________________;
A―→B:_________________________________________________;
D―→E:___________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com