
| A�� | 0.1mol•L-1CH3COOH��Һ��ˮϡ�ͺ���Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$��ֵ���� | |
| B�� | pH=4��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ�ǡ����ȫ��Ӧ����ԭCH3COOH��Һ��CH3COOH�ĵ����Ϊ1% | |
| C�� | amol•L-1H2C2O4��Һ��2amol•L-1��NaOH��Һ�������Ϻ�c��C2O42-����c��HC2O4-����c��H2C2O4����c��OH-�� | |
| D�� | 0.1mol•L-1��������Һ�У���NH4Al��SO4��2��Һ ��NH4Cl��Һ����CH3COONH4��Һ��c��NH4+���Ĵ�С˳��Ϊ�٣��ڣ��� |
���� A��CH3COOH��Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$=$\frac{Kw}{c��{H}^{+}��}$���ݴ˻ش�
B��pH=4��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ�ǡ����ȫ��Ӧ��������Ũ����0.01mol/L�����ݵ���ȸ��������㣻
C��amol•L-1H2C2O4��Һ��2amol•L-1��NaOH��Һ�������Ϻ�õ����Dz����Ƶ���Һ�����ݲ�������ӵ�ˮ��ԭ�����жϣ�
D��NH4Al��SO4��2��Һ��笠�������������ˮ������ƣ�CH3COONH4��笠���������������ˮ����ٽ���
��� �⣺A��CH3COOH��Һ��$\frac{c��C{H}_{3}CO{O}^{-}��}{c��C{H}_{3}COOH��}$=$\frac{Kw}{c��{H}^{+}��}$��CH3COOH��Һ��ˮϡ�ͺ���Һ��������Ũ�ȼ�С�����Դ�������Ӻʹ���Ũ�ȵı�ֵ���ӣ���A��ȷ��
B��pH=4��CH3COOH��Һ��pH=12��NaOH��Һ�������Ϻ�ǡ����ȫ��Ӧ��������Ũ����0.01mol/L��ԭCH3COOH��Һ��CH3COOH�ĵ����Ϊ$\frac{0.0001mol/L}{0.01mol/L}$��100%=1%����B��ȷ��
C��amol•L-1H2C2O4��Һ��2amol•L-1��NaOH��Һ�������Ϻ�õ����Dz����Ƶ���Һ�����ݲ�������ӵ�ˮ��ԭ�����õ���c��C2O42-����c��OH-��
��c��HC2O4-����c��H2C2O4������C����
D��NH4Al��SO4��2��Һ��笠�������������ˮ������ƣ�CH3COONH4��笠���������������ˮ����ٽ������ԣ���ͬ���ʵ���Ũ�ȵ�������Һ�У���NH4Al��SO4��2����NH4Cl����CH3COONH4����c��NH4+���ɴ�С��˳���ǣ��٣��ڣ��ۣ���D��ȷ��
��ѡC��
���� ���⿼��������Ũ�ȴ�С�Ƚϣ���Ŀ�ѶȲ�����ȷ�ε�ˮ��ԭ��Ϊ���ؼ���ע����������������ε�ˮ���Ӱ�죬��������������ѧ���ķ������������������Ӧ�û���֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0.025 mol | B�� | 0.050 mol | C�� | 0.10 mol | D�� | 0.20 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Mg��HCO3��2��Һ�м�������� NaOH��Һ��Mg2++2HCO3-+4OH-=Mg��OH��2��+2CO32-+2H2O | |
| B�� | FeBr2��Һ��ͨ������ʵ���Cl2��2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | |
| C�� | ����KMnO4��Һ�м�H2O2����ɫ��ȥ��2MnO4-+H2O2+6H+=2Mn2++3O2��+4H2O | |
| D�� | ��CuSO4��Һ�м���Na2O2��2Na2O2+2Cu2++2H2O=4Na++2Cu��OH��2��+O2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
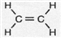
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������� | B�� | �������� | C�� | �������� | D�� | ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com