
【题目】下列相关叙述正确的是( )
A.甲烷的燃烧热为-890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B. 500℃、30MPa下,将0.5mol N2和 1.5molH2置于密闭的容器中充分反应生成NH3,放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g)![]() 2NH3(g) ; △H=-38.6kJ·mol-1
2NH3(g) ; △H=-38.6kJ·mol-1
C. H2SO4(aq)+ 2NaOH(aq)=Na2SO4(aq)+2H2O(l) △H=-114.6 kJmol-1 为 H2SO4和 NaOH 反应的中和热对应的热反应方程式
D.由 C(石墨)=C(金刚石); △H= +1.9 kJ·mol-1 可知, 金刚石比石墨能量高
科目:高中化学 来源: 题型:
【题目】【加试题】药物K可用于治疗哮喘、系统性红斑狼疮等。其合成路线如下图所示。
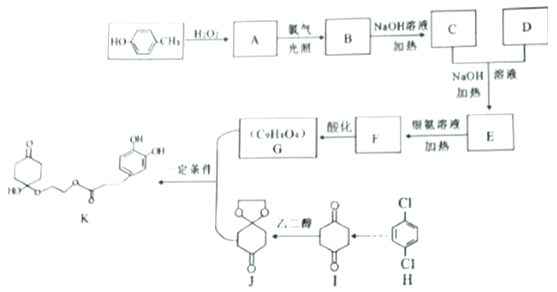
已知:
①通常在同一个碳原子上连有两个烃基不稳定,易脱水形成羰基
②醛能发生烃醛缩合反应,再脱水生成不饱和醛:
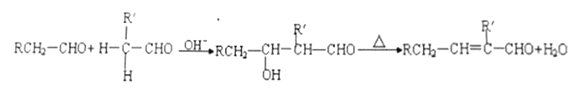
③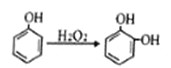
请回答:
(1)下列说法不正确的是_______
A.化合物A能与FeCl3发生显色反应
B.化合物C能够发生银镜反应
C.I转化为J属于加成反应
D.K与足量NaOH溶液反应时,1molK最多可消耗3molNaOH
(2)化合物D的结构简式为_______。
(3)E![]() F的化学方程式为___________。
F的化学方程式为___________。
(4)写成符合下列条件的A的所有同分异构体的结构简式_______。
①能与氯化铁溶液发生显色反应
②1H-NMR谱显示分子中苯环上有两种不同化学环境的氢原子
(5)通常采用有机物H为原料合成有机物I,请设计该合成路线_______(用流程图表示,无机试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用括号中的试剂及相应操作除去下列各组中的少量杂质,合理的一组是
A. 溴苯中的苯(NaOH溶液,分液) B. 乙醇中的水(新制的氧化钙,蒸馏)
C. 乙酸中的乙醇(金属钠,蒸馏) D. 苯中的甲苯(酸性高锰酸钾溶液,分液)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应(表内物质均为反应物)刚开始时,放出H2的速率最大的是( )
编号 | 金属(粉末状) | 物质的量 | 酸的浓度 | 酸的体积 | 反应温度 |
A | Mg | 0.1mol | 6mol/L硝酸 | 10mL | 60℃ |
B | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 30℃ |
C | Fe | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
D | Mg | 0.1mol | 3mol/L盐酸 | 10mL | 60℃ |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【加试题】氮及其化合物在生活和生产中应用广泛。
(1)N2O是一种强大的温室气体,在一定条件下,其分解的化学方程式为:2N2O(g)=2N2(g)+O2(g) ΔH<0,你认为该反应的逆反应是否自发进行,请判断并说明理由___________。
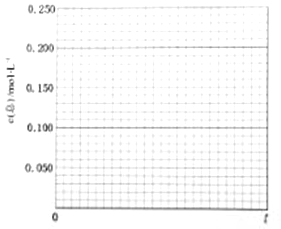
某研究小组为针对N2O的分解进行研究,常温下,在1L恒容容器中充入0.100mol N2O气体,加热到一定温度后使之反应,请画出容器中气体的总浓度c(总)随时间t变化的总趋势图。_____________
(2)①N2O5是一种新型硝化剂。工业上可用N2O4通过电解制备N2O5,阴、阳极室之间用质子交换膜隔开,两极电解液分别为稀硝酸溶液和溶有N2O4的无水硝酸,用惰性电极电解时,生成N2O5极室的电极反应式为_____________。
②已知,一定条件下有下列反应:
Ⅰ2N2O5(g)![]() 4NO2(g)+ O2(g) ΔH1
4NO2(g)+ O2(g) ΔH1
Ⅱ2NO2(g)![]() 2NO(g)+ O2(g) ΔH2
2NO(g)+ O2(g) ΔH2
Ⅲ2NaOH(aq)+N2O5(g)=2NaNO3(aq)+H2O(1) ΔH3
写出NO和O2的混合物溶于NaOH溶液生成硝酸盐的热化学方程式___________。
在容积为2L的恒容密闭容器中充入1.00mol N2O5,假设在T℃时只发生反应Ⅰ、Ⅱ,若达到平衡状态后O2为1.00mol,NO2为0.400mol,则T℃时反应Ⅰ的平衡常数的值为_________。
(3)NH3和Cr2O3固体在高温下可以制备多功能材料CrN晶体,其反应为Cr2O3(s)+2NH3(g) ![]() 2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
2CrN(s)+3H2O(g)。在800℃时,为降低相同时间内收集到的粗产品中氧的含量,通过提高反应器中NH3(g)流量的工艺手段达成,请解释可能的原因___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物不能由CH2═CH2通过加成反应制取的是( )
A.CH3CH2Cl
B.CH2Cl﹣CH2Cl
C.CH3﹣CH2OH
D.CH3﹣COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照物质的树状分类和交叉分类,HNO3应属于
①强酸
②氧化物
③含氧酸
④一元酸
⑤电解质
⑥混合物
⑦无机化合物
A.①③④⑤⑦
B.①②③④⑤⑦
C.①②③④⑥
D.①④⑥⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com