
一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol·L-1的NaOH溶液(密度为1.12 g·mL-1)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.05mol。求:
(1)原NaOH溶液的质量分数。
(2)所得溶液中Cl-的物质的量。
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
设NA代表阿伏加德罗常数的数值,下列说法中正确的是
①常温常压下,9g甲烷(CH4)所含的中子数为5NA
②常温常压下,22.4L N2气体的分子数小于NA
③64g的铜发生氧化还原反应,一定失去2NA个电子
④常温常压下,100mL 0.5mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA
⑤标准状况时,22.4L二氯甲烷所含有的分子数为NA
⑥常温常压下,1mol氦气分子含有的核外电子数为4NA。
A.①② B.②④ C.③④ D.⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
已知3.2 g某气体的分子数目为3.01×1022,由此可推知该气体的摩尔质量是
A. 64 g B. 32 g·mol-1 C. 32 g D. 64 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的饱和NaOH溶液中加入少量Na2O2固体,恢复到原来温度时,下列说法中正确的是
A.溶液中的Na+总数增大 B.溶液的碱性增强
C.溶质的质量分数不变 D.溶液的质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
溶液、胶体和浊液这三种分散系的根本区别是 ( )
A.是否大量分子或离子的集合体 B.分散质粒子直径的大小
C.是否能通过滤纸或半透膜 D.是否均一、稳定、透明
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中Cl-浓度最大的是 ( )
A.200mL 2mol/L MgCl2溶液 B.1000mL 2.5mol/L NaCl溶液
C.250mL 1mol/L AlCl3溶液 D.300mL 5mol/L KCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修3;物质结构与性质](15分)
周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。回答下列问题;
(1)b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(2)a和其他元素形成的二元共价化合物中,分子呈三角锥形,该分子的中心原子的杂化方式为______;分子中既含有极性共价键、又含有非极性共价键的化合物是________(填化学式,写出两种)。
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是________;酸根呈三角锥结构的酸是________。(填化学式)
(4)e和c形成的一种离子化合物的晶体结构如图(a),则e离子的电荷为________。
(5)这5种元素形成的一种1∶1型离子化合物中,阴离子呈四面体结构;阳离子呈轴向狭长的八面体结构[如图(b)所示]。
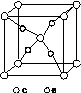
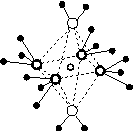
(a) (b)
该化合物中,阴离子为________,阳离子中存在的化学键类型有________;该化合物加热时首先失去的组分是________,判断理由是______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.分子中含两个氢原子的酸一定是二元酸
C.含有金属离子的晶体一定是离子晶体
D.元素的非金属型越强,其单质的活泼型一定越强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com