
【题目】①~⑨是几种有机物的名称或化学式:
①2,2,3﹣三甲基丁烷、②3﹣甲基﹣1﹣氯戊烷、③甲苯、④![]() 、 ⑤ClCH=CHCl、⑥
、 ⑤ClCH=CHCl、⑥![]() ⑦
⑦ ⑧
⑧ ⑨1,3,5﹣庚三烯
⑨1,3,5﹣庚三烯
据此回答下列问题:
(1)上述有机物中,互为同分异构体的是______(用编号表示),存在顺反异构的是______(用编号表示).
(2)以③有机物为原料制备TNT炸药的化学方程式为______.
(3)已知在有机物分子中,若某个碳原子上连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”,如 中带*的C原子。[若同一个碳原子上连着2个碳碳双键(如C═C═C)时,分子极不稳定,不存在。]⑨1,3,5﹣庚三烯的众多链烃同分异构体中:含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的______种.含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是____.
中带*的C原子。[若同一个碳原子上连着2个碳碳双键(如C═C═C)时,分子极不稳定,不存在。]⑨1,3,5﹣庚三烯的众多链烃同分异构体中:含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的______种.含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是____.
【答案】 ②和⑦ ⑤ 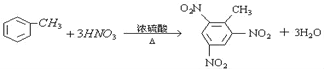 5
5 ![]() .
.
【解析】(1)分子式相同而结构不同的有机物互称同分异构体,故②和⑦互为同分异构体;当结构中有碳碳双键、且碳碳双键两端的每个碳原子上所连的两个基团不同的有机物才有顺反异构,故⑤有顺反异构,故答案为:②和⑦;⑤;
(2)甲苯在浓硫酸作用下可与浓硝酸反应生成TNT,反应的化学方程式为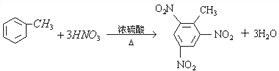 ,故答案为:
,故答案为: ;
;
(3)链烃C7H10,同一个碳原子形成2个碳碳双键(如C=C=C)时,不能稳定存在,则说明该烃中含有一个碳碳双键和一个碳碳三键,该烃中含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的同分异构体有:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,共有5种;含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”,则加成后出现了相同的基团,则其结构简式为
,共有5种;含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”,则加成后出现了相同的基团,则其结构简式为![]() ,故答案为:5;
,故答案为:5;![]() 。
。


 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A. 一定条件下反应2SO2+O2![]() 2SO3达到平衡时,v(O2)正=2v(SO3)逆
2SO3达到平衡时,v(O2)正=2v(SO3)逆
B. 用如图所示方法可保护钢闸门不被腐蚀

C. 常温下,向NH4Cl溶液中加入少量NaOH固体,溶液中![]() 的值增大
的值增大
D. 常温下, pH=2的HCl溶液与pH=12的Ba(OH)2溶液等体积混合,两者恰好完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.4.1gH3PO3可与2gNaOH完全反应生成正盐,则H3PO3为__________元酸。该正盐的电离方程式为_________________。
Ⅱ、小苏打、胃舒平、达喜都是常用的中和胃酸的药物。
(1)小苏打片每片含0.504gNaHCO3,2片小苏打片能中和胃酸中的H+是_____mol。
(2)胃舒平每片含0.234gAl(OH)3,中和胃酸时,6片小苏打片相当于胃舒平__________。
(3)达喜的化学成分是铝和镁的碱式碳酸盐。取该碱式盐粉末3.01g,逐滴加入2.0mol/L盐酸使其溶解(其他成分不与盐酸反应),当加入盐酸42.5mL时,开始产生CO2,加入盐酸至45.0mL时怡好反应完全,则该碱式盐样品中氢氧根与碳酸根的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上从含镍电镀废渣(除含镍外,还含有Cu、Zn、Fe等杂质)中制备NiCO3的工艺流程如下。
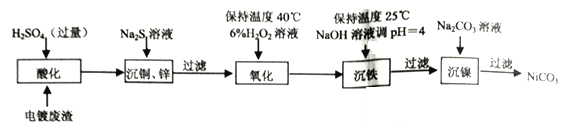
(1)“酸化”时需将电镀废渣粉碎并适当加热,原因是________________________。
(2)“氧化”时需要控制温度不超过40℃,其目的是________________________;“沉铁”后所得滤液中c(Fe3+)=____________mol·L-1[该温度下 Fe(OH))3的Ksp=2.64×10-39]。
(3)Fe2+也可以用NaCO3氧化,一定条件下可生成黄铁矾钠[Na2Fe6(SO4) 4(OH)12沉淀而被除去;如图是pH-温度关系图,图中阴影部分为黄铁矾钠稳定存在区域。

①FeOOH中铁的化合价是____________价。.
②酸性条件下,ClO3ˉ恰好氧化Fe2+时,氧化剂与还原剂物质的量之比是____________。
③根据上图,当T=120℃、pH=4时Fe元素的存在形式是____________(填化学式),该温度下,若要制得黄铁矾钠需控制pH范围____________(填字母选项)。
a.0~1 b.1~2.5 c.2.5~4
(4)已知SOCl2能与水反应生成SO2和HCl。写出NiCl2·6H2O在亚硫酰氯(SOCl2)中加热脱水制无水NCl2的化学方程式____________________________________。NCl2·6H2O需在亚硫酰氯(SOCl2)中加热脱水的原因是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素W、X、Y、Z的原子序数依次增加。p、q、r是由这些元素组成的二元化合物。m、n分别是元素Y、Z的单质,n通常为深红棕色液体,0.01 mol/L r溶液的pH为2,p被英国科学家法拉第称为“氢的重碳化合物”,s通常是难溶于水、比水重的油状液体。上述物质的转化关系如图所示。下列说法错误的是

A. q的溶液显酸性
B. W的氧化物常温常压下为液态
C. p不能使酸性高锰酸钾溶液褪色
D. Z的氧化物的水化物一定为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的密闭容器中,反应A(g)+B(g)![]() 2C(g)达到平衡状态的标志是
2C(g)达到平衡状态的标志是
A. 混合气体的质量不再发生变化
B. 容器内的总压强不再发生变化
C. 混合气体的平均相对分子质量不再发生变化
D. 单位时间内生成n mol A,同时消耗n mol B
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 硫离子的结构示意图:![]()
B. 23Na、24Mg两种核素的中子数相等,因此互为同位素
C. CH3COOH的电离方程式为:CH3COOH![]() CH3COO-+H+
CH3COO-+H+
D. 16O、1H、2H、3H四种核素可构成4种水分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系:
![]()
其中①②③均为有单质参与的反应。
(1)若A是常见的金属,①③中均有同一种气态非金属单质参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式_______________________________。
(2)如何检验上述C溶液中的阳离子?______________________。
(3)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。C的化学式是____________,写出反应①的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤的主要组成元素是碳、氢、氧、硫、氮,还有极少量的磷、砷、锗、镓、铟等元素, 燃煤产生CxHy、SO2、NOX等大气污染物,研究NO2、NO、CO、SO2等大气污染物和水污染物的处理对建设美丽中国具有重要意义。
(1)锗是第四周期第ⅣA元素,其原子结构示意图为_______________。
(2)利用煤的气化获得的水煤气(主要成分为CO、CO2和H2)在催化剂作用下可以合成绿色燃料甲醇。
已知:H2O(l)=H2O(g) △H1=+44.0kJ/mol
CO2(g)+H2(g)=CO(g)+H2O(l) △H2=-3.0 kJ/mol
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3=-58.7 kJ/mol
写出由CO与H2制备CH3OH气体的热化学方程式_________________。
(3)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3,简称DMC):
2CH3OH(g)+CO2(g)![]() CH3OCOOCH3(g)+H2O(g) △H4<0
CH3OCOOCH3(g)+H2O(g) △H4<0
①该化学反应的平衡常数表达式为K=________________。
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是_______(填标号)。
A.v正(CH3OH)= 2v逆(H2O) B.容器内气体的密度不变
C.容器内压强不变 D.CH3OH与CO2的物质的量之比保持不变
③一定条件下分别向甲、乙、丙三个恒容密闭容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如下表,反应过程中DMC的物质的量浓度随时间变化如下图所示:


甲容器中,在5-15min中的平均反应速率v(CO2) =__________。乙容器中,若平衡时n(CO2) =0.2mol,则T1__________T2(填“>”“<"或”=”)。甲、丙两容器的反应达平衡时CO2的转化率:甲__________丙(填“>”“<"或”=”)。
(4)直接排放含SO2的烟气会形成酸雨,危害环境。可用NaOH吸收,所得含硫各微粒(H2SO3、HSO3-和SO32-)存在于反应后的溶液中,它们的物质的量分数X(ⅰ)与溶液pH的关系如图所示。

①若是0.1mol/LNaOH 反应后的溶液,测得溶液的pH=8时,溶液中各离子浓度由大到小的顺序是__________________。
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2 溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com