
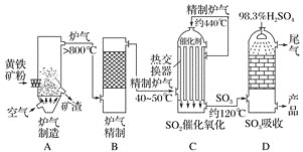
【题目】以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:
请回答下列问题:
(1)在炉气制造中,黄铁矿粉碎的目的是____________,生成二氧化硫的化学方程式是_____________。
(2)炉气精制的目的是__________________________________。
(3)二氧化硫催化氧化的化学方程式是________________________。
(4)浓硫酸是不是可以用水代替:__________,原因是__________________________________。
(5)尾气的主要成分是__________,若将尾气通入氢氧化钙浊液中,最后能得到的副产品是________。
【答案】增大反应接触的表面积,加快反应速率 4FeS2+11O2![]() 2Fe2O3+8SO2 防止催化剂中毒 2SO2+O2
2Fe2O3+8SO2 防止催化剂中毒 2SO2+O2![]() 2SO3 不可以 避免用水吸收三氧化硫形成酸雾 二氧化硫、三氧化硫和空气 石膏
2SO3 不可以 避免用水吸收三氧化硫形成酸雾 二氧化硫、三氧化硫和空气 石膏
【解析】
(1)根据外界条件对反应速率的影响分析;黄铁矿的主要成分是FeS2,在高温条件下与氧气反应生成二氧化硫和氧化铁;
(2)在催化氧化时必须进行除尘、洗涤、干燥,以达到除去砷、硒等化合物的效果,这些物质会使催化剂中毒;
(3)二氧化硫催化氧化生成三氧化硫;
(4)根据用水吸收会酸雾分析解答;
(5)根据二氧化硫的催化氧化是可逆反应以及二氧化硫能和氢氧化钙反应生成亚硫酸钙,亚硫酸钙能转化为硫酸钙判断。
(1)在炉气制造中,黄铁矿粉碎的目的是增大反应接触的表面积,加快反应速率;黄铁矿的主要成分是FeS2,在高温条件下与氧气反应生成二氧化硫和氧化铁,则生成二氧化硫的化学方程式是4FeS2+11O2![]() 2Fe2O3+8SO2。
2Fe2O3+8SO2。
(2)在催化氧化时必须进行除尘、洗涤、干燥,以达到除去砷、硒等化合物的效果,这些物质会使催化剂中毒,因此炉气精制的目的是防止催化剂中毒;
(3)二氧化硫催化氧化生成三氧化硫,反应的化学方程式是2SO2+O2![]() 2SO3。
2SO3。
(4)由于用水吸收三氧化硫会形成酸雾,所以浓硫酸是不是可以用水代替的。
(5)由于二氧化硫的催化氧化是可逆反应,所以尾气的主要成分是二氧化硫、三氧化硫和空气。若将尾气通入氢氧化钙浊液中,二氧化硫被吸收转化为亚硫酸钙,三氧化硫被吸收转化为硫酸钙。亚硫酸钙易被氧化为硫酸钙,因此最后能得到的副产品是石膏。


科目:高中化学 来源: 题型:
【题目】网络趣味图片“一脸辛酸”,是在人脸上重复画满了辛酸的键线式结构(如图)。在辛酸的同分异构体中, 含有一个“-COOH”和三个“-CH3”的结构(不考虑立体异构),除![]() 外,还有( )
外,还有( )
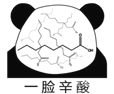
A. 7种 B. 11种 C. 14种 D. 17种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E。其中A、B、C是同一周期的非金属元素。化合物DC的晶体为离子晶体,D的二价阳离子与C的阴离子具有相同的电子层结构。AC2为非极性分子。B、C的氢化物的沸点比它们同族相邻周期元素氢化物的沸点高。E的原子序数为24,ECl3能与B、C的氢化物形成六配位的配合物,且两种配体的物质的量之比为2 :1,三个氯离子位于外界。请根据以上情况,回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序为________。
(2)B的氢化物分子的空间构型是________,其中心原子采取________杂化。
(3)写出化合物AC2的电子式________;一种由B、C组成的化合物与AC2互为等电子体,其化学式为______________。
(4)E的核外电子排布式是________,ECl3形成的配合物的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L层上有2对成对电子;E+离子核外有3层电子且M层3d轨道电子全充满。请回答下列问题:
(1)E元素基态原子的电子排布式为________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为________(填元素符号),其原因是________________________________________________________________________。
(3)D元素与氟元素相比,电负性:D________(填“>”“=”或“<”)F,下列表述中能证明这一事实的是______(填选项序号)。
A.常温下氟气的颜色比D单质的颜色深 B.氟气与D的氢化物剧烈反应,产生D的单质
C.氟与D形成的化合物中D元素呈正价态 D.比较两元素的单质与氢气化合时得电子的数目
(4)由A、C两元素可形成化合物CA5含有的化学键类型为________。
(5)B2A4是重要的石油化工原料,B2A4的结构式为________。B2A4通过聚合反应可以生成一种有机高分子化合物,反应方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,被美国食品药品监督管理局批准为心血管疾病的临床药物。其合成路线(部分反应条件略去)如下所示:

回答下列问题:
(1)A的名称为_______,E中官能团名称为________。
(2)B的结构简式为________。
(3)由C生成D的化学方程式为_________
(4)⑤的反应类型为______,⑧的反应类型为_________。
(5)F的同分异构体中,同时符合下列条件的同分异构体共有__________种。
a.能与FeCl3溶液发生显色反应 b.能发生银镜反应
其中核磁共振氢谱为五组峰的结构简式为_________。
(6)参照上述合成路线,设计一条由苯酚(![]() )、乙酸酐(CH3CO)2O和苯甲醛(
)、乙酸酐(CH3CO)2O和苯甲醛(![]() )为原料,制备
)为原料,制备 的合成路线(其他无机试剂任选)_____。
的合成路线(其他无机试剂任选)_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在严格无氧的条件下,碱与亚铁盐溶液反应生成白色胶状的 Fe(OH)2,在有氧气的情况下迅速 变为灰绿色,逐渐形成红褐色的氢氧化铁,故在制备过程中需严格无氧。现提供制备方法如下:
方法一:用 FeSO4 溶液与用不含 O2 的蒸馏水配制的 NaOH 溶液反应制备。
(1)配制 FeSO4 溶液时需加入铁粉的原因是_____;除去蒸馏水中溶解的 O2常采用_____的方法。
(2)生成白色 Fe(OH)2 沉淀的操作是用长滴管吸取不含 O2 的 NaOH 溶液,插入 FeSO4 溶液液面下,再挤出 NaOH 溶液。这样操作的理由是_____。
方法二:
在如图装置中,用 NaOH 溶液、铁屑、稀 H2SO4 等试剂制备。

(1)在试管Ⅰ里加入的试剂是_____;
(2)在试管Ⅱ里加入的试剂是_____;
(3)为了制得白色 Fe(OH)2 沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤 是_____。
(4)这样生成的 Fe(OH)2 沉淀能较长时间保持白色,其理由是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅晶体是空间立体网状结构,如图所示。下列关于二氧化硅晶体的说法中不正确的是( )
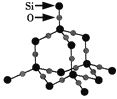
A. 1 mol SiO2晶体中含2 mol Si—O键 B. 晶体中Si、O原子个数比为1:2
C. 晶体中Si、O原子最外电子层都满足8电子稳定结构 D. 晶体中最小环上的原子数为12
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com