
| A、丁硫醇与甲硫醇及乙硫醇互为同系物 |
| B、沸点不同的丁硫醇有四种 |
| C、甲硫醇分子中含有四个共价键 |
| D、丁硫醇在空气中完全燃烧生成三氧化硫、二氧化碳和水 |


科目:高中化学 来源: 题型:
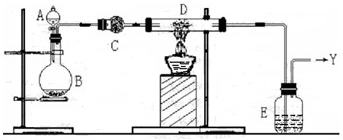 如图.B中盛装的是一种固体物质,当A中的溶液滴入B内反应一段时间后,所得产物经装置C即得纯净气体X,X分子中有10个电子,且该气体极易溶于水,一体积水能溶解700体积的该气体.D中盛装的是氧化铜,当X气体通过D时,氧化铜逐渐变成铜.最后从装置E中出来的气体是纯净的Y,Y是分子中含14个电子的单质气体.装置A、B、C、E中的药品从下列范围中选择.
如图.B中盛装的是一种固体物质,当A中的溶液滴入B内反应一段时间后,所得产物经装置C即得纯净气体X,X分子中有10个电子,且该气体极易溶于水,一体积水能溶解700体积的该气体.D中盛装的是氧化铜,当X气体通过D时,氧化铜逐渐变成铜.最后从装置E中出来的气体是纯净的Y,Y是分子中含14个电子的单质气体.装置A、B、C、E中的药品从下列范围中选择.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②③①④ | B、④①③② |
| C、③②①④ | D、③②④① |
查看答案和解析>>
科目:高中化学 来源: 题型:
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HI、H2、I2的浓度不再发生变化 |
| B、HI、H2、I2的浓度相等 |
| C、HI、H2、I2在密闭容器中共存 |
| D、反应停止,正、逆反应速率都等于零 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C(s)+O2(g)=CO2(g)△H=+393.5 kJ/mol | ||
B、C(s)+
| ||
| C、C+O2=CO2△H=-393.5 kJ/mol | ||
| D、C(s)+O2(g)=CO2(g)△H=-393.5 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com