
在恒温、恒压和使用催化剂的条件下,已知:在容积可变的密闭容器中,充入1 L含3 mol H2和1 mol N2的混合气体,反应达平衡时有a mol NH3生成,N2的转化率为b%。
(1)若在恒温、恒压和使用催化剂的条件下,在体积可变的密闭容器中充入x mol H2和y mol N2,反应达平衡时有3a mol NH3生成,N2的转化率仍为b%。则x= ; y= 。
(2)在恒温、恒压和使用催化剂的条件下,设在体积可变的密闭容器中充入x mol H2、y mol N2和z mol NH3,若达平衡时N2转化率仍为b%,则x、y的关系为 ;z的取值范围为 。
(3)在恒温[与(1)温度相同]和使用催化剂的条件下,在容积不可变的密闭容器中,充入1 L含3 mol H2和1 mol N2的混合气体,反应达平衡时N2的转化率为c%,则b、c的关系为 (用“<”、“=”或“>”表示),理由是 。
科目:高中化学 来源: 题型:
根据稳定岛假说,元素周期表的最终界限可能在175号元素左右,科学家预测114号元素位于第七周期ⅣA族,下列有关此元素的预测中,正确的是( )
A.它为非金属 B.其离子比Cu2+离子的氧化性强
C.其低价氧化物是酸性氧化物 D.它有+2价与+4价
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.只有反应体系中所有分子同时都发生有效碰撞的反应才是放热反应
B.通常条件下能够自发进行的反应必须具备△H和△S均大于0
C.任何化学反应只要是自发进行的放热反应都可以设计成原电池,为外界提供电能
D.实验室通常将固态氯化铁溶解在盐酸中,再稀释到相应浓度来配置氯化铁溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与平衡移动无关的是( )
A.向0.1 mol/L的CH3COOH中加水稀释,溶液pH增大
B.向氯水中投入AgNO3,最终溶液酸性增强
C.夏天,打开冰镇啤酒的盖子后,有大量的气泡冒出
D.在滴有酚酞的Na2CO3溶液中,慢慢滴入BaCl2溶液,溶液的红色逐渐褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
设某元素原子核内的质子数为m,中子数为n,则下述论断正确的是( )
A.不能由此确定该元素的相对原子质量
B.这种元素的相对原子质量为m+n
C.若碳原子质量为wg,此原子的质量为(m+n)wg
D.核内中子的总质量小于质子的总质量
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,同种规格的铝片分别与下列物质混合,化学反应速率最大的是:
A.0.1mol/L的盐酸15mL; B.0.2mol/L的盐酸15mL
C.18mol/L的硫酸溶液15mL; D.0.15mol/L的硫酸溶液8mL
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定的温度下,在固定容积的密闭容器中,能表示反应X(气)+2Y(气)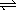 2Z(气)一定达到化学平衡状态的是:
2Z(气)一定达到化学平衡状态的是:
①.容器内压强不随时间改变; ②.C(x)·C2(Y) =C2(z)
③.生成Z的速率与生成Y的速率相等; ④.容器内混合气体的密度不随时间改变
⑤.X、Y、Z的物质的量之比 1∶2∶2
⑥.一定温度下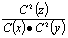 为一常数
为一常数
A.①③⑤ B.①③⑥ C.②④⑥ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.1mol[Ag (NH3)2]OH配合物中含有9NA个σ键
B.标准状况下,22.4L C2H6O中含C-H键5NA
C.1mol冰醋酸和lmol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为NA
D.KClO3+6HCl ===KCl+3Cl2↑+3H2O反应中,生成71g Cl2时,转移的电子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2===LiNH2+LiH,下列有关说法正确的是( )
A.Li2NH中N的化合价是-1
B.该反应中H2既是氧化剂又是还原剂
C.Li+和H-的离子半径相等
D.此法储氢和钢瓶储氢的原理相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com