
【题目】下列图示与对应的叙述相符的是
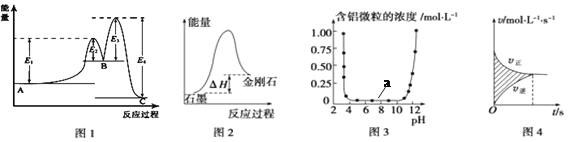
A. 图1所示,A→C反应的ΔH =E1-E2
B. 图2所示,金刚石比石墨稳定
C. 图3表示的是Al3+与OH-反应时含铝微粒浓度变化曲线,图中a区域的物质是Al(OH)3
D. 图4所示,图中阴影部分面积的含义是(υ正-υ逆)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器里,A与B反应生成C,其反应速率分别用vA、vB、vC表示,已知2vB=3vA、3vC=2vB , 则此反应可表示为( )
A.2A+3B=2C
B.A+3B=2C
C.3A+B=2C
D.A+B=C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,0.01mol·L-1r溶液的pH为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是( )

A. 原子半径的大小W <X<Y B. 元素的非金属性Z>X>Y
C. Y的氢化物常温常压下为液态 D. X的最高价氧化物的水化物为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时下列说法正确的是( )
A.在pH=12的溶液中由水提供的c(OH﹣)一定是10﹣12mol?L﹣1
B.将pH=2的酸溶液和pH=12的碱溶液等体积混合后溶液的pH=7
C.将pH=6和pH=4的两种盐酸等体积混合后其c(OH﹣)接近0.5×(10﹣8+10﹣10) mol?L﹣1
D.Na2CO3溶液中:c(Na+)>c(CO ![]() )>c(OH﹣)>c(HCO
)>c(OH﹣)>c(HCO ![]() )>c(H+)
)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关装置图的叙述中正确的是
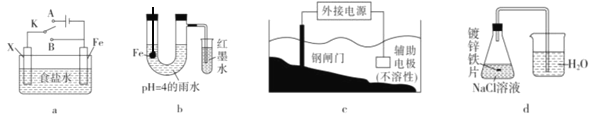
A. 图a中,如果X为锌电极,开关K放到A处或放到B处都能使铁电极受到保护
B. 图b小试管中的导管开始一段时间内液面上升
C. 为保护钢闸门,图c中的钢闸门应与外接电源的正极相连
D. 图d的右侧烧杯中,导管口有气泡冒出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3 (g) +5O2(g)![]() 4NO(g) +6H2O(g), △H=-a kJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是
4NO(g) +6H2O(g), △H=-a kJmol-1,在5L密闭容器投入1molNH3和1mol的O2,2分钟后NO的物质的量增加了0.4mol,下列说法正确的是
A. 2分钟反应放出的热.量值小于0.1akJ
B. 用氧气表示2分钟的反应速率:v(O2)=0.05mol ·L-1 ·min-1
C. 2分钟内NH3的转化率是50%
D. 2分钟末 c(H2O)=0.6mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应: H2S(g)+ ![]() O2(g)═SO2(g)+H2O(g)△H1
O2(g)═SO2(g)+H2O(g)△H1
2H2S(g)+SO2(g)═ ![]() S2(g)+2H2O(g)△H2
S2(g)+2H2O(g)△H2
H2S(g)+ ![]() O2(g)═S(g)+H2O(g)△H3
O2(g)═S(g)+H2O(g)△H3
2S(g)═S2(g)△H4
则△H4的正确表达式为( )
A.△H4= ![]() (△H1+△H2﹣3△H3)
(△H1+△H2﹣3△H3)
B.△H4= ![]() (3△H3﹣△H1﹣△H2)
(3△H3﹣△H1﹣△H2)
C.△H4= ![]() (△H1+△H2﹣3△H3)
(△H1+△H2﹣3△H3)
D.△H4= ![]() (△H1﹣△H2﹣3△H3)
(△H1﹣△H2﹣3△H3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)某学生用0.20molL﹣1的标准NaOH溶液滴定未知浓度的盐酸,其操作为如下几步:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体
③调节液面至“0”或“0”刻度线稍下,并记下读数
④移取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液
⑤用标准液滴定至终点,记下滴定管液面读数.
请回答:
a.以上步骤有错误的是(填编号)
b.步骤⑤中,在记下滴定管液面读数时,滴定管尖嘴有气泡,将导致测定结果(填“偏大”、“偏小”或“无影响”)
c.下图是某次滴定时的滴定管中的液面,其读数为 mL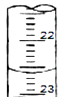
d.根据下列数据:请计算待测盐酸溶液的浓度: mol/L
滴定次数 | 待测体积(ml) | 标准烧碱体积(ml) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 4.00 | 24.00 |
第三次 | 20.00 | 2.00 | 24.10 |
(2)按要求回答下列问题:
a.某温度时,水的离子积常数KW=10﹣13 , 将此温度下pH=11的Ba(OH)2溶液aL与pH=1的H2SO4溶液bL混合,设混合溶液体积为两者之和,所得固体体积忽略不计.若所得混合溶液为中性,则a:b=
b.已知在25℃的水溶液中,AgX、AgY、AgZ均难溶于水,且Ksp(AgX)=1.8×10﹣10 , Ksp(AgY)=1.0×10﹣12 , Ksp(AgZ)=8.7×10﹣17 . 则AgX、AgY、AgZ三者的溶解度(mol/L)S(AgX)、S(AgY)、S(AgZ)的大小顺序为:;若向AgY的饱和溶液中加入少量的AgX固体,则c(Y﹣)(填“增大”“减小”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列转化关系(反应条件略去),A、B、C、D中均含有同一种元素,回答下头问题:
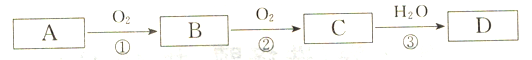
(1)若A为Na,则固体C的颜色为__________________,写出反应③的化学方程式___________________________。
(2)若A为N2,写出反应③的化学方程式___________________________。
(3)若A为S,写出D的浓溶液与Cu在加热情况下反应的化学方程式____________________。
(4)若A为NH3,则__________(填“能”与“不能”)用铁制容器储存D的浓溶液。写出过量Fe与D的稀溶液反应(还原产物只有B)的离子方程式_______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com