
| A. | SO3 | B. | H2O2 | C. | NO2 | D. | Na2O2 |
分析 A.二氧化硫与氧气反应生成三氧化硫;
B.水不能与氧气反应;
C.一氧化氮与氧气反应生成二氧化氮;
D.氧化钠与氧气反应生成过氧化钠.
解答 解:A.二氧化硫与氧气在催化剂加热的条件下反应生成三氧化硫,反应方程式为2SO2+O2$?_{加热}^{催化剂}$2SO3,故A错误;
B.水不能与氧气反应生成过氧化氢,不能实现转化,故B正确;
C.一氧化氮与氧气在常温下反应生成二氧化氮,反应方程式为2NO+O2=2NO2,故C错误;
D.氧化钠与氧气加热生成过氧化钠,反应方程式为2Na2O+O2$\frac{\underline{\;加热\;}}{\;}$2Na2O2,故D错误;
故选B.
点评 本题考查常见氧化物的性质,为高频考点,侧重于学生的分析能力的考查,注意把握常见氧化物的类型和性质,注意相关基础的积累,难度不大.


 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 25℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA | |
| B. | 1mol苯乙烯中含有的碳碳双键数为4NA | |
| C. | 标准状况下,2.24L己烷中原子数为2NA | |
| D. | 通常状况下,18g水所含的中子数为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

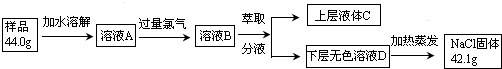

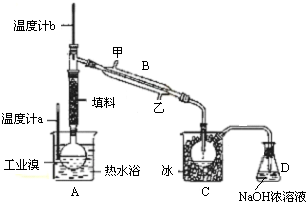
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室做钠的实验时,余下的钠屑投入到废液缸中 | |
| B. | 实验室制硝基苯时,将硝酸与苯混合后再滴加浓硫酸 | |
| C. | 把玻璃管插入橡胶塞孔时,可用厚布护手,紧握用水湿润的玻管,缓慢旋进塞孔中 | |
| D. | 实验室制乙酸丁酯时,须用水浴加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 化学反应方程式 | 反应类型 |
| A | CH3COOH+CH3CH2OH $?_{△}^{浓硫酸}$CH3COOCH2CH3 | 酯化反应 |
| B | CH4+Cl2 $\stackrel{光照}{→}$CH3Cl+HCl | 置换反应 |
| C | CH2=CH2+Br2→CH3CHBr2 | 加成反应 |
| D | 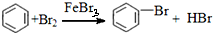 | 取代反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| B. | 向氟化钠溶液中加入适量氢氟酸,得到的酸性混合溶液:c(Na+)>c(F-)>c(H+)>c(OH-) | |
| C. | 25℃时,等体积pH=3的HA和HB两种酸分别与足量的锌反应,相同时间内HA与Zn反应生成的氢气更多,HA是弱酸 | |
| D. | Na2CO3溶液中加入少量Ca(OH)2固体,CO32-水解程度减小,溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
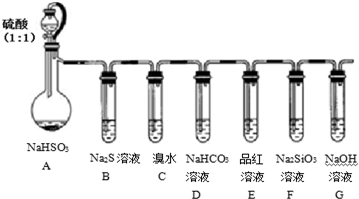
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com