
| A、8:1 | B、4:1 |
| C、2:1 | D、1:1 |
科目:高中化学 来源: 题型:
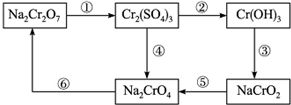
查看答案和解析>>
科目:高中化学 来源: 题型:
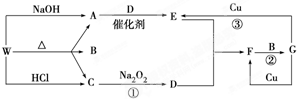
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Kw |
| B、c(H+)/Ka |
| C、c(HA)/c(A-) |
| D、c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等物质的量浓度的各溶液pH关系为:pH(CH3COONa)>pH(Na2S)>pH(NaCN) |
| B、a mol/LHCN溶液与b mol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定大于b |
| C、NaHS和Na2S的混合溶液中,一定存在c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-) |
| D、某浓度的NaCN溶液的pH=d,则其中由水电离出的c(H+)=10-dmol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
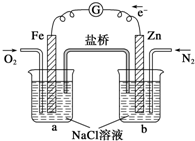
| A、烧杯a中的溶液pH降低 |
| B、烧杯b中发生氧化反应 |
| C、烧杯a中发生的反应为2H++2e-═H2 |
| D、烧杯b中发生的反应为2Cl--2e-═Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)氢气是一种新型的绿色能源,又是一种重要的化工原料.氢气燃烧热值高.实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出 142.9kJ 热量.则能表示H2标准燃烧热的热化学方程式为
(1)氢气是一种新型的绿色能源,又是一种重要的化工原料.氢气燃烧热值高.实验测得,在常温常压下,1gH2完全燃烧生成液态水,放出 142.9kJ 热量.则能表示H2标准燃烧热的热化学方程式为查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用带火星的木条鉴别空气和氧气 |
| B、用可见光束照射以区别溶液和胶体 |
| C、用熟石灰粉末与之混合、研磨,鉴别硫酸铵和氯化铵两种化肥 |
| D、用燃烧的方法鉴别羊毛和合成纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com