



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�� | �����Ϣ |
| X | X������������Ӧ��ˮ���ﻯѧʽΪH2XO3 |
| Y | Y�ǵؿ��к�����ߵ�Ԫ�� |
| Z | Z�Ļ�̬ԭ�����������Ų�ʽΪ3s23p1 |
| W | W��һ�ֺ��ص�������Ϊ28��������Ϊ14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
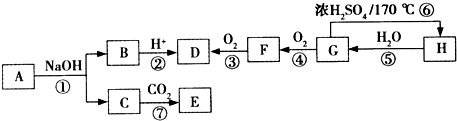
| ʵ�鲽�� | Ԥ���������� |
| ����1��ȡ����������Ʒ������������ˮ�� | ������ȫ�ܽ����ɫ������Һ |
| ����2�� | |
| ����3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
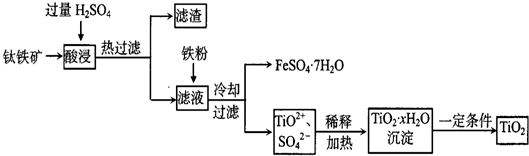
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ�еμ�FeCl3��ϡ��Һ�����Ʊ�Fe��OH��3���� |
| B��������ζ��������ƣ��÷�̪��ָʾ��������ƿ����Һ����ɫ��ɺ�ɫʱ���ﵽ�ζ��յ� |
| C�������£���pH��ֽ�ⶨŨ��Ϊ0.1 mol?L-1 NaClO��Һ��0.1 mol?L-1 CH3COONa��Һ��pH���Ƚ�HClO��CH3COOH������ǿ�� |
| D�������£���Mg��OH��2�м��뱥���Ȼ����Һ��ʹMg��OH��2�ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
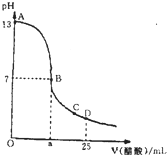 �����£���25mL 0.1mol/L NaOH��Һ����μ���0.2mol/L CH3COOH��Һ��������ͼ������������Һ���ʱ������仯���й�����Ũ�ȱȽϻ�˵����ȷ���ǣ�������
�����£���25mL 0.1mol/L NaOH��Һ����μ���0.2mol/L CH3COOH��Һ��������ͼ������������Һ���ʱ������仯���й�����Ũ�ȱȽϻ�˵����ȷ���ǣ�������| A����A��B����һ�㣬��Һ��һ������c��Na+��+c��H+��=c��CH3COO-��+c��OH-�� |
| B����B��ʱ��a=12.5 |
| C����C�㣺c��CH3COO-����c��Na+����c��H+����c��OH-�� |
| D����D�㣺c��CH3COO-��=c��CH3COOH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CH4 |
| B��CH3CH3 |
| C��C2H2 |
| D��C3H8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��8��1 | B��4��1 |
| C��2��1 | D��1��1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com