
����Ŀ��ijѧ��̽��С�齫һ�������ĵ�����·������õ���71%Cu��20%Al��5%Fe������Au��Pt�Ƚ����Ļ�������Ƴ������Ʊ�����ͭ�����·�ߣ�

��֪��Cu+4HNO3(Ũ)=Cu(NO3)2+2H2O+2NO2��
�ش��������⣺
��1������1����Ҫ�ɷ�Ϊ___��
��2���ڢڲ�����H2O2Ŀ���ǽ�Fe2+������Fe3+�������ӷ���ʽΪ___��ʹ��H2O2��Ϊ���������ŵ���___��
��3���õڢ۲�����CuSO4��5H2O��������Ʊ���ˮCuSO4��������Ҫ����___��
��4��������2��ȡAl2(SO4)3��18H2O��̽��С����������ַ�����

�������ַ����У����з�����___�����в����з�����ԭ����___��
���𰸡�Pt��Au H2O2 +2Fe2+ +2H+ =2Fe3+ +2H2O �������������Ҳ�������Ⱦ ������ �� ��
��������
��1��.����1�ɷ�ӦΪPt��Au�������ȶ�����Ũ�����ϡ���ᷴӦ��
��2��.H2O2��Fe2+������Fe3+��ͬʱ�䱻��ԭΪH2O����������Ⱦ�������������
��3��.�����ᾧ���̻��õ���Ҫ�������������ڴ��ʡ�
��4��.��Һ1��H2O2��Ϊ�˽���Һ��Fe2+��Fe3+��Ȼ��ͨ����NaOH��PHֵʹAl3+��Fe3+��������������ʹ��Һ2ֻ��Cu2+��������2�ɷ�ΪFe(OH)3��Al(OH)3,��������ȡAl2(SO4)3��18H2OʱҪ���dz�ȥFe3+Ӱ�졣
��1��.Pt��Au�����ڻ�ѧ�����ȶ��Ľ�������������1��Pt��Au����ΪPt��Au��
��2��.���ݷ�����H2O2����Fe2+�����ӷ���ʽΪH2O2 +2Fe2++2H+=2Fe3+ +2H2O����Ӧ����ֻ��H2O��Fe3+��û������������������Ⱦ����ΪH2O2 +2Fe2+ +2H+ =2Fe3+ +2H2O���������������Ҳ�������Ⱦ��
��3��.�ɷ�����֪Ϊ������Ϊ������
��4��.���ݷ���������2������ü�����������ȥFe3+�����ջ�ò���Ậ������Fe2(SO4)3�ɷ֡���������ҷ�����������Al�ۿ����û���Feͬʱ��Al3+������������NaOH�ܽ�Al(OH)3Ȼ����ˣ����ų�Fe3+Ӱ�죬���Աȷ�������ԭ�������ʲ��ߡ��ʴ�Ϊ�ң��ס�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2.56gͭ�ۼ���100mL0.4mol��L-1��ϡHNO3��Һ�У����ȳ�ַ�Ӧ���ټ���100mL0.2mol��L-1��H2SO4��Һ���������ȣ�����ַ�Ӧ��������Һ��Cu2+�����ʵ���Ũ����(������Һ����仯)�� ��
A.0.15mol��L-1B.0.2mol��L-1C.0.075mol��L-1D.0.45mol��L-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����³�ѹ�£�����֧��ͬ���Թ��У��ֱ�װ������ʵ�����ϵ��������塣����������������£�
�Թܱ�� | 1 | 2 | 3 | 4 |
���������� | Cl2��SO2 | NO2��O2 | NO��O2 | NH3��N2 |
����֧�Թ�Ѹ��ͬʱ������ˮ���У���Һ���ȶ���ˮ�������߶��ɴ�С��ȷ���ǣ� ��
A.1��2��3��4B.3��1��4��2
C.4��2��3��1D.1��3��2��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��FeS��CuS���ܶȻ������ֱ�Ϊ6.3��10��18 mol2��L��2��1.3��10��36 mol2��L��2������˵���У���������( )
A.25��ʱ��FeS���ܽ�ȴ���CuS���ܽ��
B.��ӦCuSO4��H2S��CuS����H2SO4���ܷ���
C.����FeS����������ȥ��ˮ�е�Cu2��
D.25��ʱ������CuS��Һ�У�Cu2����Ũ��Ϊ![]() ��10��18 mol��L��1
��10��18 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������1.92gͭͶ��һ������Ũ�����У�ͭ��ȫ�ܽ⣬���ɵ�������ɫԽ��Խdz�����ռ�����״���µ�����672mL����ʢ�и����������������ˮ�У�ͨ���״����һ�������������ǡ��ʹ������ȫ����ˮ�У���ͨ������������ǣ�������
A. 168mL B. 224mL C. 504mL D. 336mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������������ǻ�����������Ҫ���̣����ֳ����������¡��ش�������⣺
����I���������������������е�SO2����֪���չ����к���������ʵ�����������ҺpH�ı仯��ϵ��ͼ��ʾ��
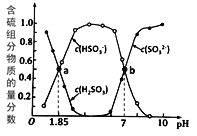
(1)��ѡ�� (NH4)2SO3��Ϊ����Һ(��֪NH3��H2O �ĵ��볣��Kb=1.74��10-5)��
��H2SO3��pKa1=________( pKa1 = -lgKa1)��
��(NH4)2SO3��Һ��________(������������������������������)��������________________��
��ͼ��b����Һ��n(HSO3- ) : n(NH4+) =_________��
(2)��ѡ��0.1mol/L ��Na2SO3��Ϊ����Һ�����չ����У������й�����Ũ�ȹ�ϵһ����ȷ����(������Һ����ı仯)_________��
A.Na2SO3��Һ�д��ڣ�c(Na+)>c(SO32-)>c(H2SO3)>c(HSO3-)
B.NaHSO3��Һ�д��ڣ�c(Na+)>c(HSO3-)>c(SO32-)>c(H2SO3)
C.������Һ������ʱ��2c(SO32-)+c(HSO3-)=0.2mol/L
D.������Һ������ʱ��c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3)
����II���ú�����ˮ���������е�SO2������ԭ����ͼ��ʾ��
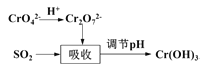
(3)���������з�Ӧ�����ӷ���ʽΪ____________________
(4)��ʹ��ˮ�еĸ�Ԫ����ȫת��ΪCr(OH)3������Ӧ����pH�ķ�ΧΪ____��(������Ksp[Cr(OH)3]=1.0��10-32)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeBr2��һ�ֻ���ɫ���壬ijѧϰС���Ʊ���̽�����Ļ�ԭ�ԡ�
I.�Ʊ�FeBr2����
ʵ��������ͼ��ʾװ����ȡ�廯����������AΪCO2����װ�ã�D��d�о�ʢ��Һ�壬EΪ����¯˿�IJ���ֹܣ�e���������µĴ�������ʢ��ϸ���ۡ�
ʵ�鿪ʼʱ���Ƚ����������CO2����ͨ��D�У��ٽ����ۼ�����600-700�棬E�������ۿ�ʼ��Ӧ�����Ͻ�d��Һ������¶�Ϊ100-120���D�У�����һ��ʱ���������Ӧ���ڲ���ֹ��ڲ�������ɫ��Ƭ״�廯������
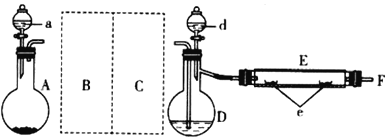
��1������A��ʢ����CaCO3��a��ʢ��6mol/L�����ᡣΪʹ����D�е�CO2Ϊ���﴿�������壬ͼ��C����ϴ��ƿ��װ��Ũ���ᣬ��B��Ϊ___��������Eװ���е�CO2δ�������ܷ����ĸ���Ӧ�Ļ�ѧ����ʽΪ___��
��2��E���еķ�Ӧ��ʼǰͨ��CO2����Ҫ������___��E���еķ�Ӧ��ʼ�����ͨ��CO2����Ҫ������___��
II.̽��FeBr2�Ļ�ԭ��
��3����ʵ����Ҫ90mL0.2mol/LFeBr2��Һ��ȡ������Ӧ�Ƶõ�FeBr2�������Ƹ���Һ�������������ձ�����Ͳ������������ͷ�ι��⣬����Ҫ�IJ���������___��
��4����֪��Cl2��CCl4��Һ�ʻ���ɫ��Br2��CCl4��Һ�ʳȺ�ɫ��Cl2��������Br-��Ҳ������Fe2+��ȡ10mL����FeBr2��Һ�������еμӼ������Ƶ���ˮ������Һ�ʻ�ɫ��ȡ������Ӧ�����Һ����KSCN��Һ����Һ��ΪѪ��ɫ����ȡ������Ӧ�����Һ����CCl4�����²�Ϊ��ɫҺ�塣����ʵ����۱�����ԭ�ԣ�Fe2+___Br-(����>������<��)��
��5������30mL���裨3����FeBr2��Һ��ͨ���״����179.2mL��Cl2��ȡ������Ӧ�����Һ����CCl4�����²�Һ���___ɫ��д���÷�Ӧ�����ӷ���ʽ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CaCO3��CaO��Ca��OH)2��NaOH�ĸ�����Ӧ�У�������Ӧ���Ͳ������� ��
A.���Ϸ�ӦB.�ֽⷴӦC.�û���ӦD.���ֽⷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Т�BaCl2���� �ڽ��ʯ ��NaOH���� �ܹ�������������ʣ�������Ҫ����գ�
��1���ۻ�ʱ����Ҫ�ƻ���ѧ������____���������գ���ͬ����ֻ�����Ӽ�����____�����ڹ��ۻ��������____���۵���ߵ���____��
��2��д��NaOH�ĵ���ʽ____������Ŀռ乹��____��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com