
【题目】金属铜是人们最早使用的金属之一,下列关于铜电极的叙述不正确的是( )
A.铜锌原电池中铜是正极
B.用电解法精炼粗铜时粗铜做阳极
C.在镀件上镀铜时可用金属铜做阳极
D.电解水制H2、O2时铜做阳极
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A (g)+xB(g)2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的如图所示.下列说法中正确是( ) 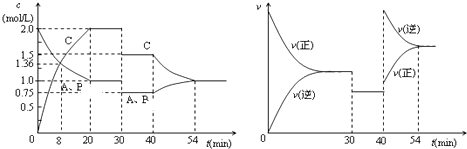
A.8min前A的平均反应速率为0.08mol/(Ls)
B.30min时扩大容器的体积,40min时升高温度
C.反应方程式中的x=1,正反应为吸热反应
D.30min和54min的反应的平衡常数相等4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是
A. 氯气溶于水中:Cl2+H2O![]() H++Cl-+HC1O
H++Cl-+HC1O
B. 碳酸钙溶解于盐酸中 :CO32-+2H+=CO2↑ +H2O
C. 用苛性钠溶液吸收过量SO2:SO2+2OHˉ=SO32-+H2O
D. 硫酸与氢氧化钡溶液混合 :H++SO42-+Ba2++OHˉ =BaSO4↓ +H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是当今世界最重要的化工产品之一。
I.硫酸的各种制法。
(1)早在1000多年前,我国就已采用加热胆矾(CuSO4· 5H2O)或绿矾(FeSO4·7H2O)的方法制取硫酸。FeSO4受热分解的化学方程式:2 FeSO4![]() Fe2O3+SO2↑ +SO3↑。
Fe2O3+SO2↑ +SO3↑。
① 将FeSO4受热产生的气体通入如下图装置中,以检验产生的气体中是否含有SO3和SO2。 能说明SO2存在的实验现象是_________。

② 有同学提出虚线框内盛装NaOH溶液的装置可以换成上图右边的a装置,其中多孔玻璃球泡的作用是__________。
(2)目前工业上主要采用接触法制备硫酸,其中一步为:2SO2+O2![]() 2SO3。实验室模拟该过程常用下图装置进行实验。b装置中装有浓硫酸,写出b装置的作用__________(写出两点)。
2SO3。实验室模拟该过程常用下图装置进行实验。b装置中装有浓硫酸,写出b装置的作用__________(写出两点)。
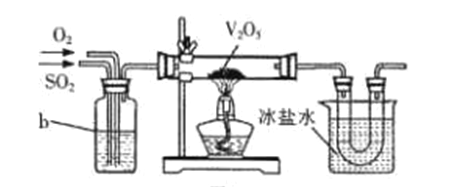
Ⅱ.硫酸的性质。
(3)下图中甲试管内发生反应的化学方程式_________ ,该反应体现了浓硫酸的性质为______。
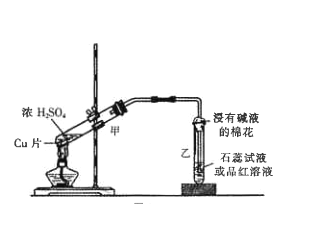
(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到白色固体,请写出检验白色固体的方法______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式正确的是( )
A.氨气通入醋酸溶液:CH3COOH+NH3=CH3COONH4
B.澄清的石灰水与盐酸反应:H++OH-=H2O
C.碳酸钡加入稀硫酸:BaCO3+2H+=Ba2++H2O+CO2↑
D.碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.6 mol Ba(OH)2中,含有OH-的数目是 ( )
A.约为1.2B.约为7.22×1023
C.约为6.02×1023D.约为3.01×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)═Mg2+(aq)+2OH﹣(aq)时,为使Mg(OH)2固体的量减少,可加入少量的( )
A.NaOH
B.NH4Cl
C.MgSO4
D.NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氯水的叙述中,正确的是
A.新制氯水中有3种分子,有4种离子
B.新制氯水在光照的条件下,可以产生气体,该气体是氯气
C.向新制氯水中滴加硝酸银溶液,没有任何现象
D.新制氯水不可以使干燥的有色布条褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com