
����Ŀ��ԭ����ȩ��һ��ҽҩ�м��壬һ�ֺϳ�·����ͼ��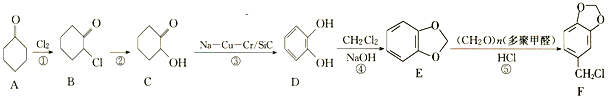
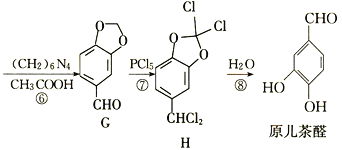
�ش��������⣺
(1)A�еĹ�����������________��
(2)̼ԭ��������4����ͬ��ԭ�ӻ����ʱ����̼��Ϊ����̼��B��____(������������û����)����̼��
(3)��Ӧ�ٵ�������__________����Ӧ�������Լ��������ֱ�Ϊ________��
(4)ԭ����ȩ�ķ���ʽΪ________��
(5)W��C��Ϊͬ���칹�壬W�в�����״�ṹ���ܷ���ˮ�ⷴӦ���˴Ź�������ֻ��3����ҷ����֮��Ϊ6��3��1��W�Ľṹ��ʽΪ_________(ֻдһ��)��
(6)����Ա��Ӻ�(CH2O)nΪԭ���Ʊ�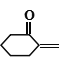 �ĺϳ�·��_______��(���Լ���ѡ)����֪�������ڶ�ۼ�ȩ���Ȼ��������£�����λ����ȡ����Ӧ��
�ĺϳ�·��_______��(���Լ���ѡ)����֪�������ڶ�ۼ�ȩ���Ȼ��������£�����λ����ȡ����Ӧ��
���𰸡��ʻ� �� ȡ����Ӧ NaOH/H2O���� C7H6O3 (CH3)2C=CHCOOCH3��CH3COOCH=C(CH3)2��![]()

![]()
![]()
![]()
![]()
![]()
![]()
![]()
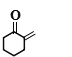
��������
(1)���ݳ��������ŵĽṹ�������
(2)��������̼�ĸ�����B(![]() )�����жϣ�
)�����жϣ�
(3)��Ӧ�����ʻ���λ����ԭ�ӱ���ԭ��ȡ������������ͼ����Ӧ��Ϊ±��ԭ�ӵ�ˮ�ⷴӦ���ݴ˷������
(4)����ԭ����ȩ(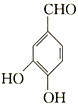 )�жϷ���ʽ��
)�жϷ���ʽ��
(5) W��C��Ϊͬ���칹�壬CΪ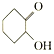 ��W�в�����״�ṹ���ܷ���ˮ�ⷴӦ����Ŀ�ṹ�к����������˴Ź�������ֻ��3����ҷ����֮��Ϊ6��3��1����W��Ӧ��3�����������������Ļ�ѧ������ͬ���ݴ���дW�Ľṹ��ʽ��
��W�в�����״�ṹ���ܷ���ˮ�ⷴӦ����Ŀ�ṹ�к����������˴Ź�������ֻ��3����ҷ����֮��Ϊ6��3��1����W��Ӧ��3�����������������Ļ�ѧ������ͬ���ݴ���дW�Ľṹ��ʽ��
(6)�Ա��Ӻ�(CH2O)nΪԭ���Ʊ�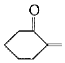 ��Ŀ������뱽�ӱȽϣ�������һ��̼ԭ�ӣ����ԭ�ϣ����������з�Ӧ�ݵ���Ϣ�Ⱥϳ�
��Ŀ������뱽�ӱȽϣ�������һ��̼ԭ�ӣ����ԭ�ϣ����������з�Ӧ�ݵ���Ϣ�Ⱥϳ�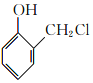 ������H2�뱽�������ӳɷ�Ӧ(�α��ϱ��ƻ�����ķ�Ӧ)��Ȼ�������ǻ����ʻ���������±��������ȥ��Ӧ��
������H2�뱽�������ӳɷ�Ӧ(�α��ϱ��ƻ�����ķ�Ӧ)��Ȼ�������ǻ����ʻ���������±��������ȥ��Ӧ��
(1)A(![]() )�еĹ�����Ϊ�ʻ����ʴ�Ϊ���ʻ���
)�еĹ�����Ϊ�ʻ����ʴ�Ϊ���ʻ���
(2)B(![]() )�к���1������̼�����Ǻ�(*)���B�е�����̼��
)�к���1������̼�����Ǻ�(*)���B�е�����̼��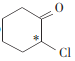 ���ʴ�Ϊ���У�
���ʴ�Ϊ���У�
(3)��Ӧ�����ʻ���λ����ԭ�ӱ���ԭ��ȡ��������ȡ����Ӧ����������ͼ����Ӧ��Ϊ�ڼ��ȵ������£���ԭ����NaOHˮ��Һ�з���ˮ�����ɴ����ʴ�Ϊ��ȡ����Ӧ��NaOH/H2O������
(4)ԭ����ȩ( )�ķ���ʽΪC7H6O3���ʴ�Ϊ��C7H6O3��
)�ķ���ʽΪC7H6O3���ʴ�Ϊ��C7H6O3��
(5) W��C��Ϊͬ���칹�壬CΪ ��W�в�����״�ṹ���ܷ���ˮ�ⷴӦ����Ŀ�ṹ�к����������˴Ź�������ֻ��3����ҷ����֮��Ϊ6��3��1����W��Ӧ��3�����������������Ļ�ѧ������ͬ���ʷ��������W��(CH3)2C�TCHCOOCH3��CH3COOCH�TC(CH3)2��
��W�в�����״�ṹ���ܷ���ˮ�ⷴӦ����Ŀ�ṹ�к����������˴Ź�������ֻ��3����ҷ����֮��Ϊ6��3��1����W��Ӧ��3�����������������Ļ�ѧ������ͬ���ʷ��������W��(CH3)2C�TCHCOOCH3��CH3COOCH�TC(CH3)2��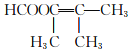 ���ʴ�Ϊ��(CH3)2C�TCHCOOCH3��CH3COOCH�TC(CH3)2��
���ʴ�Ϊ��(CH3)2C�TCHCOOCH3��CH3COOCH�TC(CH3)2��![]() ��
��
(6)Ŀ������뱽�ӱȽϣ�������һ��̼ԭ�ӣ����ԭ�ϣ����������з�Ӧ�ݵ���Ϣ�Ⱥϳ� ������H2�뱽�������ӳɷ�Ӧ(�α��ϱ��ƻ�����ķ�Ӧ)��Ȼ�������ǻ����ʻ���������±��������ȥ��Ӧ����ϳ�·��Ϊ��
������H2�뱽�������ӳɷ�Ӧ(�α��ϱ��ƻ�����ķ�Ӧ)��Ȼ�������ǻ����ʻ���������±��������ȥ��Ӧ����ϳ�·��Ϊ��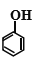
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ���ʴ�Ϊ��
���ʴ�Ϊ��
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ͬ��ͬѹ�£�H2(g)��Cl2(g)��2HCl(g)���ڹ��պ͵�ȼ�����µġ�H(��ѧ��������ͬ)�ֱ�Ϊ��H1����H2����H1_____��H2(����>����<��������������ͬ)��
(2)��ͬ�����£�1 mol P4�����е�����_______4 mol Pԭ�������е�������
(3)��֪P4(���ף�s)![]() 4P(���ף�s) ��H����17 kJ�� mol��1���Ƚ����з�Ӧ�С�H�Ĵ�С����H1_____��H2��
4P(���ף�s) ��H����17 kJ�� mol��1���Ƚ����з�Ӧ�С�H�Ĵ�С����H1_____��H2��
��P4(���ף�s)��5O2(g)��P4O10(s) ��H1��
��4P(���ף�s)��5O2(g)��P4O10(s) ��H2��
(4)��֪��ϡ��Һ�У�H��(aq)��OH��(aq)��H2O(l) ��H����57.3 kJ�� mol��1����Ũ������ϡ����������Һ��Ӧ����2 molˮ���ų�������______114.6kJ��
(5)��֪��28gFe(s)��CO2(g)��һ�������£���ȫ��Ӧ����FeO(s)��CO(g)��������a kJ�������÷�Ӧ���Ȼ�ѧ����ʽ��___________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ƵĹ�ҵ��ˮ������ NH4NO3�����õ�ⷨ�������乤��ԭ����ͼ�� ʾ����Ĥ����Ĥ�ֱ�ֻ���������Ӻ�������ͨ�����������й�˵����ȷ�ģ���
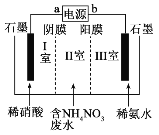
A.a ��Ϊ��Դ������b ��Ϊ��Դ����
B.װ�ù���ʱ������ b �������������ߡ����� ���� a ��
C.I �Һ� III �����վ��ܵõ�����Ʒ NH4NO3
D.�����缫��ӦʽΪ 2NO3-+12H++10e-==N2��+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����(N2H4)����ȼ�ϵ�ص�ԭ��ʾ��ͼ��ͼ��ʾ������ܷ�ӦΪ��N2H4+O2=N2+2H2O������˵���������

A.�缫b������ԭ��Ӧ
B.�����ɵ缫a�������õ�������缫b
C.����Y��NaOH��Һ
D.�缫a�ĵ缫��ӦʽΪN2H4 + 4OH����4e��=N2�� + 4H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ͷ��ƾƾ��Ĺ��̿ɴ��Ա�ʾ���£�
�٣�C6H10O5��n+nH2O![]() nC6H12O6 ��C6H12O6
nC6H12O6 ��C6H12O6![]() 2C2H5OH+2CO2��
2C2H5OH+2CO2��
��1��������ѧ����ʽ����C6H10O5��n���ܱ�ʾ_____ ____����������������
��2��C6H12O6������_________������_____ ____�Լ��������������
��3��Ϊ����ƻ����������з����˷�Ӧ�٣�������ƻ��֭�еμӵ�ƣ���Һ��_________ɫ������ƻ��֭�м���Cu��OH��2����Һ�����ȣ���Ӧ����____ ____����ʵ������
��4���������ò�����ˮ�ⷴӦ����_________
A������ͷʱ���������ζ
B��������Һ��ϡ���Ṳ��һ��ʱ��μӵ�ˮ������ɫ
C��������Ũ����մ��Ƥ���ϻ���ֻ�ɫ�ߺ�
D����֬������������Һ���������Ƶ÷���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��FeCl2���ж��е���ɫ������������ӡȾ����ֽ��ҵ����ˮ������FeCl3�ڼ�����������ˮ����ˮ�⡣FeCl3��FeCl2��������C6H5Cl��C6H4Cl2�������ش��������⣺
(1)��FeCl36H2O�Ƶø���FeCl2�Ĺ������£�
i.��ʢ��FeCl36H2O�������м������SOCl2(Һ�壬��ˮ��)�����ȣ������ˮFeCl3��
ii.����ˮFeCl3���ڷ�Ӧ���У�ͨ��һ��ʱ�����������ȣ�����FeCl2��
��FeCl36H2O�м���SOCl2�����ˮFeCl3�Ļ�ѧ����ʽΪ________��(��֪�÷�ӦΪ��������ԭ��Ӧ)
�� ii��ͨ��һ��ʱ����������ټ��ȵ�Ŀ����__________��
(2)���÷�Ӧ2FeCl3 + C6H5Cl![]() 2FeCl2+ C6H4Cl2 +HCl������ȡ��ˮFeCl2����������ƿ�м�����ˮ�Ȼ����������ȱ������Ʒ�Ӧ�¶���һ����Χ�ڼ���3 h����ȴ�����롢�ᴿ�õ��ֲ�Ʒ��ʵ��װ����ͼ��(����װ����ȥ)
2FeCl2+ C6H4Cl2 +HCl������ȡ��ˮFeCl2����������ƿ�м�����ˮ�Ȼ����������ȱ������Ʒ�Ӧ�¶���һ����Χ�ڼ���3 h����ȴ�����롢�ᴿ�õ��ֲ�Ʒ��ʵ��װ����ͼ��(����װ����ȥ)

������B�������� _____����Ӧǰ����A��ͨ��N2��Ŀ����________��
�ڷ�Ӧ��������ȴʵ��װ��A����������ƿ�����ʵ�������____��____������õ�FeCl2�ֲ�Ʒ��
�۸�װ�ô��ڵIJ���֮����__________��
(3)FeCl2�Ĵ��Ȳⶨ��
��ȡa g��Ʒ���Ƴ�100 mL��Һ��������Һ����ȡ������Һ5.00mL������500 mL��ƿ�ڲ���ˮ200mL������������ƿ�м�����������Һ20.00 mL����0.1 molL-1����KMnO4����Һ�ζ����յ�ʱ��������KMnO4����ҺV mL���ζ����յ���ж�������______________����������Һ����(FeCl2)=kV(VΪ���ĵ����Ը�����ر���Һ�ĺ�����)g��L-1��k=____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧ����պī֭��д���ֽ���������缫��ͼ1������Ʋ���װ��һ�����͡����۵��Ŀɳ��﮿�����أ��乤��ԭ����ͼ2��ʾ�������й�˵����ȷ����

A.�պϿ���K��﮵�س�磬XΪֱ����Դ����
B.�ŵ�ʱ��ֽ���е���ά����﮵�ص�����
C.�ŵ�ʱ��Li+����������Һ���л����������
D.���ʱ�������ĵ缫��ӦʽΪLi2O2+2e -=O2��+2Li+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ��Ӧԭ���ڿ��к��������й㷺Ӧ�á�
��1�����������Ƚ�������Ҫ�ɷ�Ϊ CO��CH4��H2����SO2��һ�������»�ԭΪ����������� ��������֪����C��s��+O2��g��=CO2��g����H1= -393.5 kJ��mol-1
��CO2��g��+C��s��=2CO��g�� ��H2= + 172.5 kJ��mol-1
��S��s��+O2��g��=SO2��g�� ��H3= -296.0kJ��mol-1
CO��SO2��ԭΪ��������Ȼ�ѧ����ʽΪ_______��
��2��CO�����ںϳɼ״���һ���¶��£������Ϊ2L���ܱ������м���CO��H2������ ��ӦCO��g��+2H2��g��![]() CH3OH��g�����ﵽƽ����ø���ֵ�Ũ�����£�
CH3OH��g�����ﵽƽ����ø���ֵ�Ũ�����£�
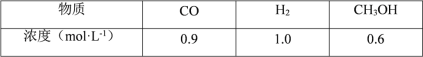
�ٷ�Ӧ�ﵽƽ��ʱ��CO��ת����Ϊ_______��
�ڸ÷�Ӧ��ƽ�ⳣ��ֵ K=_______��
�ۺ��º��������£�����˵����Ӧ�Ѵﵽƽ��״̬����_______�����ţ���
A v ����CO��=2v ����H2�� B ���������ܶȲ���
C ��������ƽ����Է����������� D CH3OH��CO��H2 ��Ũ�ȶ����ٷ����仯
������������������䣬�ٳ��� 0.6mol CO �� 0.4mol CH3OH����ʱv��_______v�������� >�� ��< ������= ������
��3���ڳ����£�������HNO2�ĵ��볣�� Ka=7.1��10-4mol��L-1��NH3��H2O�ĵ��볣�� Kb=1.7��10-5mol��L-1��0.1mol��L-1 NH4NO2��Һ������Ũ���ɴ�С��˳����__________��������NO2-ˮ�ⷴӦ��ƽ�ⳣ��Kh=_______��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴Ӧ2SO2+ O2![]() 2SO3�ﵽƽ��ı�־��
2SO3�ﵽƽ��ı�־��
������2 mol SO2��ͬʱ����2 mol SO3
�� SO2��O2��SO3�����ʵ���֮��Ϊ2��1��2
����Ӧ������У�SO3�������������ٸı�
A.�٢�B.�٢�C.ֻ����D.ֻ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com