
【题目】室温下,下列说法正确的是![]()
A.![]() 的
的![]() 溶液或醋酸中,由水电离出的
溶液或醋酸中,由水电离出的![]() 均为
均为![]()
B.![]() 的醋酸和
的醋酸和![]() 的NaOH溶液等体积混合后,
的NaOH溶液等体积混合后,![]()
C.同体积同pH的氢氧化钠溶液和氨水分别稀释相同倍数,氨水的pH较大
D.![]()
![]() 溶液和
溶液和![]()
![]() 溶液等体积混合,溶液中
溶液等体积混合,溶液中![]()
【答案】C
【解析】
A、pH=5的NH4Cl溶液由水电离出的c(H+)=10-5mol/L;pH=5的醋酸中由水电离出的c(H+)=10-9mol/L,A错误;
B、pH=3的醋酸和pH=11的NaOH溶液等体积混合后醋酸有剩余,溶液显酸性pH值小于7,B错误;
C、氨水属于弱电解质,稀释过程中电离程度增大,所以同体积同pH的氢氧化钠溶液和氨水分别稀释相同倍数,稀释后氨水的pH较大,C正确;
D、0.1mol/L Na2CO3溶液和0.1mol/L NaHSO4液等体积混合,反应生成碳酸氢钠和硫酸钠,电荷守恒式子为:c(Na+)+c(H+)=2c(CO32-)+2c(SO42-)+c(HCO3-)+c(OH-),D错误;
故选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】![]() 的两种一元碱溶液X、Y各
的两种一元碱溶液X、Y各![]() ,分别稀释至
,分别稀释至![]() ,其pH与溶液体积
,其pH与溶液体积![]() 的关系图所示,下列说法不正确的是( )
的关系图所示,下列说法不正确的是( )
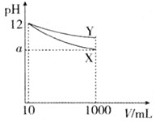
A.若X、Y都是弱碱,则![]()
B.等浓度的X、Y溶液的碱性:![]()
C.稀释至![]() 时两种碱的物质的量浓度:
时两种碱的物质的量浓度:![]()
D.完全中和等体积相同pH的X、Y两溶液时,消耗同浓度盐酸的体积![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化氢一定条件下可发生分解:2H2O2(l)=2H2O(l)+O2(g),其能量变化如下图所示,下列说法正确的是

A.该分解反应为吸热反应
B.2molH2O2具有的能量小于2molH2O和1molO2所具有的总能量
C.加入MnO2或FeCl3均可提高该分解反应的速率
D.其他条件相同时,H2O2溶液的浓度越大,其分解速率越慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝热反应是铝的一个重要性质,该性质用途十分广泛。 “铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。已知:Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
物质 | Al | Al2O3 | Fe | Fe2O3 |
熔点/℃ | 660 | 2 054 | 1 535 | 1 462 |
沸点/℃ | 2 467 | 2 980 | 2 750 | - |
I.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________,反应的离子方程式为______________________________________。
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是________(填序号)。
A、浓硫酸 B、稀硫酸 C、稀硝酸 D、氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入6mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
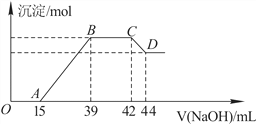
(1)依题意,请写出熔融物中铁与该稀的硝酸反应的离子方程式:____________________
(2)图中OA段没有沉淀生成,此阶段发生反应的离子方程式为__________________。
(3)在BC段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为_____________;
(4)熔融物中铝元素的物质的量为________mol。
(5)B点对应的沉淀的物质的量为______mol,A点对应的氢氧化钠溶液的体积为________mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置制备溴苯,下列说法错误的是( )
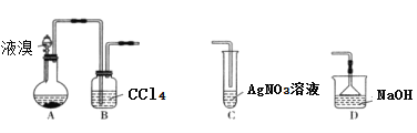
A.装置A中长玻璃导管仅起导气作用,装置B中的实验现象是CCl4由无色变橙色
B.若装置B后连接装置C,装置C中生成淡黄色沉淀,可证明装置A中发生取代反应
C.若装置B后连接装置D,则装置D的作用是吸收尾气
D.向反应后的装置A中加入NaOH溶液,振荡静置,下层为无色油状液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学对电化学原理进行了一系列探究活动。
(1)如图为某实验小组依据氧化还原反应_______________(用离子方程式表示)设计的原电池装置,反应前,电极质量相等,一段时间后,两电极质量相差 12 g,导线中通过__________mol 电子。
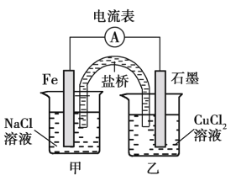
(2)其他条件不变,若将 CuCl2溶液换为 NH4Cl 溶液,石墨电极发生的电极反应为___________,这是由于 NH4Cl 溶液显_______________(填“酸性”、“碱性” 或“中性”)。用吸管吸出铁片附近的溶液少许置于试管中,向其中滴加少量新制饱和氯水,然后滴加几滴 KSCN 溶液,溶液变红,继续滴加过量新制饱和氯水,溶液颜色褪去,同学们对此做了多种假设,某同学的假设:“溶液中的+3 价铁被氧化为更高价态。” 如果+3 价铁被氧化为 FeO42-,写出发生反应的离子方程式___________________。
(3)其他条件不变,若将盐桥换成弯铜导线与石墨连成的形装置如图所示,一段时间后,在甲装置铜丝附近滴加酚酞溶液,现象是____________,电极反应为__________;乙装置中石墨(Ⅰ)为__________(填“正”、 “ 负” 、 “ 阴”或“阳”)极。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知HNO2在低温下较稳定,既有氧化性又有还原性,其氧化产物、还原产物与溶液pH的关系如下表,且酸性:![]() 。下列有关说法错误的是
。下列有关说法错误的是![]()
![]()
pH范围 |
|
|
产物 |
| NO、 |
A.碱性条件下,NaNO2与NaClO反应的离子方程式为![]()
B.向冷的NaNO2溶液中通入H2S气体,有淡黄色沉淀产生
C.低温时不用其它试剂即可区分HNO2溶液与Na2CO3溶液
D.向冷的NaNO2溶液中通入SO2可得到HNO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向0.1mol·L1二元弱酸H2A的溶液中逐滴加入NaOH溶液,H2A、HA-、A2的物质的量分数随pH的变化如图所示。下列叙述正确的是( )
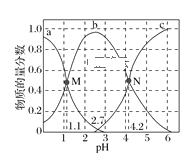
A.a曲线代表HA的物质的量分数随pH的变化
B.M点pH=1.1时,溶液中微粒浓度关系为c(H+)>c(HA)=c(H2A)
C.pH=2.7时,c(A2)+c(HA)+c(H2A)=0.1mol·L1
D.N点pH=4.2时,c(A2)=c(HA),溶液中不存在H2A分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溶液X中可能含有K+、Mg2+、Al3+、AlO、SiO、CO、SO、SO中的若干种离子。某同学对该溶液进行了如下实验:

下列判断正确的是( )
A. 气体甲一定是纯净物 B. 沉淀甲是硅酸和硅酸镁的混合物
C. K+、AlO和SiO一定存在于溶液X中 D. CO和SO一定不存在于溶液X中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com