
| A、若体系恒容,通入H2S(g),则正反应速率增大,逆反应速率减小 |
| B、升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C、增大压强,平衡向逆反应方向移动,将引起体系温度降低 |
| D、若体系恒容,注入一些H2后达新平衡,H2浓度将减小 |


科目:高中化学 来源: 题型:
| A、电解过程中阴极没有气体生成 |
| B、电解过程中转移的电子的物质的量为0.4 mol |
| C、原CuSO4溶液的浓度为0.1 mol?L-1 |
| D、电解过程中阳极收集到的气体体积为1.12 L(标况下) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化钠可用食物调整碱性的添加剂 |
| B、棉、麻完全燃烧可以生成CO2和H2O |
| C、脂肪在一定条件下都能发生水解反应 |
| D、汽油、柴油、煤油的主要成分都是碳氢化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
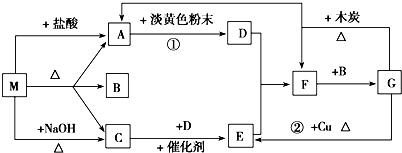
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、C气体的体积分数增大 |
| B、m+n>p |
| C、气体A的转化率升高 |
| D、平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、熵变小于零而焓变大于零的反应肯定不能发生 |
| B、用蒸馏水稀释0.1mol/L的醋酸至0.01mol/L,稀释过程中温度维持25℃不变,溶液中各离子浓度均减小 |
| C、已知2H2(g)+O2(g)=2H2O(g)△H=-483.6 kJ/mol,则H2燃烧热为241.8 kJ/mol |
| D、已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2;则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、有机玻璃(制不粘锅) |
| B、SiO2(制光纤) |
| C、钢化玻璃(火车窗玻璃) |
| D、氮化硅陶瓷(制导热剂) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com