
【题目】甲醇是重要的化工原料,在有机合成中具有广泛应用。
I.(1)用甲醇制取甲胺的反应为![]() △H
△H
已知该反应中相关化学键的键能数据如下:
共价键 | C―O | H―O | N―H | C―N |
键能/kJ·mol-1 | 351 | 463 | 393 | 293 |
则该反应的△H=__________kJ·mol-1
Ⅱ.一定条件下,将2mol CO和6mol H2通入2L密闭容器中发生如下反应
主反应:![]() △H<0 Ⅰ
△H<0 Ⅰ
副反应:![]() △H<0 Ⅱ
△H<0 Ⅱ
反应到t min时,达到平衡状态。平衡时CH3OH的体积分数φ(CH3OH)如图所示:
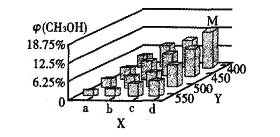
(2)图中a___b(填“大于”或“小于”)。图中Y轴表示温度,其理由是__________
(3)若反应II的平衡常数K值变小.则下列说法中正确的是___________(填序号)。
A.平衡均向正反应方向移动
B.平衡移动的原因是升高了温度
C.达到新平衡后,φ(CH3OH)减小
D.容器中φ(CH3OCH3)增大
(4)平衡时,M点CH3OH的体积分数为12.5%,c(CH3OCH3)=0.1mol·L-1,则此时CO的转化率为________;用H2表示I的反应速率为______mol·L-1·min-1。反应Ⅱ的平衡常数K=___________(用分数表示)
【答案】-12 小于 随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度 BC 56% ![]()
![]()
【解析】
(1)反应热=反应物总键能-生成物总键能;
(2) 根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,结合平衡移动原理回答;
(3) 反应II为放热反应,若反应II的平衡常数K值变小,说明平衡逆向移动,温度升高;
(4)平衡时,c(CH3OCH3)=0.1mol·L-1,则n(CH3OCH3)=0.2mol,根据![]() ,分解的CH3OH为0.4mol,生成的水为0.2mol,根据三段式计算解答。
,分解的CH3OH为0.4mol,生成的水为0.2mol,根据三段式计算解答。
I.(1)设C-H的键能为x,反应CH3OH(g)+NH3(g)═CH3NH2(g)+H2O(g)的△H=反应物总键能-生成物总键能=(3x+351+463+393×3-3x-293-393×2-463×2)kJ/mol=-12kJ/mol,故答案为:-12;
Ⅱ.(2)根据图示信息:X轴上a点的数值比b点小,随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度,故答案为:小于;随着Y值的增加,CH3OH的体积分数φ(CH3OH)减小,平衡逆向移动,故Y表示温度;
(3) 反应II为放热反应,若反应II的平衡常数K值变小,说明平衡逆向移动,温度升高。A.反应II为放热反应,若反应II的平衡常数K值变小,说明平衡逆向移动,故A错误; B.平衡常数只与温度有关,反应II为放热反应,若反应II的平衡常数K值变小,说明平衡逆向移动,故B正确;C.温度升高,CO(g)+2H2(g)CH3OH(g)△H<0,平衡逆向移动,达到新平衡后,φ(CH3OH)减小,故C正确;D.![]() ,平衡逆向移动,导致CO(g)+2H2(g) CH3OH(g) △H<0,平衡逆向移动,容器中气体的总物质的量增大,容器中φ(CH3OCH3)减小,故D错误;故答案为:BC;
,平衡逆向移动,导致CO(g)+2H2(g) CH3OH(g) △H<0,平衡逆向移动,容器中气体的总物质的量增大,容器中φ(CH3OCH3)减小,故D错误;故答案为:BC;
(4)平衡时,c(CH3OCH3)=0.1mol·L-1,则n(CH3OCH3)=0.2mol,根据![]() ,分解的CH3OH为0.4mol,生成的水为0.2mol,设CO的转化量是x。
,分解的CH3OH为0.4mol,生成的水为0.2mol,设CO的转化量是x。
CO(g)+2H2(g)CH3OH(g);
初始量(mol): 2 6 0
变化量(mol): x 2x x
平衡量(mol):2-x 6-2x x-0.4
平衡时,CH3OH的体积分数为12.5%,则![]() ×100%=12.5%,解得x=1.12 mol ,所以CO的转化率为
×100%=12.5%,解得x=1.12 mol ,所以CO的转化率为![]() ×100%=56%,用H2表示I的反应速率=
×100%=56%,用H2表示I的反应速率=![]() =
=![]() mol·L-1·min-1;反应Ⅱ的平衡常数K=
mol·L-1·min-1;反应Ⅱ的平衡常数K=![]() =
=![]() ,故答案为:56%;
,故答案为:56%;![]() ;
;![]() 。
。


科目:高中化学 来源: 题型:
【题目】现需要配制500 mL 1 mol·L-1硫酸溶液。
(1)需量取质量分数为98%、密度为1.84 g·cm-3的浓硫酸________mL。
有如下操作步骤:
①把量好的浓硫酸沿烧杯壁慢慢注入蒸馏水中,并用玻璃棒搅拌溶解。
②把①所得溶液冷却后小心转入500mL容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度线1~2cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面底部与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
⑤将容量瓶塞塞紧,充分摇匀。
请填写下列空白:
(2)操作步骤的正确顺序为______________(填序号)。
(3)本实验必须用到的玻璃仪器有10ml量筒、玻璃棒、烧杯、_________。
(4)下列情况使所配溶液的浓度偏高的是_________
A.某同学观察液面的情况如图所示

B.没有进行操作步骤④;
C.加蒸馏水时不慎超过了刻度线,再吸出一部分水。
D.向容量瓶中转移溶液时(操作步骤②)溶液流到容量瓶外面
(5)若实验过程中出现(4)中D选项情况应如何处理?:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)等质量的二氧化硫和二氧化碳,它们的物质的量之比___,所含原子数之比为___,同温同压下的密度之比为___。
(2)有氢原子数相等的甲烷和氨气(NH3)的质量之比为___。
(3)3.22g的Na2SO4·10H2O溶于水中,要使每100个分子中含有1个Na+,则需要水的质量为___。
(4)同温同压下某容器充满氮气重64g,充满氦气重52g,现在充满某气体重66g,则该气体的摩尔质量为___。
Ⅱ.(1)油画所用颜料含有某种白色铅化物,此颜料置于空气中长时间后就会变成黑色PbS,从而使油画的色彩变暗,若用双氧水H2O2来清洗,则可将PbS变成PbSO4,从而使油画复原。上述清洗反应的化学方程式为PbS+4H2O2=PbSO4+4M(已配平)。
生成物M的化学式为___ ;若发生转移的电子数目4mol时,参加反应的H2O2的质量为___。
(2)在反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O中,氧化剂是___,氧化产物是___,氧化产物与还原产物物质的量之比是___,氧化剂和还原剂的物质的量之比为___,若有36.5gHCl被氧化,则产生Cl2的质量为___。
(3)2.3g的金属钠,在干燥的空气中被氧化后得到固体的质量为3.5g,则反应后固体中氧化钠的质量为___。
(4)配平下列方程式并用单线桥表示电子的转移(不需写出配平过程)___
Cu+HNO3(稀)=Cu(NO3)2+NO↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验。
请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是 (填选项字母)
A.滴定终点读数时,俯视滴定管刻度,其他操作正确。
B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
滴定次数 | 待测液体积 | 标准KMnO4溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 3.00 | 23.00 |
第三次 | 25.00 | 4.00 | 24.10 |
①滴定时,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是
②该草酸溶液的物质的量浓度为_____________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。
参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10-10 | 5.35×10-13 | 1.21×10-16 | 1.12×10-12 | 1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下合成乙烯:6H2(g)+2CO2(g)![]() CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )
CH2=CH2(g)+4H2O(g);已知温度对CO2的平衡转化率和催化剂催化效率的影响如图,下列说法不正确的是( )

A. 生成乙烯的速率:v(N)一定大于v(M) B. 该反应的逆反应为吸热反应
C. 平衡常数:KM>KN D. 当温度高于250 ℃,升高温度,催化剂的催化效率降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数,下列叙述中正确的是( )
A.0.1mol/L NaCI溶液中所含Na+数目为0.1NAB.1mol NH3所含有的原子数为NA
C.标准状况下,22.4L水中所含原子数为3NAD.常温常压下,48g O3所含的原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【题目】生产上用过量烧碱溶液处理某矿物(含Al2O3、MgO),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:

下列有关说法不正确的是
A. 原NaHCO3溶液中c(H2CO3)+c(HCO3-)+c(CO32-)=0.8moL/L
B. a点水的电离程度小于c点水的电离程度
C. a点溶液中存在:c(Na+)+c(H+)=c(AlO2-)+(OH-)
D. 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O=Al(OH)3↓+CO32-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)水的电离平衡曲线如右图所示,若A点表示25 ℃时水的电离达平衡时的离子浓度,B点表示100 ℃时水的电离达平衡时的离子浓度。则100 ℃时1 mol·L-1的NaOH溶液中,由水电离出的c(H+)=________mol·L-1,KW(25 ℃)________KW(100 ℃)(填“>”、“<”或“=”)。

(2)25 ℃时,向水的电离平衡体系中加入少量NH4Cl固体,对水的电离平衡的影响是________(填“促进”、“抑制”或“不影响”)。
已知如表数据。
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7 K2=5.6×10-11 |
(3)25 ℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为____ ___。(填化学式)
(4)25 ℃时,等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,则c(Na+)________c(CH3COO-)(填“>”、“<”或“=”)。
(5)向NaCN溶液中通入少量CO2,反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物W在工业上常用作溶剂和香料,其合成方法如图,下列说法不正确的是

A. M、N、W均能发生加成反应和取代反应
B. N、W组成上相差一个CH2原子团,所以互为同系物
C. 1molM与1molw完全燃烧消耗O2的物质的量相同
D. M苯环上的二氯代物有6种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com