
【题目】[物质结构与性质]
[Zn(CN)4]2–在水溶液中与HCHO发生如下反应:
4HCHO+[Zn(CN)4]2–+4H++4H2O===[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________。
(2)1 mol HCHO分子中含有σ键的数目为____________mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是______________。
(4)与H2O分子互为等电子体的阴离子为________________。
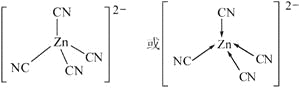
(5)[Zn(CN)4]2–中Zn2+与CN–的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为_____________。

【答案】(1)1s22s22p62s23p63d10(或[Ar] 3d10) (2)3 (3)sp3和sp (4)NH2-
(5)
【解析】试题分析:(1)Zn是30号元素,Zn2+核外有28个电子,根据原子核外电子排布规律可知基态Zn2+核外电子排布式为1s22s22p62s23p63d10;
(2)甲醛的结构式是![]() ,由于单键都是σ键,双键中有一个σ键和一个π键,因此在一个甲醛分子中含有3个σ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
,由于单键都是σ键,双键中有一个σ键和一个π键,因此在一个甲醛分子中含有3个σ键和1个π键,所以在1 mol HCHO分子中含有σ键的数目为3 mol;
(3)根据HOCH2CN的结构简式可知在HOCH2CN分子中,连有羟基-OH的碳原子形成4个单键,因此杂化类型是sp3杂化,—CN中的碳原子与N原子形成三键,则其杂化轨道类型是sp杂化;
(4)原子数和价电子数分别都相等的是等电子体,H2O含有10个电子,则与H2O分子互为等电子体的阴离子为NH2-;
(5)在[Zn(CN)4]2–中Zn2+与CN-的C原子形成配位键,C原子提供一对孤对电子,Zn2+的空轨道接受电子对,因此若不考虑空间构型,[Zn(CN)4]2–的结构可用示意图表示为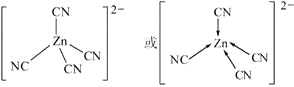 。
。


科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖花落锂离子电池,美英日三名科学家获奖,他们创造了一个可充电的世界。像高能LiFePO4电池,多应用于公共交通。电池中间是聚合物的隔膜,主要作用是在反应过程中只让Li+通过。结构如图所示。

原理如下:(1x)LiFePO4+xFePO4+LixCn![]() LiFePO4+nC。下列说法不正确的是( )
LiFePO4+nC。下列说法不正确的是( )
A.放电时,正极电极反应式:xFePO4+xLi++xe-=xLiFePO4
B.放电时,电子由负极经导线、用电器、导线到正极
C.充电时,阴极电极反应式:xLi++xe-+nC=LixCn
D.充电时,Li+向左移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近在-100℃的低温下合成一种烃X,烃X分子的结构如图所示(图中的连线表示化学键)。下列说法正确的是( )
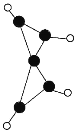
A.充分燃烧等质量的X和甲烷,X消耗的氧气较多
B.X是一种常温下能稳定存在的液态烃
C.X和乙烷类似,都易发生取代反应,不易发生加成反应
D.X既能使溴的四氯化碳溶液褪色又能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A2+3B2 =2AB3在2L的密闭容器中进行,5s后,A2的物质的量增加了0.3mol,则此反应的平均速率可表示为:
A.v (A2)=0.01 mol/(L·s)B.v (B2)=0.08 mol/(L·s)
C.v (AB3)=0.03 mol/(L·s )D.v (AB3)=0.06 mol/(L·s )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于
A.1.7B.2.0C.12.0D.12.4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4种(不考虑立体异构)
的一溴代物都有4种(不考虑立体异构)
B.CH3CH=CHCH3分子中的四个碳原子在同一直线上
C.按系统命名法,化合物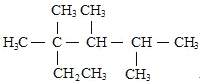 的名称是2,3,4-三甲基-2-乙基戊烷
的名称是2,3,4-三甲基-2-乙基戊烷
D.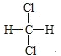 与
与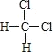 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇的结构简式为![]() 。请回答下列问题:
。请回答下列问题:
①基态镍原子的价电子排布式为________。
②![]() 键,烯丙醇分子中碳原子的杂化类型是__________。
键,烯丙醇分子中碳原子的杂化类型是__________。
(2)乙炔是有机合成的一种重要原料。实验室可用![]() 与水反应得到乙炔。
与水反应得到乙炔。
①将乙炔通入![]() 溶液中生成
溶液中生成![]() 红棕色沉淀。基态
红棕色沉淀。基态![]() 的核外电子排布式为____。
的核外电子排布式为____。
②乙炔与![]() 反应可得丙烯腈(
反应可得丙烯腈(![]() ),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有
),丙烯腈分子中碳原子的的杂化轨道类型是_______,分子中含有![]() 键的数目为___________。
键的数目为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子液体是一种由离子组成的液体,在低温下也能以液态存在,是一种很有研究价值的溶剂。研究显示最常见的离子液体主要由图示正离子和负离子组成:
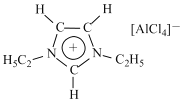
回答下列问题:
(1)按电子排布,Al划分在元素周期表中的______区(填“s”“p”“d”或“ds”),图中负离子的空间构型为____________________。
(2)基态Cl原子的价电子排布图为____________________。
(3)图中正离子有令人惊奇的稳定性, 它的电子在其环外结构中高度离域。该正离子中C原子的杂化方式为_________。该化合物中不存在____(填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键 E.氢键
(4)C、N、H三种元素的电负性由大到小的顺序为 __________,NH3与CH4的中心原子均为 sp3杂化,但是H-N-H 的键角小于H-C-H的键角,原因是________。
(5)AlN是一种陶瓷绝缘体,具有较高的导热性和硬度, 其立方晶胞如图所示,Al原子周围紧邻的Al原子有_____个。已知:氮化铝的密度为dg/cm3, 阿伏加德罗常数为NA,则最近的N原子与Al原子间的距离为_____________pm。
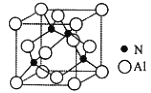
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物 X 分子式为C3H6O,有多种同分异构体。其中之一丙醛(液态)的燃烧热为1815kJ/mol。下列说法不正确的是
A.X 的同分异构体中,含单官能团的共 5 种
B.1mol X 最多能和 1mol H2 加成
C.表示丙醛燃烧热的热化学方程式为:C3H6O(l)+4O2(g) = 3CO2 (g)+3H2O(l) △H=+1815kJ/mol
D.X 的同分异构体其中之一 CH2=CHCH2OH 可以发生取代反应、加成反应、加聚反应、氧化反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com