
某化学兴趣小组利用某废弃的氧化铜锌矿制取活性ZnO实验流程如下:
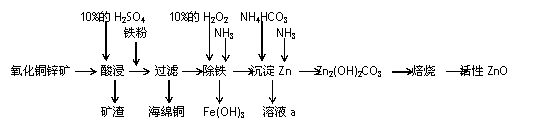
请回答下列问题:
⑴加入铁粉后发生反应的离子方程式为_________________________,_______ _。
⑵甲、乙两同学选用下列仪器,采用不同的方法制取氨气。

①甲同学使用的药品是熟石灰与氯化铵,则应选用装置_______(填写装置代号),生成氨气的化学方程式为_______________________________________;
②乙同学选用了装置B,则使用的两种药品的名称为______________ _。
⑶H2O2的作用是____________________________________________________。
⑷除铁过程中得到的Fe(OH)3可用KClO溶液在碱性环境将其氧化得到一种高效的多功能水处理剂(K2FeO4),该反应中氧化剂与还原剂的物质的量之比为____________。
⑸已知溶液a中含有CO2- 3、SO2- 4两种酸根阴离子,若只允许取用一次样品,检验这种离子存在的实验操作过程为_____________________________
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
下列有关钢铁腐蚀与防护的说法正确的是
A.钢管与电源正极连接,钢管可被保护
B.铁遇冷的浓硝酸表面钝化,可保护内部不被腐蚀
C.钢管与铜管露天堆放在一起时,钢管不易被腐蚀
D.钢铁发生析氢腐蚀时,负极反应是Fe→Fe3++3e-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
A.2.4 g金属镁变为镁离子时失去的电子数为0.1NA
B.1 mol HCl气体中的粒子数与0.5 mol/L盐酸中溶质粒子数相等
C.任何条件下,16gCH4与18 g H2O所含有电子数均为10NA
D.22.4 L的CO气体与1 mol N2所含的电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
除去下列括号内杂质的试剂和方法正确的是( )
A.Fe3+ (Al3+),加过量的氨水,过滤
B.KCl溶液(BaCl2),加入足量K2SO4溶液,过滤
C.CO2 (SO2),饱和碳酸氢钠溶液,浓硫酸,洗气
D.N2 [NO2(主要)、NO],NaOH溶液,浓硫酸,洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述或化学用语书写正确的是( )
A.向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:
Ba2++OH-+H++SO2- 4=BaSO4↓+H2O
B.稀硫酸中加入铁粉:2Fe+6H+=2Fe3++3H2↑
C.FeSO4溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+=2Fe3++2H2O
D.金属铝与氧化镁发生铝热反应:2Al+3MgO 高温 3Mg+Al2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
市场上销售的“84”消毒液,其商品标识上有如下叙述:①本品为无色液体,呈碱性②使用时加水稀释③可对餐具、衣物进行消毒,可漂白浅色衣物。其有效成分可能是( )
A. Cl2 B. SO2 C. NaClO D. KMn04
查看答案和解析>>
科目:高中化学 来源: 题型:
根据反应(1)→(4),可以判断下列4个物质的氧化性由强到弱的正确顺序是( )
⑴Cl2+2KI=2KCl+I2; ⑵2FeCl2+Cl2=2FeCl3;
⑶2FeCl3+2HI=2FeCl2+2HCl+I2,⑷H2S+I2=S+2HI;
A. S>I2>Fe3+>Cl2 B. Cl2>Fe3+>I2>S
C. Fe3+>Cl2>S>I2 D. Cl2>I2>Fe3+>S
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ.测定过氧化的含量,请填写下列空白:
(1) 移取10.00 ml密度为ρ g/mL的过氧化氢溶液至烧杯后全部将其转移到250 ml (填仪器名称)中,加水衡释至刻度,摇匀。移取稀释后的过氧化氢溶液25. 00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。

 MnO4-+
MnO4-+
 H2O2+
H2O2+
 H+=
H+=
 Mn2++
Mn2++
 H2O+
H2O+



(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
Ⅱ.探究过氧化氢的性质
该化学兴趣小组根据所提供的实验条件设计了两个实验,分别证明了过氧化氢的氧化性和不稳定性。(实验条件:试剂只有过氧化氢溶液、氯水、碘化钾演粉溶液、饱和硫化氢溶液,实验仪器及用品可自选。)请将他们的实验方法和实验现象填入下表:
| 实 验 内 容 | 实 验 方 法 | 实 验 现 象 |
| 验证氧化性 | ||
| 验证不稳定性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶转移液体
A.①和② B.①和④ C.③和④ D.①和③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com