
【题目】开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H1=﹣1275.6kJmol-1
②2CO(g)+O2(g)=2CO2(g) △H2=﹣566.0kJmol-1
③H2O(g)=H2O(l) △H3=﹣44.0kJmol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:___。
(2)工业上甲醇利用水煤气合成,反应为CO(g)+2H2(g)=CH3OH(g) ΔH<0。在一定条件下,将1molCO和2molH2通入密闭容器中进行反应,当改变某一外界条件(温度或压强)时,CH3OH的体积分数φ(CH3OH)变化趋势如图所示:

①平衡时,M点CH3OH的体积分数为10%,则CO的转化率为___。
②X轴上a点的数值比b点___(填“大”或“小”)。
③生产甲醇的原料CO和H2来源于:CH4(g)+H2O(g)CO(g)+3H2(g) △H>0,一定条件下CH4的平衡转化率与温度、压强的关系如图1。则T1___T2(填“<”、“>”、“=”,下同);A、B、C三点处对应平衡常数(KA、KB、KC)的大小关系为____。

(3)现以H2、O2、熔融盐Na2CO3组成的燃料电池,采用电解法制备N2O5,装置如图2所示,其中Y为CO2。

写出石墨Ⅰ电极上发生反应的电极反应式___。在电解池中生成N2O5的电极反应式为___。
【答案】CH3OH(1)+O2(g)=CO(g)+2H2O(1) △H=﹣442.8kJmol-1 25% 小 < KC=KB>KA ![]() N2O4+2HNO3﹣2e-=2N2O5+2H+
N2O4+2HNO3﹣2e-=2N2O5+2H+
【解析】
(1)根据盖斯定律![]() 得目标方程式,求得目标方程式焓变;
得目标方程式,求得目标方程式焓变;
(2)①列三段式计算一氧化碳的转化率,②根据方程式系数及反应焓变判断反应的移动方向和温度压强的关系,进而判断,③平衡常数只与温度有关,根据温度比较平衡常数;
(3)判断阴阳极,正负极根据题目信息写出电极反应式即可。
(1)已知:①![]() ②
②![]() ③
③![]() ,根据盖斯定律,
,根据盖斯定律,![]() 可得:
可得:![]() ,
,
故答案为:![]() ;
;
(2)①设平衡时生成甲醇xmol,列三段式: ,根据M点
,根据M点![]() 的体积分数为10%,即
的体积分数为10%,即![]() ,解得x=0.25,故
,解得x=0.25,故![]() 的转化率为
的转化率为![]() ,
,
故答案为:25%;
②![]() ,升温该反应逆向移动,即温度越高甲醇体积分数小,加压该反应正向移动,即压强越大甲醇体积分数越大,由图像可知Y轴代表温度,X轴代表压强,且abcd依次增大,
,升温该反应逆向移动,即温度越高甲醇体积分数小,加压该反应正向移动,即压强越大甲醇体积分数越大,由图像可知Y轴代表温度,X轴代表压强,且abcd依次增大,
故答案为:小;
③该反应为吸热反应,温度越高甲烷转化率越大,故T1<T2;对于吸热反应,温度越高平衡常数越大,且相同温度下平衡常数相同,故KC=KB>KA,
故答案为:<;KC=KB>KA;
(3)石墨Ⅰ电极通入氢气,发生氧化反应生成水,电极反应式为:![]() ;电解池
;电解池![]() 发生氧化反应生成
发生氧化反应生成![]() ,电极反应式为:
,电极反应式为:![]() ,
,
故答案为:![]() ;
;![]() 。
。


 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】5.56gFeSO4·7H2O样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,下列说法不正确的是( )
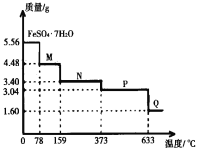
A.温度为78℃时固体物质M的化学式为FeSO4·4H2O
B.取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe2O3
C.在隔绝空气条件下,N得到P的化学方程式为FeSO4·H2O![]() FeSO4+H2O
FeSO4+H2O
D.温度为159℃时固体N的化学式为FeSO4·2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用亚硫酸钠固体和70%的浓硫酸制备SO2气体,反应方程式为Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,请设计一套实验装置,收集一试管干燥的SO2气体。
(1)在下面方框中,A表示由分液漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置、连接胶管不必画出,尾气处理部分必须画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C…;其它可选用的仪器(数量不限)简易表示如下:___

(2)根据方框中的装置图甲,在答题卡上填写下表(可不填满)___
仪器标号 | 仪器中所加物质 | 作用 |
A | 亚硫酸钠、浓硫酸 | 产生SO2 |
(3)某实验小组用如图乙装置测定收集到的气体中SO2的含量,反应管中装有酸性高猛酸钾溶液。
①SO2和酸性高猛酸钾溶液发生反应的离子方程式为:___。
②反应管内溶液紫红色消失后,若没有及时停止通气,则测得的SO2含量___(选填:“偏高”、“偏低”或“无影响”)
③若酸性高猛酸钾溶液体积为V1mL,浓度为cmol/L,量气管内增加的水的体积为V2mL(已折算成标准状况下的体积)。用c、V1、V2表示SO2的体积百分含量为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的衍生物A的化学式为C6H12O2,已知:

又知D不与Na2CO3反应,C和E均不能发生银镜反应,则A的结构可能有( )
A. 1种 B. 2种 C. 3种 D. 4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)主要用作棉纺、造纸业的漂白剂,也可用于食品消毒、水处理等,亚氯酸钠受热易分解。以氯酸钠(NaClO3)等为原料制备亚氯酸钠的工艺流程如下:

(1)ClO2中Cl的化合价为________。
(2)从“母液”中回收的主要物质是________(填化学式)。
(3)“冷却结晶”后需________(填操作名称),该操作用到的玻璃仪器有________。
(4)反应2中转移0.1NA个电子时,生成NaClO2的质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属冶炼的反应原理及方程式书写,正确的是( )
A.2AlCl3(熔融)![]() 2Al+3Cl2↑B.Fe2O3+2Al
2Al+3Cl2↑B.Fe2O3+2Al![]() Fe+Al2O3
Fe+Al2O3
C.Cu2S+O2![]() 2Cu+SO2D.Ag2O
2Cu+SO2D.Ag2O![]() 2Ag+O2↑
2Ag+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数,下列说法正确的是( )
A.由2H和18O所组成的水11 g,其中所含的中子数为4NA
B.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA
C.0.1 mol H3O+中含有的电子数为NA
D.标准状况下,1L乙醇完全燃烧产生CO2分子的数目为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下离子方程式书写正确的是
A.用醋酸除去水垢:2H+ + CaCO3 = Ca2++CO2↑+H2O
B.向NH4HCO3溶液中加入足量石灰水:Ca2+ + HCO3-+OH-= CaCO3↓ + H2O
C.向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3![]() =Al2(CO3)3 ↓
=Al2(CO3)3 ↓
D.侯氏制碱法中NaHCO3的制备:Na+ + NH3 + CO2 + H2O = NaHCO3 ↓ + NH4+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在一容积可变的容器中,反应2A(g)+B(g)![]() 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡向正反应方向移动的是( )
A.均减半B.均加倍C.均增加1molD.均减少1mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com