
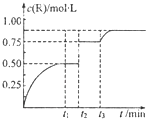
 一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )
一定温度下,将1molN气体充入2L恒容密闭容器中,发生反应:M(g)+N(g)?xR(g)+Q(s),t1时达到平衡.在t2、t3时刻分别改变反应的一个条件,测得容器中气体R的浓度随时间变化如图所示.下列说法正确的是( )| A、该反应方程式中:x=1 |
| B、t1~t3间该反应的平衡常系数均为4 |
| C、t2时刻改变的条件是使用催化剂 |
| D、t3时刻改变的条件是移去少量Q |
| 0.5×0.5 |
| 0.25×0.25 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
A、用惰性电极电解MgCl2 溶液:2Cl-+2H2O
| ||||
| B、用浓盐酸酸化的高锰酸钾溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O | ||||
| C、向NH4Al(SO4)2溶液中逐滴加入过量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+AlO2-+2H2O+NH3?H2O | ||||
| D、向澄清石灰水中滴加同浓度的少量碳酸氢钙溶液:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | X | Y | Z | 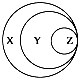 |
| A | 胶体 | 混合物 | 淀粉溶液 | |
| B | 化合物 | 酸性氧化物 | 一氧化氮 | |
| C | 气态氢化物 | 化合物 | 液溴 | |
| D | 强电解质 | 强酸 | 硫酸 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
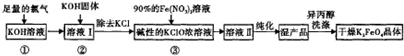
查看答案和解析>>
科目:高中化学 来源: 题型:
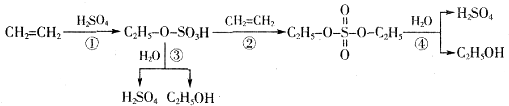
| A、该过程是一种“对环境友好型”工业生产硫酸的方法 |
| B、从以上物质的转化过程可看出硫酸可作乙烯水化法制乙醇的催化剂 |
| C、该过程中①②是加成反应 |
| D、该过程中③④是酯类的水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
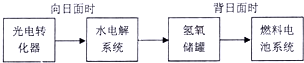
查看答案和解析>>
科目:高中化学 来源: 题型:
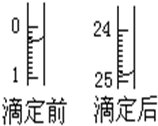 某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.
某烧碱溶液中含有少量杂质(不与盐酸反应),现用中和滴定测定其浓度.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、中性溶液的PH都相等 | ||||
| B、新型净水材料高铁酸钠是生产自来水理想的净水剂和杀菌剂 | ||||
C、
| ||||
| D、△H<0,△S<0的化学反应不能自发进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com