
【题目】实验室用如图装置制备并收集干燥纯净的Cl2。
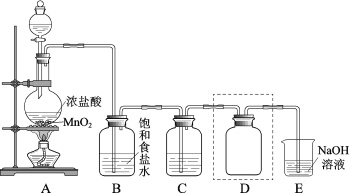
(1)装置A中反应的化学方程式是___。
(2)装置B的作用是__。
(3)装置C中盛放的物质是__。
(4)装置D用于收集Cl2,请将图中装置D的导气管补充完整___。
(5)装置E用于吸收尾气,E中反应的离子方程式是__。
【答案】MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O 除去Cl2中混有的HCl 浓硫酸
MnCl2+Cl2↑+2H2O 除去Cl2中混有的HCl 浓硫酸  Cl2+2OH-=Cl-+ClO-+H2O
Cl2+2OH-=Cl-+ClO-+H2O
【解析】
(1)装置A是用浓盐酸和二氧化锰在加热的条件下制取氯气的装置;
(2)装置B盛有饱和食盐水,用来除去氯气中的氯化氢气体;
(3)通过装置B出来的氯气中含有水,则装置C中盛放的物质是浓硫酸,除去氯气中的水分;
(4)装置D用于收集Cl2,氯气的密度比空气大,收集时,使用向上排空气法,集气瓶内的导管应长进短出;
(5)装置E盛有氢氧化钠用于吸收多余的氯气,氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水;
(1)装置A是用来制取氯气的装置,根据图示浓盐酸和二氧化锰在加热的条件下制取氯气,化学反应方程式为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O,
MnCl2+Cl2↑+2H2O,
故答案为:MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O;
MnCl2+Cl2↑+2H2O;
(2)由于盐酸具有挥发性,从装置A中出来的氯气中混有氯化氢气体,装置B盛有饱和食盐水,用来除去氯气中的氯化氢气体,
故答案为:除去Cl2中混有的HCl;
(3)通过装置B出来的氯气中含有水,则装置C中盛放的物质是浓硫酸,除去氯气中的水分,
故答案为:浓硫酸;
(4)装置D用于收集Cl2,氯气的密度比空气大,收集时,使用向上排空气法,集气瓶内的导管应长进短出,装置图为: ,
,
故答案为: ;
;
(5)装置E盛有氢氧化钠用于吸收多余的氯气,氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,离子反应方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;


科目:高中化学 来源: 题型:
【题目】下图为一定条件下采用多孔惰性电极的储氢电池充电装置(忽略其他有机物)。已知储氢装置的电流效率![]() ×100%,下列说法不正确的是
×100%,下列说法不正确的是
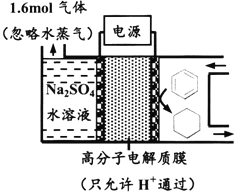
A. 采用多孔电极增大了接触面积,可降低电池能量损失
B. 过程中通过C-H键的断裂实现氢的储存
C. 生成目标产物的电极反应式为C6H6+6e-+6H+===C6H12
D. 若![]() =75%,则参加反应的苯为0.8mol
=75%,则参加反应的苯为0.8mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物是药物生产的中间体, 其结构简式如下图,下列有关叙述不正确的是
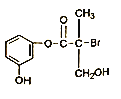
A. 该有机物与浓溴水可发生取代反应
B. 该有机物与浓硫酸混合共热可发生消去反应
C. 1mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH
D. 该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1200℃时,天然气脱硫工艺中会发生下列反应:
H2S(g)+3/2 O2(g)═SO2(g)+H2O(g) △H1
2H2S(g)+SO2(g)═3/2 S2(g)+2H2O(g) △H2
H2S(g)+1/2 O2(g)═S(g)+H2O(g) △H3
2S(g)═S2(g) △H4
则△H4的正确表达式为( )
A.△H4=3/2(△H1-△H2-3△H3)B.△H4=2/3 (3△H3-△H1-△H2)
C.△H4=3/2(△H1+△H2-3△H3)D.△H4=2/3 (△H1+△H2-3△H3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)![]() 4C(g)+6D(g) 在5 L的密闭容器中进行反应,30 min后,C的物质的量增加了 0.30 mol。下列叙述正确的是( )
4C(g)+6D(g) 在5 L的密闭容器中进行反应,30 min后,C的物质的量增加了 0.30 mol。下列叙述正确的是( )
A. 30 min中A的平均反应速率是0.010 mol·L-1·min-1
B. 容器中D的物质的量一定增加了0.45 mol
C. 容器中A、B、C、D的物质的量之比一定是4∶5∶4∶6
D. 容器中A的物质的量一定增加0.30 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由N2O和NO反应生成N2和NO2的能量变化如图所示。若生成0.5molN2,下列说法不正确的是( )

A.反应生成1molN2时转移4mole-
B.反应物能量之和大于生成物能量之和
C.N2O(g)+NO(g)=N2(g)+NO2(g) ΔH=-139kJ·mol-1
D.断键吸收能量之和小于成键释放能量之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究中有很重要的作用。下表是5种元素的相关信息,W、X都位于第三周期。
元素 | 信息 |
Q | 地壳中含量最高的元素 |
W | 最高化合价为+7价 |
X | 最高价氧化物对应的水化物在本周期中碱性最强 |
Y | 焰色试验(透过蓝色钴玻璃)火焰呈紫色 |
Z | 原子结构示意图为: |
(1)Q在周期表中的位置是__。
(2)W的最高价氧化物对应的水化物的化学式是___。
(3)X单质与水反应的离子方程式是__。
(4)金属性Y强于X,用原子结构解释原因:__,失电子能力Y大于X,金属性Y强于X。
(5)下列对于Z及其化合物的推断中,正确的是__(填字母)。
A.Z的最低负化合价与W的最低负化合价相同
B.Z的氢化物的稳定性弱于W的氢化物的稳定性
C.Z的单质可与X和W形成的化合物的水溶液发生置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa时,有以下能量转化图,下列说法不正确的是( )
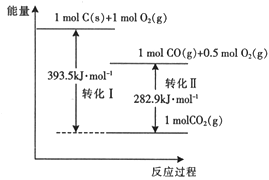
A. 转化Ⅱ的热化学方程式2CO(g)+O2(g)=2CO2(g) △H=-282.9 kJ·mol-1
B. 相同条件下,1mol C(s )和0.5 mol O2(g)总能量高于1mol CO(g)的能量
C. 由C→CO 的热化学方程式2C(s)+O2(g)=2CO(g) △H=-221.2 kJ·mol-1
D. CO2(g)分解为C(s)和O2(g)是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时燃烧生成二氧化碳,反应中放出的热量如图所示。
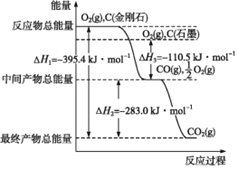
①在通常状况下,金刚石和石墨中____![]() 填“金刚石”或“石墨”
填“金刚石”或“石墨”![]() 更稳定,石墨的燃烧热为____。
更稳定,石墨的燃烧热为____。
②1mol金刚石不完全燃烧生成CO时放出的热量为____。
(2)50mL0.5molL-1的盐酸与50mL0.55molL-1的NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。请回答下列问题:
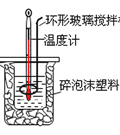
用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会___;用NaOH固体进行上述实验,测得的中和热会___![]() 均填“偏大”“偏小”“无影响”
均填“偏大”“偏小”“无影响”![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com